


Rat는 생리학 연구를 위한 이상적인 모델 동물로, 연구자들은 이미 대량의 순계 rat를 얻었으며, rat의 행동, 세포, 생리학, 생화학, 약리학 및 독성학에 대한 많은 양의 데이터를 축적했습니다. 뿐만 아니라 rat는 인간의 고혈압, 당뇨병, 유방암 및 신경계 질환을 연구하기 위한 이상적인 모델 동물입니다. Rat는 유방암과 같은 종양이 형성되었을 때 호르몬 반응이 사람과 매우 비슷합니다. 어떻게 보면, rat는 현재 인간 질병 연구에 있어서 가장 적합한 모델 동물 중의 하나로, 게놈과 기능을 결합할 수 있는 모델 동물입니다.
또한, rat는 약리학적 연구를 위해 우선적으로 선택된 동물로 심혈관 질환 및 운동 질환의 연구에도 널리 활용되고 있습니다. Rat는 거의 모든 알려진 인간 질병을 simulation하는 데 사용될 수 있으며, rat의 유전적 구조를 이해한다면 연구원들이 질병과 관련된 유전자를 발견하도록 도울 수 있으므로 유전자와 환경이 인간의 건강에 미치는 영향을 더 명확하게 밝혀내게 될 것입니다. Rat는 약의 효력과 안전성 테스트에 널리 사용되어 왔는데, rat의 게놈 서열에 대한 이해는 약물 간섭에 대한 새로운 목표를 제공할 것이며, 이는 신약 개발에 커다란 촉진 작용을 일으킬 것입니다.
Cyagen Knock-Out Rat 서비스의 장점
과배란 rat는 수정된 배아의 비율이 낮을 뿐만 아니라 기형 배아의 비율이 높고, 난세포의 strain과 개체 간 차이가 심하며, rat의 핵막과 원형질막이 더 두껍고 더 탄력성이 있어 주입하기가 더 어려워집니다. 이와 같은 다양한 어려운 문제에 대하여 Cyagen은 제작 과정의 모든 측면을 지속적으로 최적화하고 배란 유도와 수정란 주입의 두 단계에서 획기적인 진전이 이루어졌으며 생산 효율을 크게 향상시켰습니다. 또한, Cyagen의 Rat Knock-Out 기술은 SD Rat 의 유전자를 Knock-Out 할 수 있을 뿐만 아니라 Long evans Rat, F344 Rat, Wistar Rat 및 Brown Norway Rat의 유전자 Knock-Out도 가능하게 합니다.
현재 Cyagen에서 선택이 가능한 rat strains 및 해당 특징은 다음과 같습니다.
(1)SD Rat: 강한 생식력, 빠른 성장 및 강한 질병 저항력을 가지고 있습니다. 자발적인 종양 발생률이 낮고 성호르몬에 대한 민감도가 높습니다. 영양학, 내분비학 및 독성학 등의 연구에 종종 사용됩니다.
(2)Wistar Rat: 성주기가 안정적이고 생식력이 강하며 성장과 발달이 빠릅니다. 천성이 온순하고 질병 저항력이 강하며 자발적인 종양 발생률이 낮습니다. 영양학, 생리학, 약리학, 독성학 및 병리생리학 연구에 널리 사용됩니다.
(3)F344(CDF) Rat: 회전 운동성이 좋지 않고 혈청 인슐린 함량이 낮으며 뇌하수체가 큽니다. 다양한 종양의 이식과 성장을 가능하게 하며, 암 발생 연구에 많이 사용됩니다.
(4)Long evans Rat: 행동학, 영양학, 신경학, 독성학 그리고 안과 쪽의 연구에 널리 사용되고 있습니다. 호흡기 질환에 쉽게 걸리지 않고 흡입마취 시간을 연장해야 하는 외과 수술에 큰 이점이 있습니다.
(5)Brown Norway Rat: 야생 Norway Rat의 변종으로 털은 갈색을 띠며 유전학 연구에 최초로 사용되었습니다. 실험적 알레르기성 뇌척수염(experimental allergic encephalomyelitis) 및 자가면역 복합 사구체 신염(autoimmune complex glomerulonephritis)에 내성이 있습니다.
Targeted Gene Editing-Pro Conventional Knock-Out Rat란 Targeted Gene Editing-Pro Gene Knockout 기술을 통하여 target gene에 대응하는 gRNA와 cas9을 design 및 구축함으로써 target gene 기능 구역을 제거함으로써 target gene이 전신의 모든 조직 및 세포에서 발현되지 않는 래트 모델을 말합니다.
Targeted Gene Editing-Pro Conventional Knockout은 Frameshift mutation, Fragment knockout, Doubel/Polygenic knockout으로 나누어져 있습니다.
Breeding Scheme Of Frameshift Mutation Rat
1. Target gene에 대응하는 gRNA plasmid를 design 및 구축하며 체외에서 RNA로 전사시킨 후 Cas9 mRNA와 같이 원핵에 미세주입한 후에 sequence analysis 결과가 양성인 F0 generation heterozygous 래트를 생산합니다.
2. F0 generation heterozygous 래트를 wildtype 래트와 교배시켜 PCR 및sequence analysis 결과가 양성인 F1 generation heterozygous 래트를 생산합니다.
3. 동일한 F0 generation래트를 통하여 생산한 유전자형이 일치한 F1 generation 래트를 선별하며 성성숙된 후 서로 교배를 시키면 F2 generation 래트를 생산합니다. 그리고 생산된 F2 generation 래트에 대하여 PCR 및sequence analysis를 진행합니다. 이론적으로 F2 generation 래트 중에서 25%는 homozygous 래트이고 50%는 heterozygous 래트이며, 나머지 25%는 wildtype 래트입니다.
Breeding Scheme Of Fragment Knock-Out Rat
1. Target gene의 서로 다른 위치에 대응하는 한쌍의 gRNA plasmid를 design 및 구축하며 체외에서 RNA로 전사시킨 후, Cas9 mRNA와 같이 원핵에 미세주입한 후에 sequence analysis 결과가 양성인 F0 generation heterozygous 래트를 생산합니다.
2. F0 generation heterozygous 래트를 wildtype 래트와 교배시켜 PCR 및sequence analysis 결과가 양성인 F1 generation heterozygous 래트를 생산합니다.
3. 동일한 F0 generation래트를 통하여 생산한 유전자형이 일치한 F1 generation 래트를 선별하며 성성숙된 후 서로 교배를 시키면 F2 generation 래트를 생산합니다. 그리고 생산된 F2 generation 래트에 대하여 PCR 및sequence analysis를 진행합니다. 이론적으로 F2 generation 래트 중에서 25%는 homozygous 래트이고 50%는 heterozygous 래트이며, 나머지 25%는 wildtype래트입니다.
Breeding Scheme Of Doubel/Polygenic Knock-Out Rat
1. 두개의 target gene에각각 대응하는 한쌍의 gRNA plasmid를 design 및 구축하며 체외에서 RNA로 전사시킨 후 Cas9 mRNA와 같이 원핵에 미세주입한 후에 sequence analysis 결과가 양성인 F0 generation polygenicheterozygous래트를 생산합니다.
2. F0 generation heterozygous 래트를 wildtype 마우스와 교배시켜 PCR 및sequence analysis 결과가 양성인 F1 generation double geneheterozygous 래트를 생산합니다.
3. Double geneheterozygous 래트를 서로 교배시킨 후 생산된 F2 generation 래트에 대하여 PCR 및sequence analysis를 진행합니다.
Conditional Knock-Out은 target gene의 한개 또는 여러개의 중요한 exons 양쪽에LoxP site를 삽입함으로써 floxed 래트를 만드는 것입니다. 이 floxed 래트가 cre-expressing 래트와 교배하기 전에 target gene은 완전히 정상적으로 발현되고 tissue-specific cre-expressing 래트와 교배를 진행 후 target gene은 특정 조직 또는 세포에서 knockout될 수 있으며 다른 조직이나 세포에서 정상적으로 발현됩니다.
Breeding Scheme
1. Wildtype 래트와 교배: 양성Targeted Gene Editing-Pro 래트(+/flox)와 wildtype 래트(+/+)를 교배시켜 F1 generationheterozygous 래트(+/flox)를 생산합니다.
2. F1 generationheterozygous 래트(+/flox) 한 쌍을 선별하여 inbreeding시키며 F2 generation homozygous 래트(flox/flox)를 생산합니다.
Targeted Gene Editing-Pro Knockin이란 Targeted Gene Editing-Pro gene knockin 기술을 이용하여 target gene 에 대응하는 gRNA와 donor vector를 design 및 구축하며, Cas9뉴클레아제 가위 작용 및 상동재조합을 통하여 특정된 외부 유전자를 삽입하는 기술입니다. 예를 들어, target gene에 포인트 뮤테이션(인간 유전 질환 모델 시뮬레이션)을 도입하거나, homologous recombination을 통해 reporter gene (EGFP, mRFP, mCherry, mYFP 또는 LacZ 등)을 target gene의 특정 부위에 도입함으로써 reporter gene을 통해 target gene의 발현을 추적할 수 있습니다. 또한, KO/KI가 동시에 발생하도록 래트 자체의 유전자를 reporter gene으로 대체 할 수도 있습니다.
Targeted Gene Editing-Pro Knock-In Rat는 Point Mutation Rat, Fragment Gene Knock-In Rat로 나누어져 있습니다.
Breeding Scheme Of Point Mutation Rat
1. Target gene에 대응하는 gRNA plasmid를 design 및 구축하며 RNA로 전사시킵니다. 그 다음에 돌연변이 위치 정보가 포함된 donor oligo를 합성하여 Cas9 mRNA와 같이 원핵에 미세주입한 후에 sequence analysis 결과가 양성인 F0 generation heterozygous 래트를 생산합니다.
2. F0 generationheterozygous 래트를 wildtype 래트와 교배시켜 PCR 및sequence analysis 결과가 양성인 F1 generation heterozygous 래트를 생산합니다.
3. 동일한 F0 generation래트를 통하여 생산한 knockin 위치가 일치한 F1 generation 래트를 선별하며 성성숙된 후 서로 교배를 시키면 F2 generation 래트를 생산합니다. 그리고 생산된 F2 generation 래트에 대하여 PCR 및sequence analysis를 진행합니다. 이론적으로 F2 generation 래트 중에서 25%는 knockin 위치가 일치한 homozygous 래트이고 50%는 염색체 하나만 knockin된 heterozygous 래트이며, 나머지 25%는 wildtype래트입니다.
Breeding Scheme Of Fragment Gene Knock-In Rat
1. Target gene에 대응하는 gRNA plasmid와 돌연변이 위치 정보가 포함된 donor vector를 design 및 구축하며 mRNA로 전사시킨 후 Cas9 mRNA와 같이 원핵에 미세주입한 후에 sequence analysis 결과가 양성인 F0 generation 래트를 생산합니다.
2. F0 generationheterozygous 래트를 wildtype 래트와 교배시켜 PCR 및sequence analysis 결과 유전자가 무작위로 삽입된 F1 generation heterozygous 래트를 생산합니다.
3. 동일한 F0 generation래트를 통하여 생산한 knockin 위치가 일치한 F1 generation 래트를 선별하며 성성숙된 후 서로 교배를 시키면 F2 generation 래트를 생산합니다. 그리고 생산된 F2 generation 래트에 대하여 PCR 및sequence analysis를 진행합니다. 이론적으로 F2 generation 래트 중에서 25%는 knockin 위치가 일치한 homozygous 래트이고 50%는 염색체 하나만 knockin된 heterozygous 래트이며, 나머지 25%는 wildtype래트입니다.
ROSA26 Knock-In Rat란 Rosa26위치에 어떤 유전자를 삽입하는 Knock-In 래트 모델을 말합니다. (형질 전환 래트 모델이라고도 함). ROSA26 Knock-In 래트 모델은 정확한 삽입 위치를 가질뿐만 아니라, Rosa26은 안전 구역이기 때문에 외부 유전자가 이 위치에 삽입하더라도 다른 유전자의 발현에 영향을 미치지 않을 것입니다. 또한 single-copy 유전자를 삽입함으로 발현량을 더 쉽게 예측할 수 있습니다. Cre-loxP 시스템과 결합하면 특정 조직 및 특정 시간에 외부 유전자를 안정적으로 발현시킬 수 있으며 다목적 Conditional Knock-In Rat를 효율적으로 구축 할 수 있음으로 점점 더 많은 연구자들의 관심을 받고 있습니다.
Principle Of Building:
ROSA26 Knock-In Rat(Targeted Gene Editing-Pro 기술을 기반으로 함)
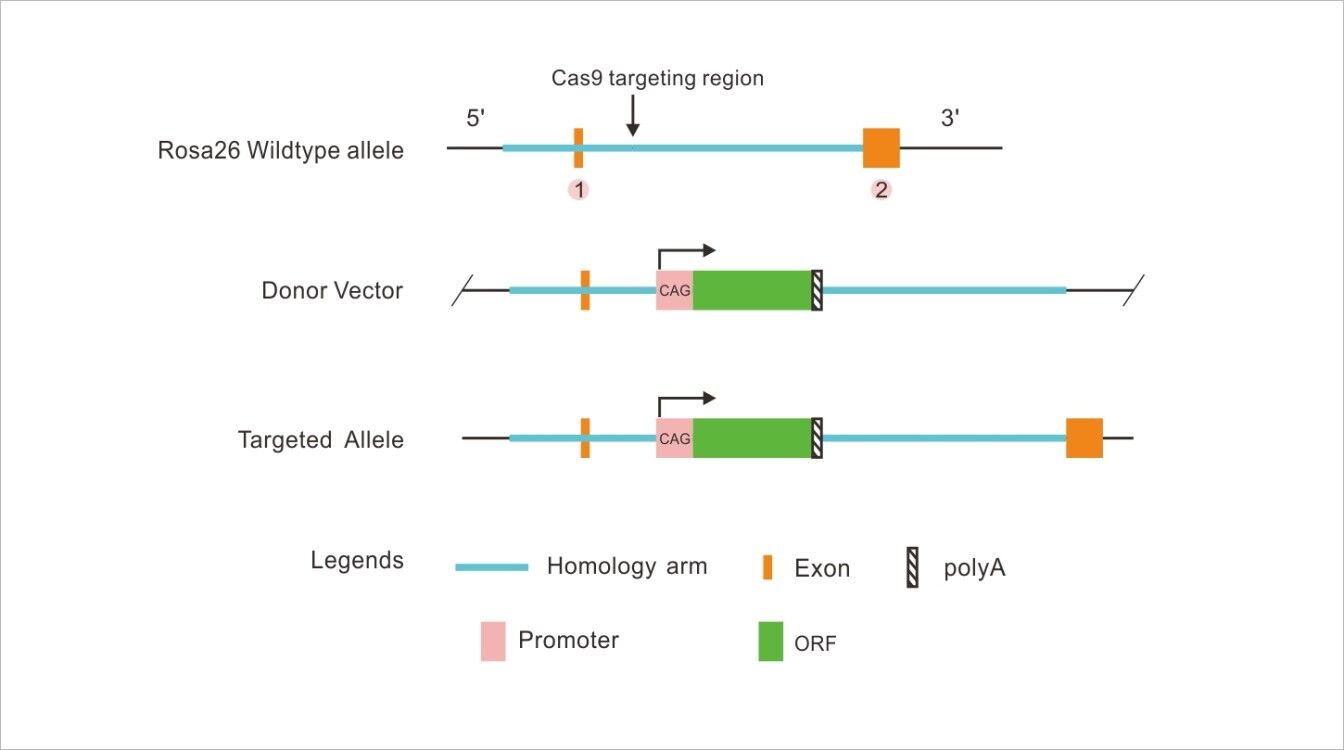
ROSA26 Conditional Knock-In Rat(Targeted Gene Editing-Pro 기술을 기반으로 함)
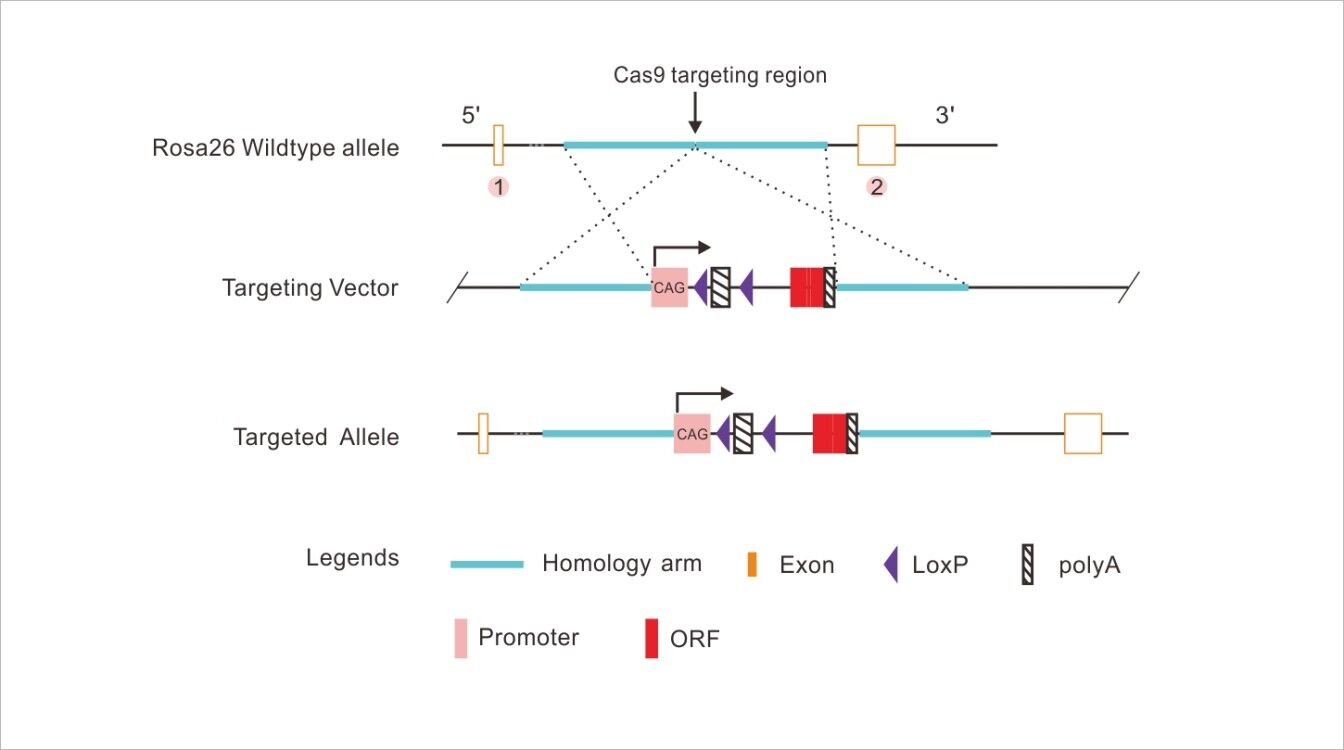
기술 장점:
1. 외부 유전자의 재조합 위치가 확정됨으르써 발현에 더욱 유리합니다.
2. Cre-loxP시스템과 결합하면 외부 유전자를 특정 조직 및 특정 시간에 발현시킬 수 있습니다.
Rosa26은 고전적인 유전자 삽입 위치로, Rosa26 locus에 대한 연구가 많지만 다중 유전자 삽입 래트를 제작할 때 다른 적합한 삽입 위치가 여전히 필요합니다. H11(Hipp11)은 또 다른 선택 가능한 삽입 위치이자 하나의 안전 구역으로, 이 위치에 삽입된 유전자는 다른 유전자의 발현에 영향을 미치지 않으며, 또한 이 삽입된 유전자의 발현은 주변 구역의 영향을 받지 않습니다.
H11은 래트 11번 염색체에 있으며, 두 유전자 Eif4enif1과 Drg1 사이에 위치한 하나의 유전자로, 2010년에 Hippenmeyer S.에 의해 발견되었고 H11에 통합된 외부 유전자가 안정적이고 효율적으로 발현될 수 있습니다. Targeted Gene Editing-Pro 유전자 편집 기술을 이용하여 외부 유전자 fragment를 래트 H11 위치에 삽입할 수 있습니다. Rosa26과 비교할 때, H11은 옆에 있는 프로모터의 영향을 받지 않는다는 장점이 있기 때문에 외부 유전자 발현에 더 적합합니다. loxp 시스템과 결합하면 Tissue-specific 래트 모델을 구축할 수 있습니다.
Principle Of Building:

기술 장점:
1. 안정적이고 후대의 발현이 일치합니다.
2. 실용적이고 유전자 A가 Rosa26 위치의 과발현 및 유전자 B가 H11 위치의 과발현을 동시에 이루어질 수 있습니다.
3. 경제적이고 F1 generation부터 실험 진행이 가능합니다.