

망막색소변성은 시야결핍, 야맹, 심지어 실명의 임상증상이 있어 환자의 일상생활에 심각한 영향을 미치는 발병률이 높은 안과질환이다.환자에게 부정적인 감정을 심어 주기도 쉽다.RPGR 유전자의 병원성 돌연변이는 X염색체 연쇄유전망막색소변성(XLRP)을 일으키는데 XLRP는 발병이 빨라 시력손상이 심하다는 특징이 있다.
RPGR 유전자 소개
RPGR 유전자는 X염색체 연쇄 유전망막색소변성(XLRP) 관련 유전자에 중요한 역할을 하는 유전자 중 하나다. 인간 RPGR 유전자는 X염색체의 짧은 팔(Xp21.1)에 위치하며 최소 10종의 선택적 전사본을 표현할 수 있고 이 중 5종은 단백질을 코딩할 수 있다. 인간 RPGR의 두 가지 주요 선택적 스플라이싱 스크립트(Alternative splicing transcripts)의 단백질은 이미 연구 성숙되어 있으며, RPGREx1-19와 RPGRORF15를 포함한다.
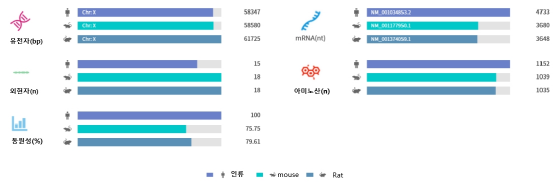
그림 1.RPGR의 유전자 관련 정보
RPGREx1-19는 815개의 아미노산 잔기를 함유하고 있으며 N단에는 6개의 완전한 RLD 구조역이 포함되어 있으며, C단에는 이소펜디엔화(isoprenylation)수식구조(CAAX)로 망막을 포함한 다양한 조직에 널리 표현되어 있다.
RPGRORF15는 1152개의 아미노산 잔기를 함유하고 있으며, 1-14번 외현자와 일부 ORF 외현자에 의해 부호화되어 주로 망막에 발현된다.외현자는 RPGR 유전자 제15호 외현자와 일부 제15호 내함자를 포함하고 있으며, C단에는 고도로 중복되는 글루탐산-글리신(Glycine) 서열이 있어 RPGR 유전자의 한 돌연변이 열점이다. 이 지역서열 돌연변이에 따른 질환은 XLRP의 약 63%를 차지한다.ORF15 돌연변이로 인한 질병은 비교적 온화하다. 돌연변이가 RLD에 있을 때 임상적으로 심각한 증상을 보인다. RP의 경우 1015%가 RPGR 유전자 돌연변이에 의해 발생하지만 XLRP의 경우 70%-90%에 이른다. 대부분의 여성환자의 증상은 비교적 경미하며, 이 현상은 X 염색체의 무작위 불활성화와 관련이 있다. RPGR 단백질은 RPGRIP1과 CEP290 단백질과 상호작용할 수 있으며, 섬모문(Phylum Ciliata) 관련 기능과 관련이 있어 단백질 이송 조절에 관여할 수 있다.
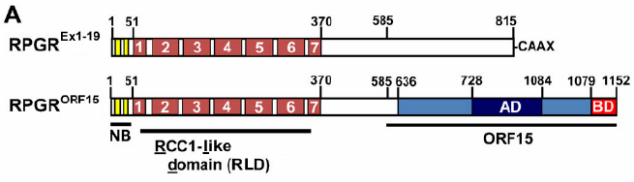
그림2. RPGR 유전자 두 가지 전사본의 차이[6]
RPGR 관련 질환 소개
시력장애는 수많은 사람들의 생활에 영향을 끼친다. 망막변성(retinal degeneration)은 망막 퇴화로 인한 질병으로 망막색소변성(retinitis pigmentosa, RP)이 가장 흔한다. 망막색소변성(retinitis pigmentosa, RP)은 일종의 원추세포(cone cell)이다. 망막 색소 변성 (retinitis pigmentosa, RP) 은 원추세포 (cone cell), 간상세포 (rod cell) 및 망막 색소 상피 세포 (retinal pigment epithelium) 를 포함한 망막 퇴행성 질환이다. 명확한 발병 원인 유무에 따라 다른 전신증상을 합병할지 여부에 따라 원발성/계발성 RP 와 증후군/비증후군 RP 로 나눌 수 있다. 유전자 치료는 원발성 비증후군형 RP가 주목되는데 X염색체 연쇄유전망막색소변성(XLRP)이 일찍 발병해 가장 심각한 손상을 입힌다는 특징이 있는데 RPGR은 XLRP 관련 유전자에 중요한 역할을 하는 유전자다.
RP는 지역별로 유병률 차이가 있어 세계적으로 약 1/4000(1/9000-1/750) 정도이며, 2013년 중국 화북지역 유병률 조사에서는 1/4000을 기록하였다. RP는 주로 진행성 시야 결손, 야맹을 일으키며 중심 시력을 서서히 손상시켜 결국 실명을 초래하고 환자의 일상생활에 심각한 지장을 초래하며 낙담, 불안, 우울, 근심, 공포 등 부정적인 감정을 갖기 쉽다. RP의 대표적인 임상증상은 야맹(nyctalopia)/암적응기능(dark adaptation, DA) 저하와 진행성 시야결손이며, 질환의 진행에 따라 중심시력이 점차 손상되면서 일부 환자는 색각장애(dyschromatopsia), 섬광감(photopsia), photophobia와시환각(visual hallucination)을 동반하기도 한다.
RPGR 유전자 녹아웃마우스
현재 비교적 많이 쓰이는 XLRP 동물모델은 천연 RPGR 돌연변이를 가진 생쥐와 두 가지 유전자공학 생쥐 모델이다.
연구진은 4-6번 외현자(expressed region)를 하나의 항생제 선별 표기로 대체하는 방식으로 구축한 Rpgr 녹아웃 마우스 모델을 보도했다. 유전자 녹아웃 마우스는 초기에 RPGR의 부재로 인해 시단백질이 안쪽으로 잘못 위치하게 되고 GFAP 단백질이 올라가 망막변성을 일으키기도 한다. 6월령 유전자는 마우스의 감광세포가 현저히 감소해 망막 기능이 떨어졌다. 망막 전위도 (ERG) 결과 암시와 명시 진폭이 각각 약 25%, 약 30% 감소한 것으로 나타났다.
또 연구진은 조건적인 녹아웃 모델 Rpgr-cko 모델을 보도했다. 이 마우스는 근단 프로모터(Promoter)와 1 번 외현자(expressed region)를 조건부로 제거함으로써 구축됐다. 이 모델 역시 두 가지 RPGR 전사본 모두 영향을 받고 있다. 유전자녹아웃 마우스를 6 주령때 간상세포 (rod cell)와 원추세포 (cone cell)의 ERG 반응이 약 40% 감소했고, 13 월령에는 외핵층 (ONL) 의 후단이 눈에 띄게 줄었다.
이 외에도 연구진은 ORF15에서 32개의 염기가 중복되는 XLRP를 자발적으로 발생시키는 Rd9 마우스에 대해서도 보도했다. 108 개의 아미노산이 부족한 단백질을 생산할 수 있다. 해당 품목은 RPGREx1-19에 영향을 미치지 않다. 그러나 RPGREx1-19는 ORF15의 부재를 보상하는 기능이 없으며, 그 외에 Rd9/Y 수컷 생쥐와 Rd9/Rd9 암컷 생쥐는 동일한 표형을 가지고 있으며 발병은 비교적 이른 편이다. 망막기능의 저하는 연령의존성으로 ERG진폭이 점차 상실되고 Cone protein가 내부부분으로 잘못 위치하며 12월령에는 ONL 두께가 감소한다.
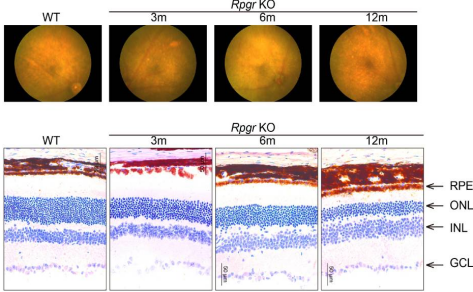
그림3. Rpgr-KO 생쥐에서 광감수기의 퇴화. 안저 사진에서 관찰되는 3월령 쥐의 망막 안저에 여러 개의 황백색 반점이 생겼고 감광기 퇴화와 함께 이 반점들이 더 커지면서 점차 합쳐졌다. 12월이 되면 얼룩은 성긴 대신 색소침착이 뚜렷해진다. 슬라이스 결과, 3 월령에 Rpgr 은 쥐의 망막 형태를 WT 쥐의 망막 형태와 맞먹는 것으로 나타났다. 12 월령에는 Rpgr 이 쥐 감광세포 건물을 두드려을 줄였다[1] .
결론
Rpgr마우스 기능 상실로 인한 망막 색소 변성은 중요한 임상적 의의를 가지고 있으며, 이 유전자에 대한 심도 있는 연구는 망막 색소 변성의 발병 메커니즘을 탐구하는 데 도움이 되며 안과 질환 치료의 새로운 방법에 대한 연구에도 사용될 수 있다.
Cyagen는 유전자 녹아웃 마우스, 조건성 녹아웃 마우스 및 해량 돌연변이 위치 마우스 품계를 망라하여 강력한 데이터베이스로 보다 편리한 경험을 선사하며, 연구자들이 Cyagen웹 사이트의 AI Knock-Out Mouse Model eBank에서 온라인으로 유전자 편집 방안을 조회하고 설계하고 최적화하여 연구 데이터와 성과를 비교하고 주문 상담을 할 수 있다.
Cyagen은 RPGR 완전성 녹아웃마우스와 RPGR 조건성 녹아웃마우스를 제공할 수 있다.
참고 문헌:
1. Hu S, Du J, Chen N, Jia R, Zhang J, Liu X, Yang L. In Vivo CRISPR/Cas9-Mediated Genome Editing Mitigates Photoreceptor Degeneration in a Mouse Model of X-Linked Retinitis Pigmentosa. Invest Ophthalmol Vis Sci. 2020 Apr 9;61(4):31. doi: 10.1167/iovs.61.4.31. PMID: 32330228; PMCID: PMC7401909.
2. Martinez-Fernandez De La Camara C, Cehajic-Kapetanovic J, MacLaren RE. RPGR gene therapy presents challenges in cloning the coding sequence. Expert Opin Biol Ther. 2020 Jan;20(1):63-71. doi: 10.1080/14712598.2020.1680635. Epub 2019 Oct 20. PMID: 31612744; PMCID: PMC7104355.
3. Martinez-Fernandez De La Camara C, Nanda A, Salvetti AP, Fischer MD, MacLaren RE. Gene therapy for the treatment of X-linked retinitis pigmentosa. Expert Opin Orphan Drugs. 2018 Feb 27;6(3):167-177. doi: 10.1080/21678707.2018.1444476. PMID: 30057863; PMCID: PMC6059358.
4. Kortüm F, Kieninger S, Mazzola P, et al. X-Linked Retinitis Pigmentosa Caused by Non-Canonical Splice Site Variants in RPGR. Int J Mol Sci. 2021;22(2):850. Published 2021 Jan 16. doi:10.3390/ijms22020850
5. Schmid F, Glaus E, Cremers FP, Kloeckener-Gruissem B, Berger W, Neidhardt J. Mutation- and tissue-specific alterations of RPGR transcripts. Invest Ophthalmol Vis Sci. 2010 Mar;51(3):1628-35. doi: 10.1167/iovs.09-4031. Epub 2009 Oct 15. PMID: 19834030.
6. Patil H, Guruju MR, Cho KI, Yi H, Orry A, Kim H, Ferreira PA. Structural and functional plasticity of subcellular tethering, targeting and processing of RPGRIP1 by RPGR isoforms. Biol Open. 2012 Feb 15;1(2):140-60. doi: 10.1242/bio.2011489. Epub 2011 Dec 30. PMID: 23213406; PMCID: PMC3507198.




영업일 기준 1-2일 내에 답변해 드리겠습니다.