

녹내장에 대해 얼마나 알고 있나요?
불가역적 피해를 주는 스텔스 시력 '킬러'
녹내장(glaucoma)은 시유두의 위축 및 함몰, 시야결손 및 시력저하를 공통적으로 특징으로 하는 질환이다. 병리성 안압이 높아지고 시신경이 혈액공급이 부족한 것은 그 발병의 원발 위험요인이며 시신경의 스트레스 손상에 대한 내성은 녹내장의 발생과 발전과도 관련이 있다. 사람의 눈의 aqueous humor circulation에 어떤 고리가 방해되면 안압이 높아져 녹내장이 생길 수 있다. 녹내장은 인류의 3대 맹안병 중 하나로 전체 발생률은 1%이며 45세 이상은 2%다. 임상상 녹내장은 원인, 방각(Angle of anterior chamber, 각막과 홍채 사이의 협각), 안압기록법(tonography)등에 따라 원발성, 계발성, 선천성 등 3가지로 분류된다.
인용: 희귀질환 데이터센터 RDDC(https://rddc.tsinghua-gd.org/details/disease?disease=xn3Mrm)
속발녹내장은 어떤 눈병이나 전신 질환이 정상적인 aqueous humor circulation을 방해하여 발생하는 것으로, 예를 들어 눈 외상으로 인한 녹내장, 신생혈관성 녹내장, 홍채 모양체염 속발녹내장(iridocyclitis secondary glaucoma), 당피질 호르몬성 녹내장(glucorticoid induced glaucoma GIG) 등이 있다. 그 원인도 비교적 명확한다. 선천성 녹내장은 배아의 발육 이상, 방각(Angle of anterior chamber) 구조의 선천적 변이로 인한 것이다.

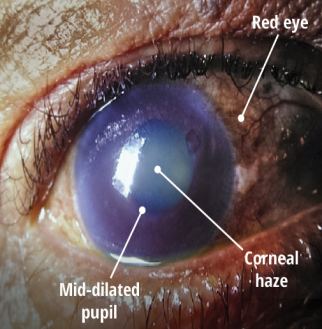
acute angle-closure glaucoma의 임상 표현 (인용:Health Plus;Du Toit N et al, 2013)
질병 증상과 발병 기전의 관련
신생혈관성 녹내장(NVG)은 주로 각종 병인에 의해 망막에 혈액 부족과 산소 결핍이 나타나며 안부에 신생혈관 증식, 안압 너무 높다 등의 문제가 생겨 유발되는 일종의 녹내장 질환이다. 비가역적인 특징을 갖고 있어 한번 걸리면 실명 가능성이 높고 장기간 눈과 두부 통증에 시달릴 수 있다[1].
원발성 폐각 녹내장(primary angle closure glaucoma, PACG)은 방각이(Anterior chamber angle) 닫히고 안압이 높아지며 녹내장성 시신경병변이 특징지어지며 아시아 지역의 비가역성 실명의 주요 원인이다. 원발성 개각 녹내장(primary open-angle glaucoma)과 달리 좁은 눈 앞부분과 앞방각(Anterior chamber angle) 구조는 PACG의 기본 해부학적 특징이며 앞방각(Anterior chamber angle)이 점차 좁아지고 닫히는 과정이 상당히 복잡하여 여러 가지 요소가 관련되어 있다[2].
원발성 개각 녹내장(primary open angle glaucoma, POAG)은 시신경 손상과 시야 결손을 주요 발현으로 하는 비가역치맹성 눈병으로 본질은 망막신경절세포(retinal ganglion cell, RGC) 손상이다. 기계학파는 안압이 시신경이 견딜 수 있는 한계를 넘어섰다고 보고 시각신경 체판(optic nerve cribriform plate)의 구조를 바꿔 신경섬유의 기계적 손상을 초래했다. 한 걸음 더 나아간 연구 결과 시신경 축삭형질(optic nerve axoplasm) 수송이 체판 영역에서 막혔다. 축삭막은 미토콘드리아를 이용하여 ATP효소를 생성하지 못한다. 축돌기는 대사 문제로 인해 단백질 생성과 이동이 감소하고 세포 기능이 손상되어 자발적으로 시들어 버린다. 혈관학설에서는 혈관경련에 의한 관개 부족이 POAG 발병의 주요 원인이라고 보고 있다[3].
흔히 볼 수 있는 녹내장 동물 모델을 점검
● spontaneous animal model
자가발형 녹내장 동물모델(spontaneous animal model)은 동물이 자발적으로 생산(유전)하거나 인위적으로 유전자 변형(유전자 변형)해 얻는 것으로 녹내장 전임상 체내 연구에 중요한 가치를 지닌다.
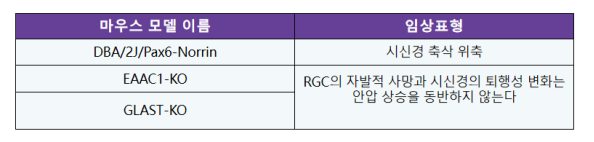
대표적인 자가발형 녹내장 유전자 마우스 모델
● DBA/2J/Pax6-Norrin
DBA/2J 마우스는 배경정보가 가장 풍부한 마우스 모델 중 하나로 인간의 녹내장과 많은 유사점을 가지고 있으며, 연령 의존성 유전성 고안압 녹내장 모델로서 녹내장 연구에 널리 사용된다. 앞방(Anterior Chamber) 이상(앞방심화, 각막부종 등), 홍채 위축, 홍채 외주 유착, 색소분산으로 안압이 약 8월령부터 높아지는 전형적인 녹내장 손상 특징을 가지고 있다. 하지만 다른 생쥐 간 손상 정도가 RGC한 차이를 보인다. 연구에 따르면 망막에서 Norrin을 표현한 유전자 변형 마우스 (Pax6-Norrin) 가 DBA/2J 쥐와 교잡해 DBA/2J/Pax6-Norrin 마우스를 받았다, 1세 DBA/2J/Pax6-Norrin 그룹 생쥐의 시신경 축삭 생존율은DBA/2J 그룹보다 유의하게 높았다. 이 연구는 녹내장 치료를 위한 새로운 타깃을 제공한다. 유전자 변형 녹내장 동물의 주요 장점은 개체 간 안압 상승, 망막과 시신경의 손상 등의 반응이 더 일치해 개체 차이가 적다는 것이다. 더 중요한 것은 유전자 변형 동물의 사용이 질병을 일으키는 유전자자리 간의 상호작용을 식별하는데 도움을 준다는 점이다.
● EAAC1-KO和GLAST-KO
자가발형 고안압 녹내장 모델 외에도 자발적 정상 안압 녹내장(normal tension glaucoma, NTG) 마우스 모델도 연구 보고되었다. 글루타메이트/아스파르트산 수송체(glutamate/aspartate transporter, GLAST)와 흥분성 아미노산 운반체 1(excitatory amino acid carrier 1, EAAC1)의 결실은 RGC의 자발적 사망과 시신경의 퇴행성 변화를 일으킬 수 있으며 안압 상승을 동반하지 않으며 병리 과정은 NTG와 유사한다.
Harada 등은 GLAST 녹아웃 마우스, EAAC1 녹아웃 마우스, 시신경단백질 E50K 녹아웃 마우스, DBA/2J 마우스, 실험적인 유도 모델 등 현재 구축된 다양한 녹내장 동물 모델을 정리하고 각각의 장점과 한계를 분석했다. 그 중 GLAST 녹아웃 마우스, EAAC1 녹아웃 마우스와 시신경단백질 E50K 녹아웃 마우스는 RGC 변성이 발생했지만 안압 발현은 정상이었다. 이 마우스들의 망막 변성은 3~5 주령으로 시작되며, 인간 녹내장 예상보다 더 빠른 시간 프로세스을 가지고 있다. 고안압모델의 연구결과는 NTG에도 유용하며 NTG모델과 고안압모델의 치료결과를 종합적으로 고려하여 비안압요인에 대한 새로운 치료법 개발을 촉진할 수 있다.
인용: 희귀질환 데이터센터 RDDC(https://rddc.tsinghua-gd.org/details/disease?disease=xn3Mrm)
● 유도형 동물모델
자가발형 유전자 모델링 외에도 녹내장 연구에서는 유도모델을 사용하는데, 구체적인 유도방식은 유인에 따라 크게 6가지로 나눌 수 있다. 앞방에 특정물질 주입, 스테로이드 유도, 레이저 광응방수(aqueous humor ) 유출 통로, 상공막 정맥(scleral vein)주사 고삼투 생리식염수, 레이저, 소작 또는 상공막 정맥 결찰, 환상각 공막 가장자리 봉합 등 포함한다[4].
유전자 치료: 녹내장 진료의 새로운 전략
최근 일련의 안질환의 잠재적 유전요인이 이미 검증되었으며 관련 동물모델의 개발도 임상전 연구에 중대한 돌파구를 마련하여 점점 더 많은 유전자 치료법이 녹내장의 표적치료에 응용되고 있다.
(1) 실험 생각 설계 : 섬모체(The ciliary body) 속 Aqp1 유전자를 제거하여 안압을 낮춘다
(2) 표적형 섬모상피(ciliary epithelium) AAV 혈청형 선택 및 검증
(3) 바이러스 패키징
(4) 체외 녹아웃 능력의 검증
(5) 바이러스 주사와 체내 약효 검증(안압 측정, 신경절 세포 계수, 구조 스캔, 냉동 슬라이스 등)
AAV를 이용하여 CRISPR-Cas을 전달하여 섬모체 내 아쿠아포린1 (Aqp1)을 파괴한다. 아쿠아포린1 (Aqp1)은 인체에서 널리 발현되는 수전송 막단백질 가족으로 Aqp1이 부족한 유전자 변형 마우스는 안압이 낮은 것으로 밝혀졌는데, 이는 유입 감소와 방수 형성의 감소로 인한 것이다.
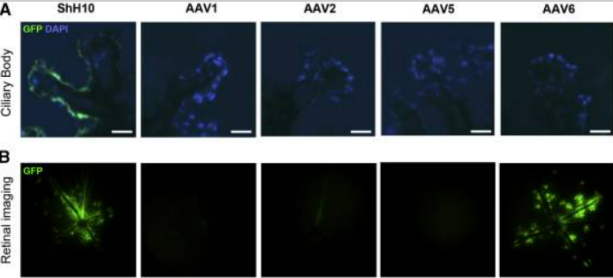
AAVShH10 혈청형이 유리체내 주사 후 효과적으로 섬모체 상피를 전도하는 것을 검증한다
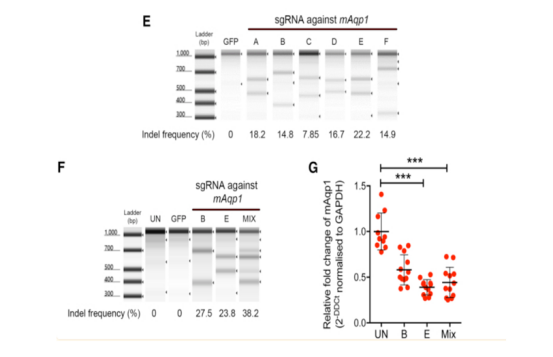
AAVShH10에 탑재된 CRISPR-Pro이 체외에서 mAqp1 유전자를 효과적으로 녹아웃할 수 있음을 검증한다
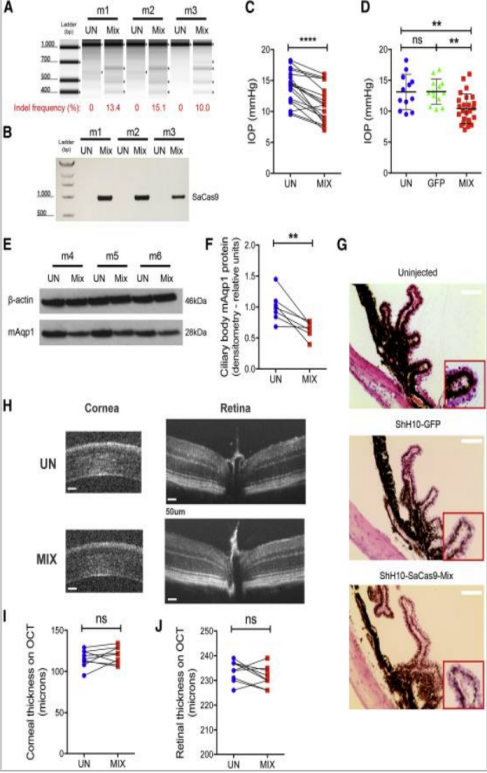
AAV 투여 후 정상 생쥐의 안압을 낮추고, 섬모체(Ciliary body) 모양 변화 없이 체내 실험으로 검증
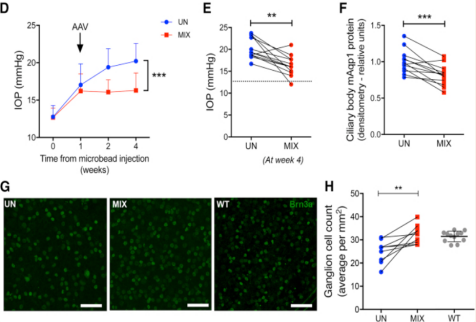
모델링을 유도하는 녹내장 생쥐에서 동일한 안압강하 효과를 낼 수 있으며 신경세포가 손실되지 않도록 보호
이와 함께 Cyagen는 안과 유전자 치료가 오랫동안 직면한 다양한 어려움을 해결하기 위해 안과 유전자 치료의 장을 적극적으로 마련하고 있다. 첨단 미세화 소동물 안과 기기 설비와 베테랑 전문 인력을 매칭하여 고객에게 전임상 표준화된 안과 유전자 치료 연구 전반의 서비스를 제공하기 위해 노력하고 있다. 더 많은 유전자 치료법이 임상시험에 들어가 선천적으로 실명된 사람들이 하루빨리 빛을 볼 수 있도록 도와주기 바란다. 86 20-31601779로 전화하시거나service-apac@cyagen.com 온라인으로 문의해 주시기 바랍니다.
참고 문헌:
● 马万秋.新生血管性青光眼的治疗进展[J].中国城乡企业卫生,2022,37(03):30-32.DOI:10.16286/j.1003-5052.2022.03.011.
● 柴永琦,关立南,高维奇.原发性闭角型青光眼前房角影像学研究进展[J].医学综述,2021,27(16):3268-3273.
● 唐静,邓平,王琼,陈晓明.原发性开角型青光眼发病机制的研究进展[J].眼科新进展,2020,40(06):587-592.DOI:10.13389/j.cnki.rao.2020.0135.
● 宋硕,孟永,李华.青光眼动物模型在青光眼研究中的应用[J].南京医科大学学报(自然科学版),2021,41(12):1850-1855.
● WuJ,BellOH,CoplandDA,etal.GeneTherapyforGlaucomabyCiliaryBodyAquaporin1DisruptionUsingCRISPR-Pro.MolTher.2020;28(3):820-829.




영업일 기준 1-2일 내에 답변해 드리겠습니다.