

Cyagen 칼럼 <Gene of the Week>는 매주 인기 연구 분야에 따라 유전자 하나를 소개해 드리며, 유전자 기본 정보, 연구 개황과 응용 배경 등을 자세히 소개하며 과학 연구의 효율성 향상에 도움을 드립니다. 각계의 지속적인 관심을 부탁 드립니다. 오늘 설명하고자 하는 주인공은 유전자 PTEN입니다.
PTEN은 지금까지 첫번째로 발견된 이중 특성 포스파타제 활성을 갖는 종양 억제 유전자이고 지질 포스파타제 및 단백질 포스파타제의 이중 특이성을 가지며 세포내 다중 신호 전달 경로의 조절에 중요한 역할을 합니다. 발견된 이래, 많은 학자들의 관심을 끌고 있습니다. PTEN 지질 포스파타제의 활성은 포스파티딜이노시톨 트리포스페이트(PIP3)를 탈인산화하여 포스파티딜이노시톨 디포스페이트로 전환해 불활성화한 다음 Pl3K/AKT 경로를 억제하고 세포 성장을 억제하며 세포 주기를 조절할 수 있습니다. 암세포에서 PTEN 기능의 손실은 거의 항상 PIP3의 축적과 관련 AKT 신호의 활성화로 이어집니다. 암에서 PI3K 경로 이펙터의 다운스트림 활성화는 PTEN 결실의 가장 중요한 징후입니다. 그러나 PTEN 결실은 또한 Ras-MAPK, Wnt/β-catenin, Notch, Hippo 경로를 포함한 PIP3 종속 신호를 통해 여러 경로를 활성화하는 것이 입증되었습니다.
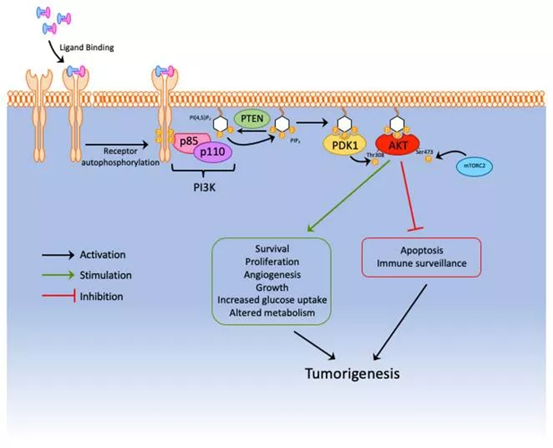
그림1. PTEN은 PI3K 경로와 AKT의 다운스트림 발암성 신호를 억제합니다. PTEN은 PIP3에 대한 인산화를 통하여 PDK1이 AKT를 활성화하는 것을 방지함으로서 종양의 발생을 예방합니다.
PTEN-PI3K 축이 이미 잘 확립되어 있지만 PTEN에 들어갈 수 있는 조절 메커니즘이 많이 있으며 PTEN이 작동하도록 할 수 있는 다운스트림 메커니즘이 많이 있어 암에서 PTEN 신호의 복잡성이 끊임없이 증가합니다. 이러한 메커니즘 중에서 번역 후 변형(PTM) 및 단백질-단백질 상호작용(PPI)이 PTEN의 안정성, 활성 및 위치를 정확하게 제어할 수 있음이 입증되었습니다. 점점 더 많은 데이터에 따르면 단백질 포스파타제 활성과 포스파타제 비의존적 기능은 모두 PTEN를 매개로 하는 종양 억제에서 역할을 합니다. 결론적으로, PTEN 신호 전달과 관련된 새로운 경로에 대한 설명을 통하여,우리는 종양 형성을 예방하는 PTEN의 역할을 더 깊이 이해하고 인식 할 수 있습니다.
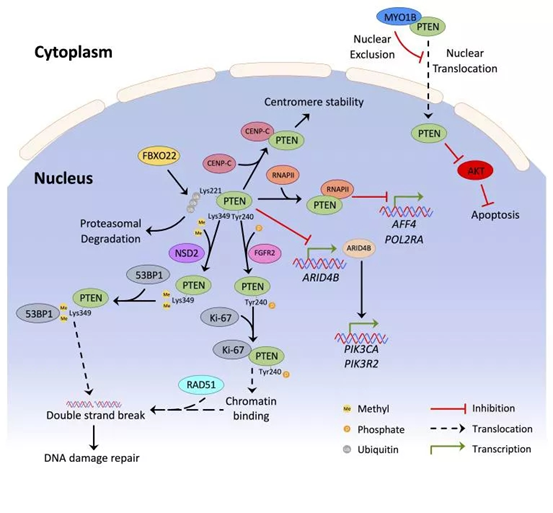
그림2. 세포핵에서 PTEN 신호 전달의 복잡성.
종양 형성에서 PTEN의 중요성 때문에, 종양 형성을 촉진하는‘PTEN 경로'의 잠재적 메커니즘을 명확히 하여 암 예방 및 치료에 대한 잠재적 치료 방법을 제공하기 위하여 복잡한 유전자 조작 마우스 모델(GEMM)을 이미 많이 설계하었습니다.
일반적으로 PTEN은 작업 수준과 그 결과 또는 목표에 따라 세 가지 범주로 나눌 수 있습니다:
(1) PTEN의 하향 조절은 단독으로 또는 다른 종양 억제 유전자의 기능 상실 또는 종양 유전자의 기능 획득과 함께 암 진행을 가속화할 수 있습니다.
(2) PTEN의 발현 및 기능 증가.
(3) 암과 관련된 PTEN 돌연변이 마우스 모델.
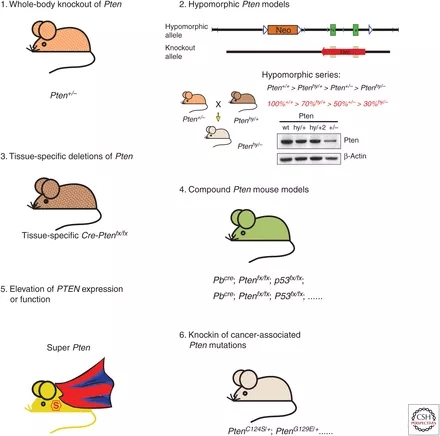
그림 3. 유전자 편집 Pten 마우스 모델. 유전적으로 변형된 Pten 마우스 모델은 아래와 같이 6가지 범주로 나눌 수 있습니다. (1) 전신 유전자 녹아웃, (2) 거대세포바이러스(CMV) 프로모터에 의해 구동되는 네오마이신(neo) 상자에 의한 표적화 Pten의 인트론3을 사용하여hypomorphic Pten model 형성. 그런 다음 이 Ptenhy/+ 마우스를 Pten+/- 마우스와 교배하여 PTEN 발현 수준이 감소된 마우스를 생성합니다(Pten+/+> Ptenhy/+> Pten+/-> Ptenhy/-), (3) 조직 특이적 녹아웃 PTEN, (4) 복합 마우스 모델: Pten 결실 및 기타 종양 억제인자 결실 또는 원 종양유전자 조합, (5)박테리아 인공 염색체(BAC) 기술을 이용하여 PTEN 유전자좌 카피를 증가한 발현 또는 기능, (6)녹인 및 CRISPR 기술에 의한 마우스의 암 시뮬레이션 관련 Pten 돌연변이.
이러한 GEMM은 많은 데이터를 생성하여 종양 형성과 관련된 세포 및 분자 메커니즘을 더 잘 이해하는 데 도움이 됩니다. 우선 Pten의 유전자 비활성화는 전신 녹아웃 기술에 의해 달성되고 조직 특이성이 결핍하며 Pten의 유전자 비활성화 시간이 제어되지 않습니다. 그러나 조직 특이적 프로모터 및 Cre 매개 재조합의 사용은 이러한 문제를 극복하고 PTEN은 조직 특이적 및 시간 제어 방식으로 유전자 변형되었습니다. 이러한 방법을 통해 연구자들은 암의 발생 및 발달에서 PTEN 조절 장애의 역할을 상세한 방식으로 연구할 수 있게 되었고 세포 배경 특이적 방식으로 연구할 수 있게 되었습니다. GEMM 종양 형성에서 PTEN의 역할의 광범위한 기능은 약물 개발을 위한 여러개의 새로운 표적을 시사해 주었고 암 예방 및 치료를 위한 잠재적인 치료 방법을 제공해 주었습니다. 이는 환자가 비정상적인 PTEN 기능으로 인한 종양과 생식계열 PTEN 돌연변이로 인한 질병에 대처할 수 있는 희망을 제공합니다.
Cyagen의 ‘AI Knock-Out Mouse Model eBank’에서는 PTEN 전신 녹아웃 마우스 및 PTEN 조건부 녹아웃 마우스를 제공할 수 있습니다. 필요한 경우 언제든지 저희에게 연락해 주십시오~
1. Chow JT, Salmena L. Recent advances in PTEN signalling axes in cancer. Fac Rev. 2020;9:31. Published 2020 Dec 23. doi:10.12703/r/9-31.
2. Yu-Ru Lee,Pier Paolo Pandolfi.2019PTEN Mouse Models of Cancer Initiation and Progression.doi: 10.1101/cshperspect.a037283.
Cyagen은 15년 동안 전 세계 연구자들에게 서비스를 제공해 왔으며 제품 및 기술은 CNS(Cell, Nature, Science) 3대 저널을 포함하여 4,800건 이상의 논문에 인용되었다. 유전자 녹아웃, 유전자 녹인, 조건부 유전자 녹아웃 맞춤형 서비스를 제공하는 외에도 Cyagen은 전문적인 수술질환 모델팀이 있어 다양하고 세밀한 소동물 수술 질환모델을 제공할 수 있습니다. 약물 선별과 평가용 마우스 플랫폼은 구미 선도 기업으로부터 도입한 면역결핍 마우스, 심혈관 및 알츠하이머병 등의 연구에 사용되는 인간화 마우스를 제공할 수 있습니다. 또한 국제 표준화 무균 마우스 기술 플랫폼은 무균마우스, 무균동물 맞춤형 서비스, 미생물균군 이식 서비스 등 무균동물 모델에 기반한 각종 제품과 서비스를 제공할 수 있으며 Cyagen의 성숙하고 안정적인 유전자 편집 마우스 플랫폼과 결합하여 균군과 유전자의 상호작용 메커니즘을 연구하는데 도움을 줄 수 있습니다.




영업일 기준 1-2일 내에 답변해 드리겠습니다.