

진행성 가족성 간내 담즙정체증 3형(PFIC3)은 간 손상을 일으키는 심각한 유전성 간 질환으로, 종종 간 이식이 필요합니다.
진행성 가족성 간내 담즙정체증 3형(PFIC3)의 병리학 및 잠재적인 치료법 연구를 진전시키기 위해, FVB-Abcb4 KO 마우스 모델은 중요한 역할을 하는 연구 모델로 자리 잡고 있습니다. FVB-Abcb4 KO 마우스 모델은 간 비대, 담즙 정체 및 섬유화와 같은 진행성 가족성 간내 담즙정체증 3형(PFIC3)의 병리학적 특징을 효과적으로 재현하여 연구자들에게 질환 발병 메커니즘 연구와 새로운 치료 접근법 평가에 적용할 수 있는 유전자 편집된 연구 모델입니다.
본문에서는 FVB-Abcb4 KO 마우스 모델의 특성, 장점 및 연구 응용 분야를 살펴보며, 이 모델이 담즙 정체 관련 연구에서 최적의 연구 모델이 되는 이유를 설명합니다. FVB-Abcb4 KO 마우스 모델이 간 질환 연구의 혁신을 지원하고 신약 개발을 가속화하는 방법을 자세히 알아보세요.
간내 담즙 정체 및 PFIC(진행성 가족성 간내 담즙정체증) 소개
간내 담즙 정체(Intrahepatic cholestasis, IHC)는 담즙산 합성 장애, 담즙 분비 이상, 담즙 흐름의 기계적 또는 기능적 장애로 인해 담즙 성분이 혈액에 유출되어 발생하는 임상 증후군입니다. 간내 담즙 정체(IHC)는 PFIC와 같은 진행성 가족성 간내 담즙정체증 및 임신성 간내 담즙정체(Intrahepatic cholestasis of pregnancy, ICP) 등 다양한 원인으로 발생할 수 있습니다.
이 중에서 진행성 가족성 간내 담즙정체증(Progressive Familial Intrahepatic Cholestasis, PFIC)은 유전성 담즙정체증의 한 형태로, 모든 신생아 담즙정체증 사례 중 약 10%~15%를 차지합니다. 진행성 가족성 간내 담즙정체증(PFIC)는 일반적으로 유아기나 어린 시절에 간내 담즙정체증으로 나타나며, 말기 간질환(ESLD)으로 진행될 수 있으며, 이는 간 이식이 필요하거나 사망에 이를 수 있습니다.[2] 진행성 가족성 간내 담즙정체증(PFIC)의 추정 발생률은 신생아 5만 명에서 10만 명 중 1명으로, 거의 모든 소아 간 이식 사례의 근본 원인으로 나타나고 있어 중요한 연구 초점이 되고 있습니다.
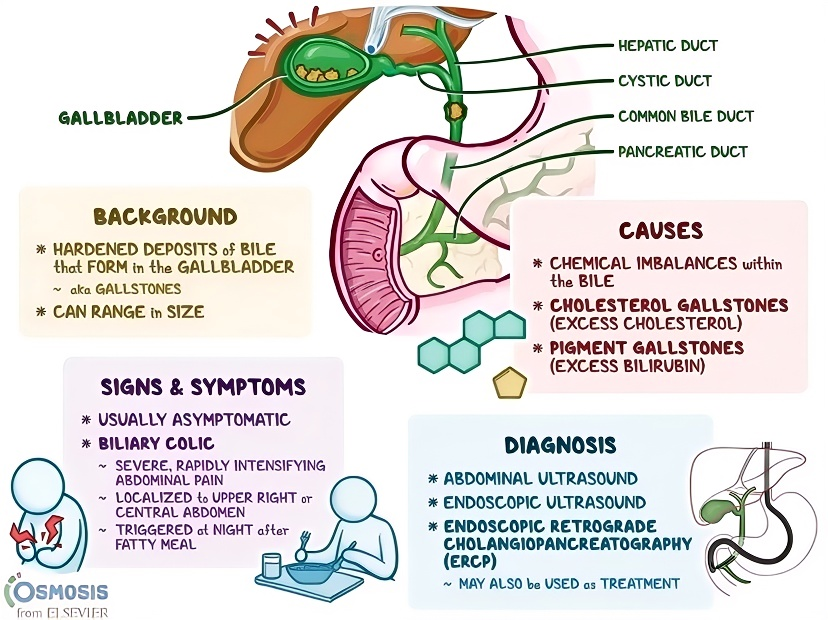
그림 1. 담즙 정체의 원인, 진단 및 증상. [3]
PFIC의 분류 및 증상
진행성 가족성 간내 담즙정체증(PFIC)은 임상 특성, 실험실 결과, 간 조직학 및 유전자 돌연변이에 따라 여섯 가지 subtype으로 분류됩니다. 가장 일반적인 형태인 진행성 가족성 간내 담즙정체증 1형, 2형, 3형(PFIC1, PFIC2, PFIC3)은 각각 ATP8B1( FIC1 단백질을 인코딩함), ABCB11( BSEP 단백질을 인코딩함) 및 ABCB4( MDR3 단백질을 인코딩하며, 설치류에서 MDR2로 알려짐)의 돌연변이에 의해 발생합니다.[4] 가장 일반적인 형태인 진행성 가족성 간내 담즙정체증 1형(PFIC1)과 2형(PFIC2)은 담즙산 수송 장애로 인해 발생하는 반면, 3형(PFIC3)은 인지질 수송 결핍으로 인해 발생하여 담즙에서 인지질 분비가 감소합니다. 진행성 가족성 간내 담즙정체증 세 가지 유형의 공동 주요 임상 증상으로는 담즙정체 황달 및 가려움증을 동반합니다. 간 섬유화 및 간경변이 진행됨에 따라 대부분의 PFIC 환자는 결국 간 이식이 필요합니다. [5]
진행성 가족성 간내 담즙정체증 3형(PFIC3)은 전체 PFIC 사례의 약 3분의 1을 차지하며, 1형(PFIC1) 및 2형(PFIC2)에 비해 보통 아동기 후반이나 청소년기에 발생합니다.[6] 비교적 늦은 발병은 종종 진단 지연을 초래하여 간 손상의 위험을 증가시킵니다. 또한, 진행성 가족성 간내 담즙정체증 3형(PFIC3)은 중등도의 가려움증, 간 종양 및 콜레스테롤 담석과 관련이 있으며, 이는 더 많은 합병증을 초래하여 말기 간질환(ESLD)으로 진행될 수 있습니다. [4-6]
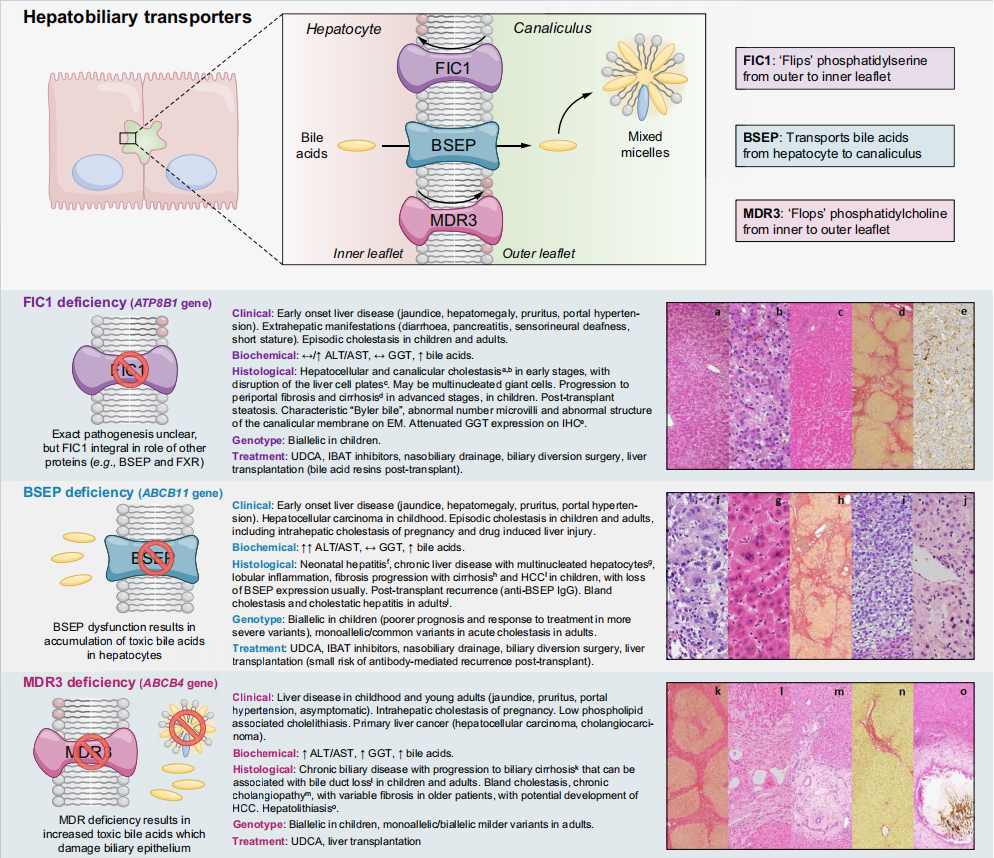
그림 2. 진행성 가족성 간내 담즙정체증(PFIC) 세 가지 주요 유형의 원인 및 전형적인 증상 [7]
진행성 가족성 간내 담즙정체증 3형(PFIC3) 마우스 모델
진행성 가족성 간내 담즙정체증 3형(PFIC3)은 ABCB4 유전자의 기능 상실 돌연변이로 인해 발생하여 MDR3 단백질의 기능 장애로 이어집니다. 이에 따라 포스파티딜콜린(PC) 수송 장애, 담즙 내 포스파티딜콜린(PC) 수치 감소, 담즙산염 농도 증가, 담즙 정체 및 간세포 손상이 발생합니다.
연구에 따르면, Abcb4 유전자가 인코딩하는 마우스 MDR2 단백질이 인간 MDR3 단백질과 상동체입니다. Abcb4 유전자 Knockout(KO) 마우스는 인간 진행성 가족성 간내 담즙정체증 3형(PFIC3)과 유사한 표현형을 나타낼 수 있는 것으로 확인됩니다. 그러나 마우스 모델에서 나타난 질환의 심각성과 진행 정도는 마우스 품종 계통의 배경에 따라 다릅니다.
일반적으로 사용되는 C57BL/6 배경에서 Abcb4-KO 마우스는 담즙산염의 독성이 낮기 때문에 상대적으로 경미한 병리학적 표현형을 나타내며, 인간 진행성 가족성 간내 담즙정체증 3형(PFIC3)과 더 유사한 표현형을 유도하기 위해 소수성 담즙산염을 추가해야 합니다.[8-10] 반면, FVB 배경의 Abcb4-KO 마우스는 특별한 식이 없이 간 비대와 간 섬유증과 같은 인간 PFIC3의 대부분 주요 바이오마커와 병리학 특징을 자발적으로 재현할 수 있습니다. Abcb4-KO 마우스 모델은 C57BL/6 배경의 동일한 유전자 편집에 비해 더 일찍 발병하고 더 심각한 질환 표현형을 나타냅니다.[10-11]
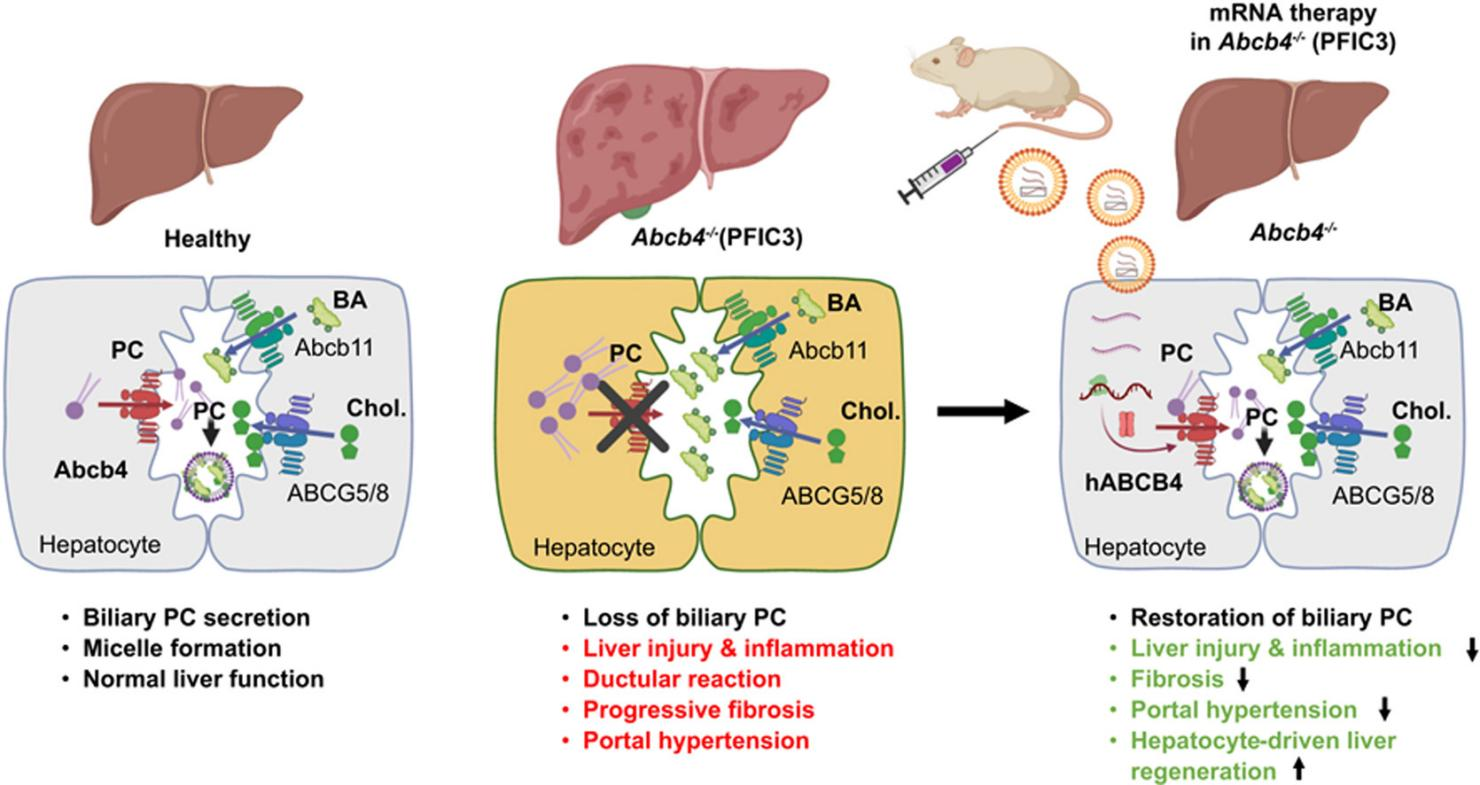
그림 3. 진행성 가족성 간내 담즙정체증 3형(PFIC3) 발병 기전 연구 및 신약 개발에 Abcb4-KO 마우스 모델의 적용 [12]
Cyagen FVB-Abcb4 Knockout 마우스 모델
Cyagen은 Knockout 기술을 통해 FVB 계통에서 Abcb4 유전자를 제거하여 FVB-Abcb4 Knockout (KO) 마우스 모델을 개발하였습니다. 이 마우스 모델은 전임상 PFIC3 연구에 사용될 수 있습니다. FVB-Abcb4 KO 마우스(제품 번호: C001590)는 Abcb4 유전자와 그에 의해 인코딩한 MDR2 단백질(murine homolog to MDR3)을 완전히 발현하지 않으며, 이 모델은 간비대, 간 기능 손상 마커 상승, 총 빌리루빈 수치 증가 등 PFIC3의 주요 특성을 재현하고, 간세포 괴사, 염증 세포 침투, 결합조직 증식, 담관 증식, 간 섬유화와 같은 심각한 간 조직 병리학적 특징을 나타냅니다.
유전자 및 단백질 발현 분석 결과, FVB-Abcb4 KO 마우스의 심장, 비장, 간에서 Abcb4 유전자 발현이 검출되지 않았으며, 간에서 ABCB4 (MDR2) 단백질 발현도 검출되지 않아, 유전자 Knockout이 성공적으로 이루어졌음을 확인했습니다.
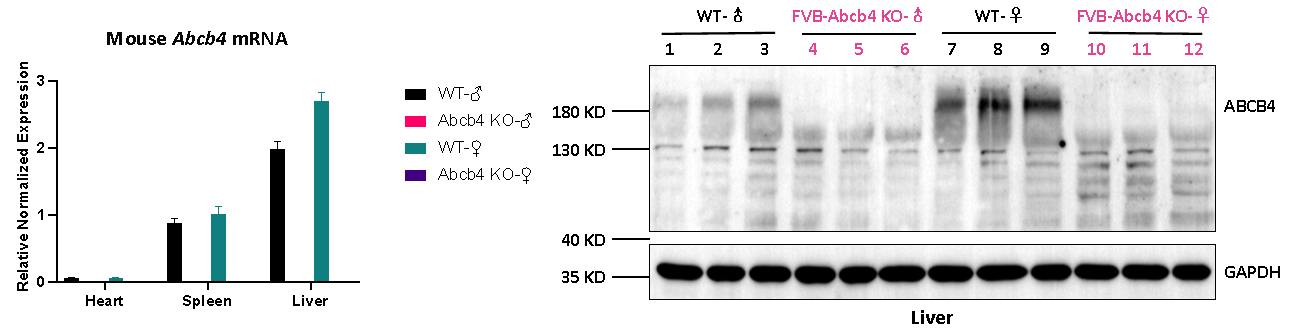
그림 4. FVB Wild-Type(WT) 마우스와 FVB-Abcb4 KO 마우스의 조직에서 Abcb4 유전자 및 ABCB4(MDR2) 단백질 발현의 검출 결과.
Wild-Type(WT) 마우스에 비해 FVB-Abcb4 KO 마우스의 간은 현저하게 비대해져 있습니다.
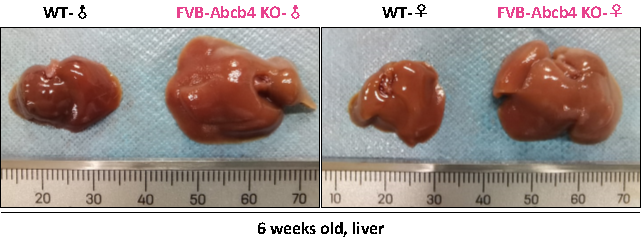
그림 5. 생후 6주령의 Wild-Type(WT) 마우스와 FVB-Abcb4 KO 마우스의 간 형태 비교.
Wild-Type(WT) 마우스에 비해, FVB-Abcb4 KO 마우스에서 다음과 같은 특징을 보입니다.
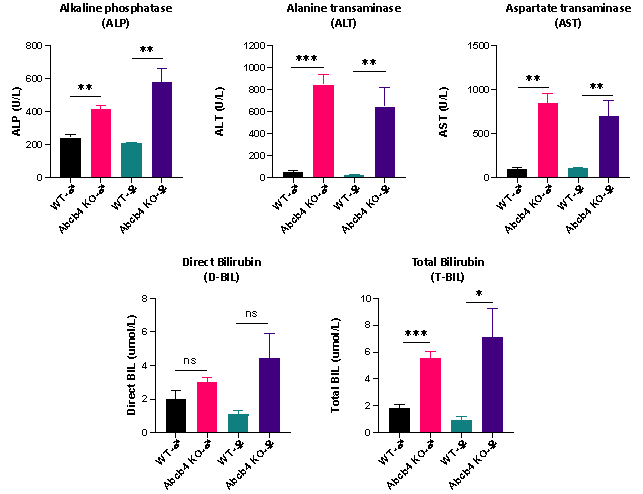
그림 6. 생후 6주령의 Wild-Type(WT) 마우스와 FVB-Abcb4 KO 마우스의 간 기능 마커 비교.
H&E 염색 및 Masson 염색 결과에 따르면 Wild-Type(WT) 마우스에 비해 FVB-Abcb4 KO 마우스의 간은 세포 괴사, 결합 조직 증식, 염증 세포 침윤, 담관 증식 증가, 콜라겐 섬유 증식 및 섬유화, 섬유 격막 형성, 인접 문맥역(Portal area) 사이의 섬유 가교 결합 등 인간 진행성 가족성 간내 담즙정체증 3형(PFIC3)의 다양한 증상을 나타냅니다.
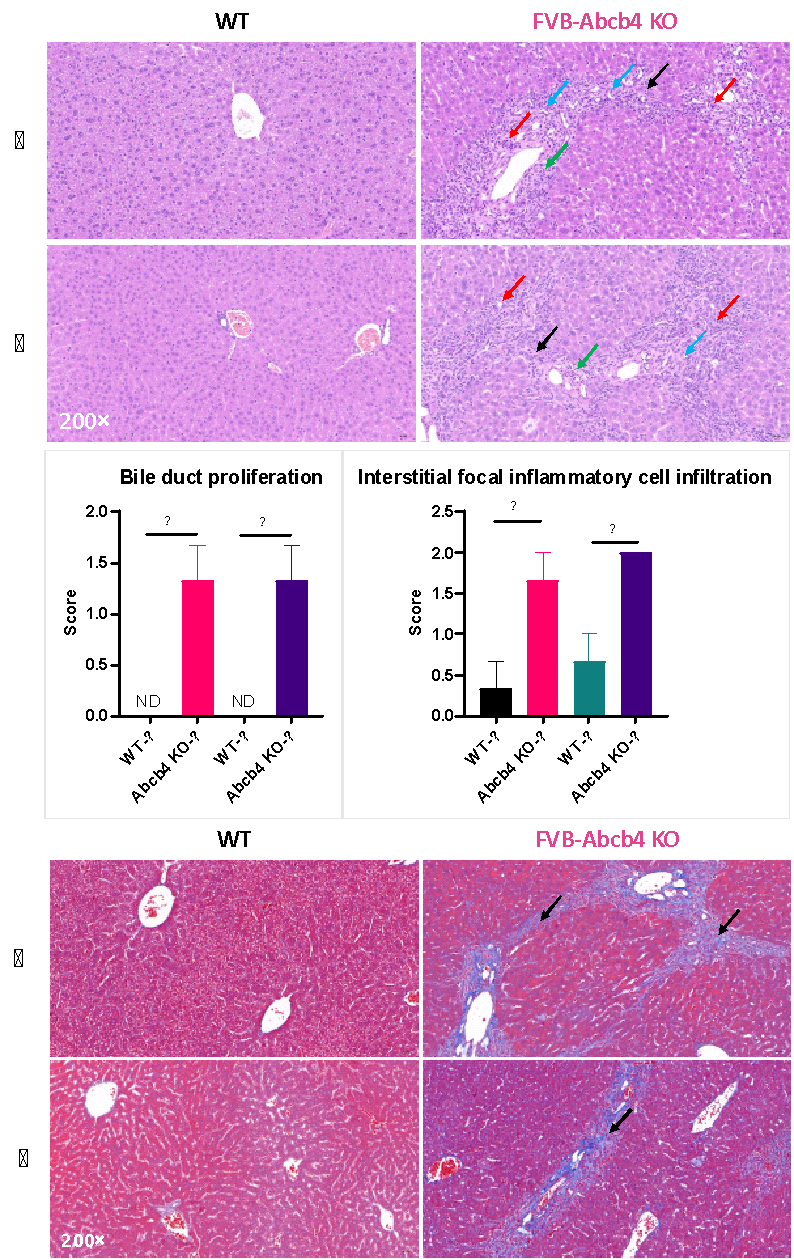
그림 7. Wild-type(WT) 마우스와 FVB-Abcb4 KO 마우스 간의 간 조직 H&E 염색, Pathological scoring 및 Masson 염색 결과의 비교.
요약
FVB-Abcb4 KO 마우스(제품 번호: C001590)는 진행성 가족성 간내 담즙정체증 3형(PFIC3) 연구에 이상적인 연구 모델입니다. Abcb4 유전자에 대한 Knockout을 통해 MDR2 단백질의 결실을 초래하여, 심각한 간 비대 및 간 기능 이상을 일으켰으며, 이는 ALT, AST, ALP 및 T-BIL(Total Bilirubin) 수치의 상승으로 입증되었습니다. 또한 이 마우스는 간세포 괴사, 간섬유화, 담관 증식 등 진행성 가족성 간내 담즙정체증 3형(PFIC3) 환자에서 나타나는 병리학적 특징을 재현합니다. 이에 따라 FVB-Abcb4 KO 마우스는 진행성 가족성 간내 담즙정체증 3형(PFIC3) 발병 기전 연구와 담즙 정체 관련 간 질환의 신약 개발에 적용됩니다.
Cyagen은 전 세계 주요 제약사, 생명공학 기업 및 학술 연구 기관과 광범위하게 협력하여 포괄적인 대사성 질환 모델을 개발하고 있습니다. Cyagen의 유전자 모델링 전문가들은 간 질환, 비만, 당뇨병, 고요산혈증, 죽상동맥경화증과 같은 대사 질환과 관련된 질환 모델을 개발하여 해당 분야의 질환 연구 및 신약 개발 연구를 가속화하고 있습니다.
|
제품 번호 |
모델명 |
품종 계통 |
응용분야 |
|
C001507 |
C57BL/6JCya |
Atherosclerosis, Hypercholesterolemia, Metabolic Dysfunction-Associated Steatohepatitis (MASH) |
|
|
C001067 |
APOE |
C57BL/6NCya |
Atherosclerosis |
|
C001291 |
B6-db/db |
C57BL/6JCya |
High Blood Sugar and Obesity |
|
C001392 |
C57BL/6JCya |
Familial Hypercholesterolemia |
|
|
C001368 |
C57BL/6JCya |
Type 2 Diabetes and Obesity |
|
|
C001232 |
C57BL/6JCya |
Hyperuricemia |
|
|
C001267 |
C57BL/6NCya |
Copper Metabolism Disorder, Wilson's Disease |
|
|
C001265 |
C57BL/6NCya |
Primary Ciliary Dyskinesia |
|
|
C001266 |
C57BL/6NCya |
Klinefelter Syndrome |
|
|
C001273 |
C57BL/6NCya |
Phenylketonuria Type 1 |
|
|
C001383 |
Alb-Cre/LSL-hLPA |
C57BL/6NCya |
Cardiovascular Targets |
|
C001421 |
C57BL/6NCya |
Metabolic Targets |
|
|
C001400 |
C57BL/6JCya |
Metabolic Targets |
|
|
C001493 |
FVB |
Diseases Related to Blood-Brain Barrier Permeability |
|
|
C001532 |
C57BL/6JCya |
Hereditary Angioedema(HAE) |
|
|
C001549 |
C57BL/6NCya |
Research on diet-induced obesity, diabetes, inflammation, fatty liver, and other metabolic diseases; drug development, screening, and preclinical efficacy evaluation for obesity. |
|
|
C001553 |
C57BL/6NCya |
Familial hypercholesterolemia (FH); atherosclerotic cardiovascular disease (ASCVD); other cardiovascular diseases (CVD). |
|
|
C001560 |
C57BL/6JCya |
Phenylketonuria (PKU) |
|
|
I001220 |
C57BL/6Cya |
Research on PCSK9-targeted drug development; studies on metabolic diseases such as hyperlipidemia, stroke, coronary heart disease, and familial hypercholesterolemia (FH). |
|
|
I001223 |
C57BL/6NCya |
Fabry Disease (FD) |
|
|
C001583 |
FVB/NJCya |
Propionic Acidemia (PA) |
|
|
C001590 |
FVB/NJCya |
Progressive Familial Intrahepatic Cholestasis Type 3 (PFIC3) |
|
|
C001594 |
C57BL/6JCya |
Glutaric aciduria type I (GA1) |
|
|
C001600 |
C57BL/6NCya; C57BL/6JCya |
Type 2 Diabetes, Obesity, and Metabolic Disorders Associated with Improper Fat Distribution and Storage |
|
|
C001601 |
C57BL/6NCya; C57BL/6JCya |
Type 2 Diabetes and Obesity |
|
|
C001591 |
C57BL/6NCya; C57BL/6JCya |
Familial hypercholesterolemia (FH); atherosclerotic cardiovascular disease (ASCVD); other cardiovascular diseases (CVD) |
|
Diet-Induced Metabolic Dysfunction-Associated Steatotic Liver Disease (MASLD) Model |
|||
참고 문헌:
[1]KuntzM, KuntzHD.Hepatology textbook and atlas.Springer Berlin Heidelberg,2008.Available from: https://link.springer.com/book/10.1007/978-3-540-76839-5
[2]A Siddiqi I, Tadi P. Progressive Familial Intrahepatic Cholestasis. [Updated 2023 Jul 3]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK559317/
[3]Cholelithiasis: What Is It, Causes, Treatment, and More." Osmosis, 6 Sept. 2022, https://www.osmosis.org/answers/cholelithiasis
[4]Srivastava A. Progressive familial intrahepatic cholestasis. J Clin Exp Hepatol. 2014 Mar;4(1):25-36.
[5]Sutton H, Karpen SJ, Kamath BM. Pediatric Cholestatic Diseases: Common and Unique Pathogenic Mechanisms. Annu Rev Pathol. 2024 Jan 24;19:319-344.
[6]Orphanet. Mucopolysaccharidosis Type II. Orphanet, n.d. Web. 9 Jan. 2025. https://www.orpha.net/en/disease/detail/79305#:~:text=Prevalence:%201-9%20/%20100,Age%20of%20onset:%20All%20ages
[7]Nayagam JS, Miquel R, Thompson RJ, Joshi D. Genetic cholestasis in children and adults. J Hepatol. 2024 Apr;80(4):670-672.
[8]Smit JJ, Schinkel AH, Oude Elferink RP, Groen AK, Wagenaar E, van Deemter L, Mol CA, Ottenhoff R, van der Lugt NM, van Roon MA, et al. Homozygous disruption of the murine mdr2 P-glycoprotein gene leads to a complete absence of phospholipid from bile and to liver disease. Cell. 1993 Nov 5;75(3):451-62.
[9]Ikenaga N, Liu SB, Sverdlov DY, Yoshida S, Nasser I, Ke Q, Kang PM, Popov Y. A new Mdr2(-/-) mouse model of sclerosing cholangitis with rapid fibrosis progression, early-onset portal hypertension, and liver cancer. Am J Pathol. 2015 Feb;185(2):325-34.
[10]Weber ND, Odriozola L, Martínez-García J, Ferrer V, Douar A, Bénichou B, González-Aseguinolaza G, Smerdou C. Gene therapy for progressive familial intrahepatic cholestasis type 3 in a clinically relevant mouse model. Nat Commun. 2019 Dec 13;10(1):5694.
[11]Aronson SJ, Bakker RS, Shi X, Duijst S, Ten Bloemendaal L, de Waart DR, Verheij J, Ronzitti G, Oude Elferink RP, Beuers U, Paulusma CC, Bosma PJ. Liver-directed gene therapy results in long-term correction of progressive familial intrahepatic cholestasis type 3 in mice.
[12]Wei G, Cao J, Huang P, An P, Badlani D, Vaid KA, Zhao S, Wang DQ, Zhuo J, Yin L, Frassetto A, Markel A, Presnyak V, Gandham S, Hua S, Lukacs C, Finn PF, Giangrande PH, Martini PGV, Popov YV. Synthetic human ABCB4 mRNA therapy rescues severe liver disease phenotype in a BALB/c.Abcb4-/- mouse model of PFIC3. J Hepatol. 2021 Jun;74(6):1416-1428.




영업일 기준 1-2일 내에 답변해 드리겠습니다.