

유세포 분석(Flow Cytometry)은 유체에 현탁된 미세입자를 계수하고 분류할 수 있는 기술로 고효율, 단순성, 정확성으로 인해 CAR-T 세포 치료의 모든 단계에서 널리 사용되었습니다. 다음은 CAR-T 임상 연구 개발 전에 유세포 분석(Flow Cytometry)의 응용에 대해 알아보겠습니다.
CAR-T 세포는 scFv를 통해 종양 세포에서 항원을 정확하게 식별하고 사멸 효과를 발휘하므로 이상적인 표적 항원을 스크리닝하는 것은 중요한 단계입니다. 고특이성 표적항원을 스크리닝하기 위해서는 모든 세포에서 표적항원의 발현량을 검출하고 종양세포에서 고도로 발현되고 정상세포에서는 발현되지 않거나 낮은 발현을 갖는 항원을 스크리닝하여 CAR-T 세포 요법의 독성 부작용을 최대한 피해야 한다. 유세포 분석은 이 과정에서 중요한 응용 프로그램이 있습니다. 예를 들어, 다음 보고서에서 저자는 유세포 분석을 통해 표적 항원 BCMA의 분포를 테스트한 결과 BCMA가 정상 및 종양 PC 세포 모두에서 높게 발현되었음을 발견했습니다.정상 조직에서는 발현되지 않거나 낮습니다.

그림 1 유세포 분석 표적 항원의 발현 풍부도[1]
CAR-T의 임상 개발 전에 CAR-T 세포의 항종양 능력의 후속 평가를 위해 CAR-T 세포 및 항원 과발현 종양 세포 모델을 구축해야 합니다. 이 과정에서 렌티바이러스의 역가는 엄격하게 품질 관리됩니다.유세포 분석은 렌티바이러스 활성 역가를 감지하는 중요한 수단 중 하나입니다. 렌티바이러스 역가 검출을 위한 유세포 분석의 적용은 다음과 같은 실례로 설명됩니다.
CD19 항원 렌티바이러스의 역가를 검사하고, CD19 항원을 코딩할 수 있는 렌티바이러스의 정제액을 0.01, 0.1, 1,10μl의 4개의 구배로 사전 접종된 293T 세포에 첨가하고, 72시간 후 293T 세포 CD19 항원의 양성률(즉, 렌티바이러스에 감염된 293T 세포가 전체 세포 수의 백분율)을 유량으로 검출한 후, 다음 공식에 따라 렌티바이러스의 형질도입 역가를 계산해야 합니다.
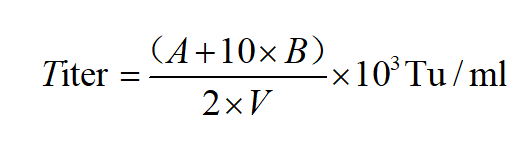
A: 0.1μl 군의 양성 세포 비율을 나타낸다
B: 0.01μl 군의 양성 세포 비율을 나타낸다
N: 바이러스 투입 시 세포 수
V: 그룹 a 에서 바이러스의 볼륨을 나타냅니다
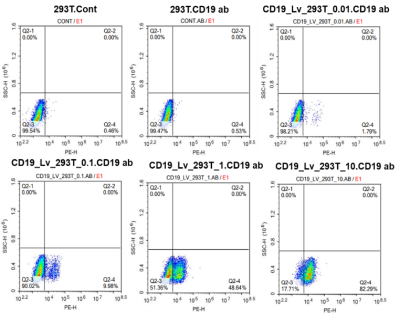
그림 2 CD19 항원 렌티바이러스 역가 검출 결과
(데이터 출처: Cyagen)
그림에서 보는 바와 같이 CD19 항원 양성 세포의 수는 형질감염 바이러스 구배가 증가함에 따라 점차 증가하여 렌티바이러스가 우수한 감염 활성을 가짐을 나타내며, 바이러스 역가는 위의 공식에 따라 1.4×108 Tu/ml로 계산되었다.
유사하게, 위의 방법을 사용하여 CD19 CAR 렌티바이러스 역가를 검출하였으며, 계산 후 바이러스 역가는 약 4.33×108Tu/ml이었다.
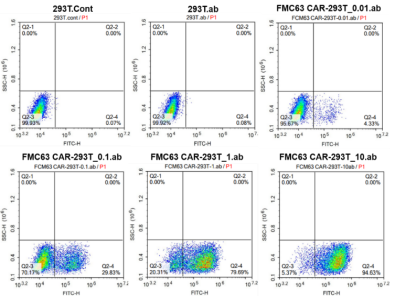
그림 3. FMC63 CAR 렌티바이러스 역가 검출 결과
(데이터 출처: Cyagen)
구축된 CAR-T 세포의 경우 기능 검증 전에 표현형 및 CAR 분자의 양성률을 테스트해야 합니다. 유사하게, 구축된 과발현 항원 세포 모델의 경우 유세포 분석에 의해 항원 발현을 검출할 수도 있습니다. 실례를 통해 소개하겠습니다.
두 가지 방법으로 제조한 T세포를 항체로 표지한 후 표현형을 분석한 결과, 두 방법 모두 고순도 T세포를 얻을 수 있지만, 두 방법 모두 증폭된 서로 다른 아형 T세포의 비율이 상당히 다르며, Method1에서 증폭된 T세포는 주로 CD8+T세포 아형이고, Method2는 CD8+T세포와 CD4+T세포의 비율 차이가 적은 T세포 집단을 증폭할 수 있으며, 이 두 방법은 서로 다른 아형 T세포의 역할을 연구하기 위한 견고한 토대를 마련했습니다. 동시에 우리는 CD19 CAR 렌티바이러스로 Method1 증폭된 T 세포를 형질감염시키고, CD19 CAR-T 세포를 구성하고, 유속법을 사용하여 CAR 단백질의 발현 효율을 검출한 결과, CD19 CAR-T의 양성률이 45.59%에 달할 수 있음을 보여 CD19 CAR-T 세포를 성공적으로 구성했음을 나타냅니다.
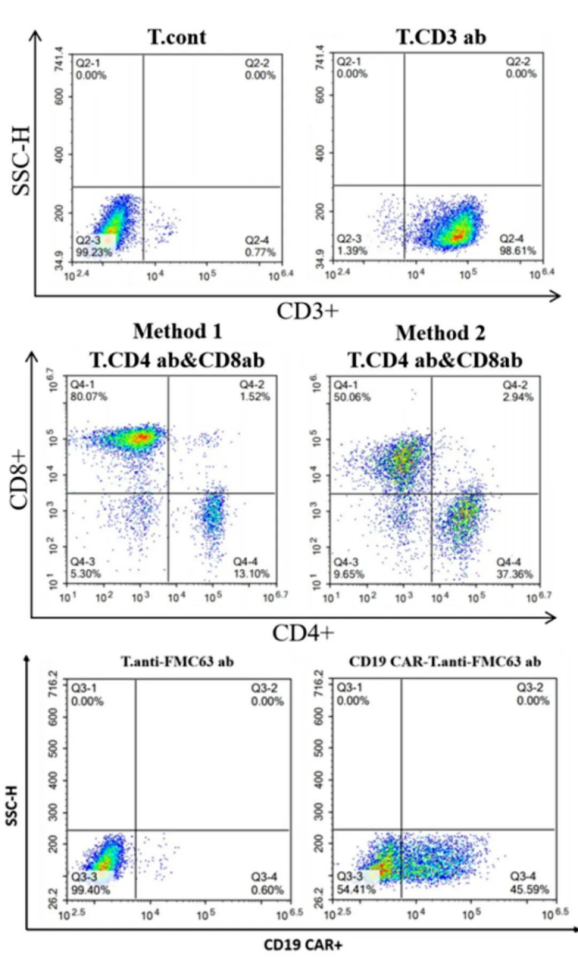
그림 4. T 세포 표현형 분석 및 FMC63 CAR-T 세포 양성률 검출. A.PBMC 활성화 및 증폭 10일째 T세포 비율 및 표현형 분석 실험 결과이다. B.FMC63 CAR-T 세포 CAR 양성률 테스트 결과입니다.(데이터 출처: Cyagen)
CD19 렌티바이러스에 의해 293T 세포를 감염시키고, CD19가 안정적으로 발현되는 293T 세포주를 구축하고, 항원 CD19의 높은 발현을 유속으로 검출하였다.
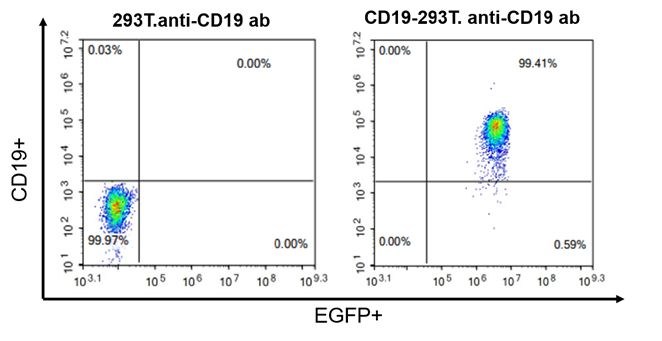
그림 5. 스트리밍 검출 CD19-293T 안정전세포주 CD19 항원 표현 (자료 출처: Cyagen)
CAR-T 세포를 종양 세포 또는 구축된 항원 과발현 세포 모델과 혼합하여 CAR-T 세포의 사멸 효과를 반영할 수 있는 종양 세포 또는 항원 과발현 세포 모델의 사멸을 감지합니다.그 중 유세포 분석은 종양 세포의 세포 사멸을 감지할 수 있습니다.이 예는 다음과 같습니다.
CD19 CAR-T 세포와 T 세포를 각각 다른 효과 과녁으로 Nalm6 세포와 함께 48h 를 부화시킨 후 종양세포가 시들어가는 것을 유류법으로 검출한다. 그림에서 보는 바와 같이 CD19 CAR-T 세포는 T 세포 그룹과 비교하여 다양한 표적 비율 조건에서 Nalm6 세포에 대한 특정 세포독성 효과를 크게 향상시켰습니다. 동시에, 세포 배양 상청액의 사이토카인 함량 검출 결과, 종양 세포와 함께 배양한 후 CD19 CAR-T 사이토카인 IFN-γ의 분비가 T 세포에 비해 유의하게 향상되었음을 보여주었다.
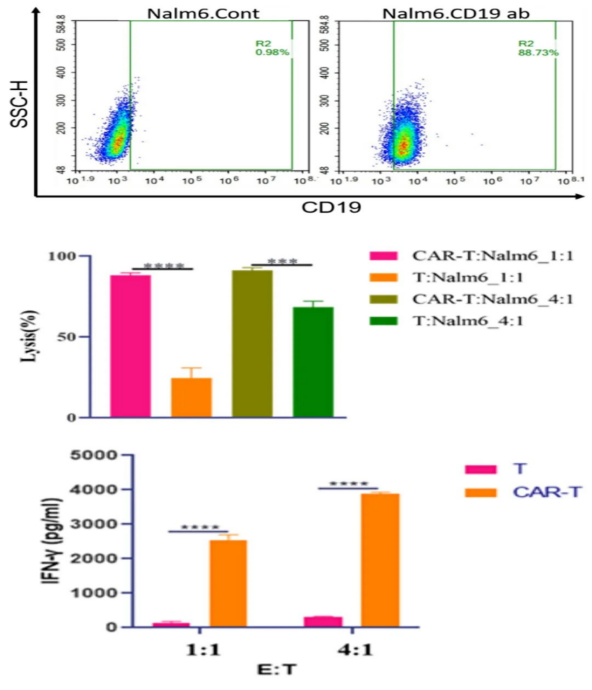
그림 6 CD19 CAR-T 세포가 Nalm6 종양세포를 죽인 실험 결과. A.Nalm6 세포 표면 CD19 항원 양성률 검사 결과; B-C.FMC63 CAR-T 세포 사멸 Nalm6 종양 세포 및 상청 사이토카인 검출 실험 결과입니다. (데이터 출처: Cyagen)
체외에서 CAR-T 세포의 표현형과 사멸 효과를 확인한 후 체내 실험을 수행할 수 있습니다. CAR-T 세포를 종양 마우스 모델(예: NSG, C-NKG, NOG 등)에 주입한 다음 다양한 일수의 말초 혈액 샘플(Peripheral blood, PB)을 채취하여 유세포 분석을 사용하여 체내에서 CAR-T 세포의 증식 활성, 세포 표현형 및 사멸 능력을 모니터링할 수 있습니다.
CAR-T 요법은 종양 치료 분야에서 가장 유망한 방향 중 하나이며 암을 '치유'하는 치료법입니다. 전임상 연구는 많은 중요한 단계를 거쳐야 하며 각 단계에는 엄격한 품질 관리 기준이 필요합니다. 최근 몇 년 동안 유세포 분석의 지속적인 발전과 자체 장점을 기반으로 CAR-T 세포 치료 제품 개발의 모든 단계에서 더 널리 사용될 것입니다.
CAR-T 및 기타 세포 치료에 대한 전임상 연구에서는 세포 모델과 동물 모델의 선택이 매우 중요하며 연구 목적을 명확히 하고 효과적인 실험 모델과 계획을 수립하면 연구가 두 배로 증가할 것입니다. Cyagen는 항체 스크리닝에서 안정적인 발현 세포주 구축, 세포/동물 모델 구축에서 약력 평가에 이르기까지 세포 치료 원스톱 서비스를 제공하고 CAR-T 및 기타 세포 치료의 연구 개발 프로세스를 더 잘 가속화합니다. 필요하시면 문의주세요~
Bu DX, Singh R, Choi EE, et al. Pre-clinical validation of B cell maturation antigen (BCMA) as a target for T cell immunotherapy of multiple myeloma. Oncotarget. 2018;9(40):25764-25780.




영업일 기준 1-2일 내에 답변해 드리겠습니다.