

연구 방향을 조율하고 학술 연구의 돌파구를? 논문 주제 선정에 대한 생각을 얻고, 발문 적중률을 높이고 싶어? 너는 학과의 발전 태세와 미래 방향을 이해해야 한다! Cyagen 칼럼 'Gene of the Week'는 매주 하나의 유전자를 핫이슈 연구분야에 따라 소개하고, 유전자 기본정보, 연구개황, 응용배경 등을 자세히 소개하여 학술연구의 예민함을 유지하고 과학연구의 효율성을 높일 수 있도록 도와드릴 예정이니 지속적인 관심을 기대합니다. 오늘날 우리가 이야기할 주인공은 비알코올성 지방간 발병 과정에서 중요한 역할을 하는 Sirt3 유전자입니다.
Sirt3 유전자 소개
SIRT3 유전자, Sirtuins 가족에 속합니다. Sirtuins는 진화적으로 보수적인 NAD+의존성 탈아세틸효소 가문으로 세포증식, DNA회복, 미토콘드리아 에너지 안정상태, 항산화 활성 등 다양한 생리 기능을 제어합니다. 포유류 Sirtuins 가족은 모두 7 명 (SIRT1-7 포함) 입니다.최근 연구에 따르면 SIRT3 는 심혈관과 대사질환에서 중요한 역할을 하는 것으로 나타났습니다.분자 메커니즘 측면에서 SIRT3는 탈아세틸 효소의 일종으로 주로 미토콘드리아에 위치합니다. 따라서 대부분의 미토콘드리아 단백질을 조절할 수 있는 라이신 아세틸화는 세포가 에너지 대사를 조절하는 중요한 센서로 미토콘드리아 ATP 생성과 스트레스에 대한 적응성 반응을 조절합니다.SIRT3 유전자는 인간 11번 염색체에 위치하며, 유전자의 전체 길이는 약 21.9kb, 총 10개의 외현자가 있으며 아미노산 수는 187개로 핵 인코딩 후 포함 N엔드 미토콘드리아 표적 서열 효소 없는 활단백질,이 서열이 미토콘드리아를 들여온 뒤 끊겨 효소가 활성화된 28kda의 단백질이 남아 있습니다.
|
종 |
인류 |
Mouse(생쥐) |
Rat(큰쥐) |
|
염색체 |
11번 염색체 |
7번 염색체 |
1번 염색체 |
|
유전자 전장(bp) |
21902 |
18647 |
21983 |
|
Mrna(nt) |
567 |
774 |
612 |
|
외현자 수량 |
10 |
8 |
8 |
|
아미노산의 수량 |
187 |
257 |
203 |
|
동원유전자 |
SIRT2,SIRT1,SIRT6,SIRT4,SIRT7,SIRT5 |
||
|
관련 질병 |
비알코올성 지방성 간(NAFLD) |
||
|
Cyagen마우스 모형 |
|||
|
상태 |
맞춤 제작 |
정자은행 |
Live(생체) |
|
KO |
√ |
√ |
√ |
|
CKO |
√ |
√ |
|
표 1. SIRT3의 기본 정보
비고:√ 로고가 있는 것은 Cyagen 붉은쥐 자원 저장소에 저장된 상태의 쥐입니다.
비알코올성지방성간질환(NAFLD)
비알코올성 지방성 간질환(nonalcoholic fatty liver disease, NAFLD)은 외원 알코올과 기타 명확한 간 손상 요인에 의한 간세포 내 지방 과다침적이 주요 특징인 임상병리증후군입니다.인슐린 저항과 유전적 감수성과 밀접한 관련이 있는 획득성 대사 자극성 간 손상입니다.NAFLD는 일련의 간 질환을 포함하여 간지방변성(NAFL), 단순성지방간(SFL), 비알코올성지방성간염(NASH) 및 그 관련 간경화를 총칭하는 말로 비만과 대사증후군의 일종입니다.
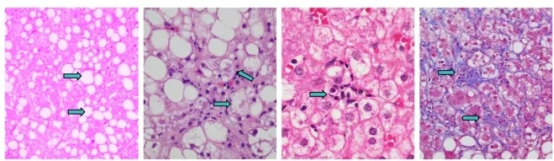
그림 1. NAFLD 환자의 간 생체검사에서 나온 영상은 간 지방변성 (기포 구조), 간 세포 풍선 변성, 소엽염증, 세포 주변 섬유화 등의 전형적인 표현을 보여준다.[1]
NAFLD의 질병 메커니즘
비알코올성 지방성 간 발병 메커니즘을 설명하는 '투 히트(two-hit)' 이론이 수년간 제기됐습니다.이 이론은 간지방변성(NAFL)의 경우에만 비알코올성 지방성 간염(NASH)의 진일보한 발전은 다른 유인(예컨대 산화반응)으로부터의 2차적인 '타격'이 필요하다는 것을 보여준다.하지만 이런 시각이 조금씩 바뀌고 있다.비알코올성 지방성 간염을 촉진하는 분자경로는 여러 가지가 있으며 모든 환자의 질병 구동요인이 같은 것은 아닙니다.이 때문에 질병을 일으키는 메커니즘과 임상적 표현은 모두 고도로 이질적입니다.
NAFL과 NASH의 발생 메커니즘을 정의할 때 새로운 연구이론은 간에서 처리하는 주요 대사 에너지저하물(탄수화물과 지방산)의 능력이 과부하되어 간에 유독성 지질 물질이 과다하게 축적되는 것으로 보고 있습니다.이들 대사산물은 간세포의 자극, 손상, 사망을 유도해 간 섬유화와 게놈 손상을 초래하고 간경화와 간세포암에 걸리기 쉽다.따라서 간세포에서 지방산의 원천과 행방을 밝히는 것은 NASH 의 대사 기초를 이해하는 데 필수적입니다. 지방산이 과다하게 공급되거나 손상된 경우 지독성 물질을 발생시키는 저물로 내질망 자극과 간세포 손상을 일으킬 수 있습니다.지독성, 내질망 자극 및 세포 손상을 일으키는 경로를 밝히면 합리적인 치료 표적지가 될 수 있습니다.[1]
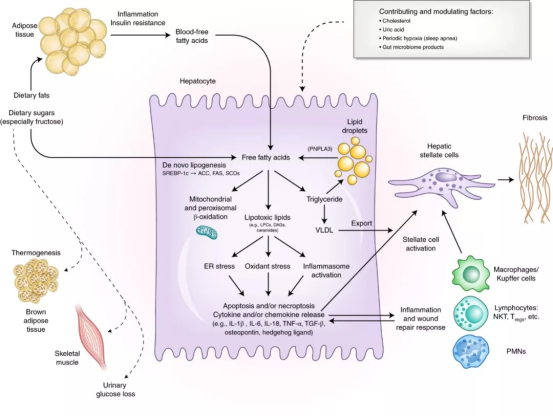
그림 2. 유리지방산은 NASH 발병 메커니즘의 핵심입니다.지방조직에서 글리세린의 지해작용에서 유래한 유리지방산은 혈액을 통해 간으로 수송됩니다.지방산은 간세포에서 두 가지 주요 경로로 미토콘드리아 베타산화 및 리에스테르화를 통해 글리세린을 형성한다.Triglyceride는 저밀도 지단백으로 혈액 속으로 들어가거나 지적에 저장할 수 있습니다.지방 방울 트라이글리세라이드는(Fat drop triglyceride) 조절된 지해작용을 통해 지방산을 간세포 유리 지방산 풀으로(Free fatty acid pool) 되돌려보냅니다.지방산은 베타-산화 또는 글리세린의 형성을 통해 지방산의 처리에 부담을 줄 때 지방산은 지독성 물질의 형성을 초래하여 내질망 자극, 산화 자극, 염증 소체가 활성화됩니다.이러한 과정은 NASH 표형의 원인으로 간세포 손상, 염증, 별 세포 활성화, 과다한 세포외 기질의 축적[1]을 들 수 있습니다.
SIRT3 유전자 및 NAFLD
대사 이상을 동반한 미토콘드리아 기능장애가 Ⅱ형 당뇨병, 비만, NAFLD 등 대사질환의 공통적인 특징이라는 연구결과가 늘고 있습니다.따라서 미토콘드리아 기능 장애가 NAFLD 에 미치는 발병기리와 잠재적 분자 표적을 탐구하는 것이 현재 연구원들이 탐구하고 있는 새로운 치료 방향이 되고 있습니다.
SIRT3는 고산화 능력을 가진 뇌, 심장, 신장, 갈색 지방조직과 간에서 높이 표현되며 주로 미토콘드리아 기질에 위치합니다. 가역적인 단백질인 아세틸화를 통해 미토콘드리아 대사에 중요한 역할을 함으로써 기체대사, 산화반응, 세포생존 등의 생물학적 과정에 광범위하게 관여하게 됩니다. Sirt3 생쥐의 녹아웃은 이미 SIRT3의 대사 중 생리작용을 밝히는 데 널리 사용되고 있습니다.장기간 고지방 식사를 하는 생쥐의 Sirt3 활성이 낮고 미토콘드리아 기능이 손상되어 간에서 단백질이 과도하게 아세틸화됩니다[2]. Sirt3 결함 쥐의 연구에 따르면 기초정상 조건 하에서 높은 아세틸화 형태의 과녁 미토콘드리아 단백질은 대사 안정을 달성하기에 충분한 활성을 가지고 있는 것으로 나타났습니다.그러나 산화적 자극조건 하에서 예를 들면 고지방 식사의 경우 기체대사에 필요한 SIRT3 효소일은 비만과 지방성 간염으로 인한 대사교란 수요를 충분히 충족시키지 못합니다.이 쥐들은 비만 가속화, 인슐린 저항, 지방성 간염 등을 나타낸다.근육 특이성 Sirt3 두들겨 쥐를 제거한 또 다른 연구에서는 산소 소비량이 증가하고 지질 이용이 증가하는 것이 관찰됐습니다[3].또한 고지방 유도 전신성 SIRT3 두들겨서 쥐를 제거하는 것은 장 미생물균군의 불균형을 심화시켜 장의 투과성을 손상시키고 NAFLD의 발달을 촉진한다[4]. 따라서 다양한 조직에서 Sirt3가 어떤 역할을 하는지에 대한 추가 연구가 필요합니다.
전반적으로 이러한 연구들은 SIRT3가 기체의 대사 상태를 감지하는 에너지 스위치로서 미토콘드리아 단백질의 아세틸화 수준을 조절함으로써 이상 대사 상황에서의 미토콘드리아 반응과 기능 장애를 방지함으로써 기체의 대사 안정 상태를 조절한다는 것을 보여준다.이 같은 결과는 SIRT3가 임상치료NAFLD의 잠재적 치료표적일 수 있음을 시사하는 것입니다.
Sirt3녹아웃 마우스 모형
C57BL/6 마우스에서 Sirt3 유전자를 두드려 얻은 Sirt3 마우스는 고지식(HFD) 유도 하에 간에 더 많은 지질이 축적되어 있으며, 간 변성 정도가 더 높아 전체적인 NAFLD 진행이 더 심합니다[5].
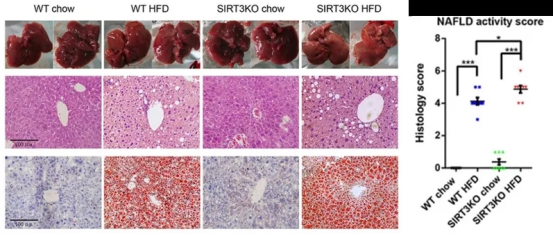
그림 3. SIRT3녹아웃 마우스표형 데이터[5]
결론
SIRT3는 미토콘드리아 기능을 조절하여 전신성 대사 안정 상태에 관여하고 있으며, 현재 연구에서는 SIRT3가 간지방 대사와 NAFLD 질병의 발전 과정에서 어떤 역할을 하는지를 밝혀내고 있으며, 이는 임상 치료 NAFLD의 잠재적 분자 표적이 될 수 있습니다. 그러나 SIRT3를 매개하는 전신효과에 어떤 특정 조직이 주도적으로 작용하는지는 알려지지 않았습니다.이런 면에서 간과 근육 특이성 Sirt3 유전자 녹아웃 동물의 고지방 식사 후 대사 표형에서 큰 차이를 보입니다. 또한, SIRT3가 열량 제한에 비해 NAFLD와 같은 에너지 과잉 조건(고지방음식, 고탄소수음식)에서 조절작용을 하는 심층분자 메커니즘에 대해 잘 알려져 있지 않으며, 세포분자 수준과 생체모델을 결합하여 더욱 검증할 필요가 있습니다.
Cyagen 원스톱 서비스 플랫폼 도움 비알코올성 지방간 연구
NAFLD는 세계적으로 간장질환의 가장 중요한 원인 중의 하나이며 앞으로 몇 십 년 동안 종말기 간질환의 주요 원인이 될 가능성이 높습니다. 이런 질병은 어른과 어린이에게 영향을 줄 수 있습니다.체내 체외 모형은 비알코올성 지방간의 병리적 생리 메커니즘을 밝히고 신약 개발에 중요한 역할을 합니다.
Cyagen원스톱 서비스 플랫폼은 NAFLD 메커니즘을 연구하는 유전자 편집 세포주, 마우스(예를 들면 Sirt3 녹아웃 마우스, 음식 유도를 하는 NAFLD 마우스), 무균 마우스를 제공합니다. 그리고 관련 표형 검사, 기능 검증, 병리 분석 등의 일련의 서비스는 많은 과학자들에게 편리한 서비스를 제공합니다. 더욱 전문적이고 효율적인 과학자 팀은 당신에게 심도 있는 기술 지원을 제공할 수 있습니다. 필요하다면 문의 주시기 바랍니다.
참고 문헌:
[1] S.L. Friedman, et al., Mechanisms of NAFLD development and therapeutic strategies, Nat Med, 24 (2018) 908-922.
[2] M. Choudhury, et al., Reduced mitochondrial function in obesity-associated fatty liver: SIRT3 takes on the fat, Aging (Albany NY), 3 (2011) 175-178.
[3] L. Lin, et al., Regulation of skeletal muscle oxidative capacity and muscle mass by SIRT3, PLoS One, 9 (2014) e85636.
[4] M.T. Chen, et al., SIRT3 Deficiency Promotes High-Fat Diet-Induced Nonalcoholic Fatty Liver Disease in Correlation with Impaired Intestinal Permeability through Gut Microbial Dysbiosis, Molecular Nutrition & Food Research, 63 (2019).
[5] S.T. Li, et al., Sirtuin 3 Acts As a Negative Regulator of Autophagy Dictating Hepatocyte Susceptibility to Lipotoxicity, Hepatology, 66 (2017) 936-952.
About Cyagen
Cyagen은 15 년 동안 발전해 전 세계 수만 명의 과학자에게 봉사했으며, 제품과 기술은 CNS(Cell, Nature, Science) 3 대 저널을 포함한 4500 여 편의 학술 논문에 직접 적용되었습니다.유전자녹아웃, 유전자노크인, 조건부 녹아웃 모델 맞춤형 서비스 외에도 Cyagen에는 전문적인 수술질환 모델팀이 있어 다양하고 세밀한 작은 동물수술 질병모델을 제공할 수 있습니다. 약물선별평가 생쥐 플랫폼은 구미 업계 리더로부터 도입한 면역결핍쥐, 심혈관 및 알츠하이머병 등의 연구에 사용되는 인간화 마우스를 제공할 수 있습니다. 국제 표준화 무균쥐 기술 플랫폼은 무균쥐, 무균동물 맞춤형 서비스, 미생물 균군 이식 서비스 등 무균동물 모델에 기반한 각종 제품과 서비스를 제공할 수 있으며, Cyagen의 성숙하고 안정적인 유전자 편집 생쥐 플랫폼과 결합하여 균군과 유전자의 상호작용 메커니즘을 연구하는데 도움을 줄 수 있습니다.




영업일 기준 1-2일 내에 답변해 드리겠습니다.