

병원성 유전자
현재 ALS 발병 요인이 가장 관련성이 높은 것은 나이와 유전이다. 나이 요인도 신경퇴행성 질환의 가장 큰 원인. 유전성 ALS는 전체 환자의 5%에 불과하지만 여전히 20여 개의 유전자가 ALS의 주범 목록에 올라 있다. 이미 1993년 Superoxide Dismutase 1, SOD1)은 ALS와 밀접한 관련이 있는 것으로 밝혀졌으며 유전성 ALS의 20% 정도가 관련돼 있다. 정상적인 SOD1은 세포에서 생성된 활성 과산화물을 과산화수소와 산소로 변환하는데, 돌연변이 SOD1은 이를 수행하지 못해 뉴런의 산화손상을 초래하고 신경근육 기능 손상을 일으킨다.
희귀질환 유전자: SOD1
돌연변이의 SOD1 단백질 자체는 세포 내에 모여 엔도솜(Endosome)을 형성하지만, ALS에서 SOD1이 가장 많이 모이는 것은 아니고 '다른 것을' 있다. SOD1은 일찍 발견되었기 때문에 관련 연구가 가장 풍부하고 ALS에 대한 연구가 심화됨에 따라 SOD1의 기타 병원성 메커니즘이 점차 발굴되고 있으며, 여기에는 축삭 수송(Axon), 척수 모세관 출혈, 염증 유발, Myelin sheath 파괴 등이 포함된다.
2001년, early-onset ALS와 관련된 ALS2가 발견되었다. 이 유전자에 의해 코드된 단백질은 핵내체(endosome) 환적을 담당한다.
2002년 RNA 가공에 참여한 SETX 발견
2004 년 내질망 및 포내막 이송과 관련된 VAPB를 발견했다.
2006년 ANG와 CHMP2B는 ALS 병원성 유전자 가문에 가입했는데, 전자는 RNA 가공에 참여하고 후자는 핵내체 수송과 자기 소모(autophagy)에 관여한다.
2008년에는 TARDBP 유전자 코드의 TDP-43(TAR DNA binding protein 43)이라는 또 다른 중요한 ALS 관련 유전자가 등장했다.
TDP-43은 AD(아즈하이머병)의 tau,PD(파킨슨병)의 α-syn,HD(헌팅턴병)의 htt와 함께 4대 악인으로 꼽힌다. TARDBP의 전체 명칭은 트랜스반응 DNA 결합단백질 4(transactive response DNA-binding protein 4)로 유전성 ALS에서 차지하는 비중은 매우 작습니다(가족성 비율 <5%와 산발성 비율 <1%). 하지만 97%에 달하는 환자의 운동피질과 척수에서 TDP-43이 모여 만든 내포체(endosome)가 발견되는데 이들 환자에서 TARDBP의 돌연변이가 나타나지 않는 것은 어떻게 된 일일까요?
희귀질환 유전자:TDP-43
TDP-43은 평소에 주로 mRNA와 관련된 작업, 예를 들어 전사 조절및 mRNA의 전단(shearing) 가공, 환적 또는 대사 등에 관여한다. 그러나 ALS 연구에서 세포핵 안에서 일해야 할 TDP-43이 대량으로 세포질로 유입돼 세포핵 내 '노동력'이 부족하고 TDP-43이 담당하는 mRNA가 완제품으로 가공되지 않는 동시에 세포질에 모여 있는 TDP-43이 움직이기 시작해 내포체를 형성하고 뉴런의 정상적인 활동을 해친다는 사실이 밝혀졌다.
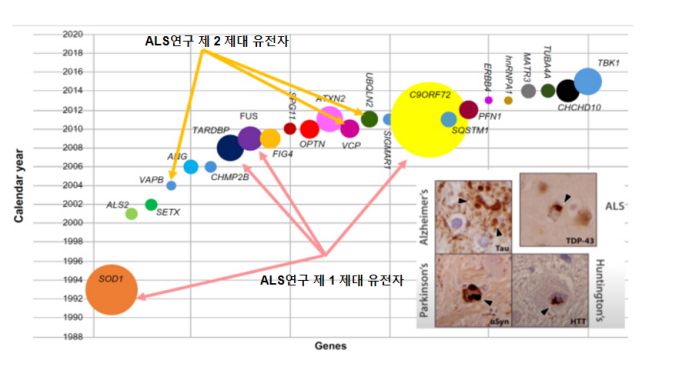
그림 1. TDP-43 퇴적물과 ALS 관련 유전자가 속속 발견되고 있다[1]
2009년에는 FUS(Fused in sarcoma) 단백질과 또 다른 핵내체 수송 융합단백질 FIG4가 발견됐다. FUS는 RNA 결합 단백질로 가족성 ALS와 산발성 ALS에서 돌연변이가 각각 4%와 1%를 차지한다. 이 단백질에 대한 연구는 처음에는 지방육종(sarcoma) 분야에서 TDP-43과 비슷한 역할을 하며 돌연변이는 각각의 단백질이 뭉치도록 유도해 뉴런을 죽인다.
이후 SPG11(세포 내 전이효소, 축삭 성장 관련), OPTN(셀프파지 관련), ATXN2(RNA 가공), VCP(셀프파지), SIGMAR1(프로테아제 시스템, 셀프파지)과 UBQLN2, ubiquitin-proteasome system, 셀프파지) 등이 잇따라 적발됐다. 이 중 UBQLN2(2011년 발견)는 X염색체에 있으며 현재 발견된 ALS 유전자 중 유일하게 성염색체에 있다.
2011년 새로 발견된 유전자 중 진짜 주역은 UBQLN2가 아니라 C9ORF72였다. C9ORF72 조각의 인트론(introns)은 GGGGCC 시퀀스가 400 ~ 2000 회 반복되었다. 정상적으로 10회 이내 반복된다. 이 변이는 가족성 ALS와 산발성 ALS에서 각각 36.7%, 6.3%를 차지하며 가족성 FTD(전측두엽 치매frontotemporaldementia)에서 25%를 차지하기 때문에 유전성 ALS에서 FTD 증상이 자주 나타난다. 연수성(Bulbar ) ALS 중 C9ORF72 관련 환자 비율이 44%에 이른다. 이 유전자의 이름에서 알 수 있듯이 아직 병원 메커니즘이 명확하지 않고, 자가소모(autophagy)나 내포체(endosome ) 수송에 관여한다는 보고가 소수 있다. 이 유전자의 관련 질환은 대부분 유럽과 미국, 아시아 대부분 지역에서 드물다.
이후 10개 가까운 ALS 관련 유전자가 속속 발견되자 일일이 소개하지 않았다. 아래 그림은 모든 ALS 유전자에 대한 세부 사항으로 색상이 핫스팟으로 표시되어 있으며 색상이 표시되지 않은 현재 연구는 비교적 적다.
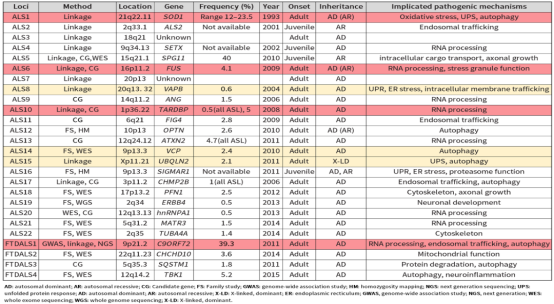
그림 2 ALS 관련 유전자 정보 목록[1]
마우스 모델
ALS는 유전자 편집이나 유전자 변형 모델링을 통해 화학유도 모델보다 더 잘 작동하기 때문에 많은 ALS 유전자 변형 생쥐가 탄생한다. ALS 관련 유전자의 대부분은 상염색체 우성이기 때문에 유전자 변형 생쥐에게 증상을 보이는 것은 어렵지 않다.
SOD1은 가장 먼저 발견되기 때문에 관련 모델 생쥐가 매우 많아 2019년 현재 30종에 육박한다. TARDBP 코딩 TDP-43 관련은 30종 이상, FUS는 10종에 육박하며 나머지 UBQLN2, VCP, VABP와 같은 동물 모델은 적다.
그러면 C9ORF72는요?
물론 이 유전자는 엑손 돌연변이가 극히 적고 병원성 원인도 인트론(Introns)에 있는 단편들이 중복돼 BAC를 통해 박아 넣는 게 일반적이다. 이 유전자는 늦게 발견되지만 ALS와 가장 연관성이 높아 연구가 많다.
현재 여러 종류의 실험 결과를 종합하여 과학자들은 세 종류의 C9ORF72에 관한 가설을 제기했다.
❖지나치게 반복되는 단편은 이 단백질의 기능 손실을 초래한다.
❖이 반복된 전사의 sense RNA와 antisense RNA은 만들어내는 독성
❖이 여섯 개의 염기 코드화된 디펩타이드 반복 단백질이 만들어내는 독성
동물모델의 구축에 대해 과발현에 의한 뉴런의 사망과 운동장애가 비교적 뚜렷하여 중말기의 병세를 모의할 수 있다(그림3에서 녹색 화살표로 나타낸다). 녹아웃은 마우스에 영향이 적고 조기 중기의 병세를 모의할 수 있다.
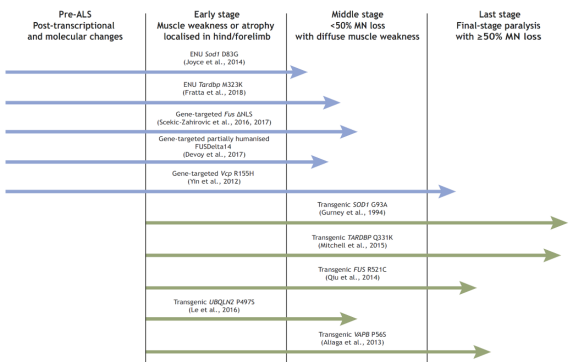
그림 3. ALS유병률[2]
유전자 녹아웃 마우스는 이들 유전자의 기능과 ALS 심층 메커니즘을 연구하는 데 중요한 도구다. 이들 유전자 중 TDP-43 순합 녹아웃 마우스는 번식할 수 없다. 왜냐하면 그 복합체는 운동 뉴런에 대해 일정한 보호 작용을 가지고 있음을 나타내기 때문이다. 반면 SOD1 유전자 녹아웃 마우스는 말초신경질환(peripheral nervous)이 심했다.
유전자 녹아웃 마우스는 돌변이된 생쥐의 유전자를 녹아웃한 것으로 기존 생쥐의 유전자 위에 염기 돌연변이를 한두 곳만 해도 ALS 병리학적 특징을 잘 나타낼 수 있다. 예를 들어 VCPR155H 생쥐의 경우 노령 시에 운동 뉴런의 50%가 사망하며 동시에 세포질에서 TDP-43 내포체(endosome)가 생성되었다. 전반적으로 녹아웃 모델의 운동능력 약화는 미미했다.
인간화 마우스 모델은 최근 몇 년간 유전자 편집 기술의 발전에 따라 핫스팟이 되었다. 마우스의 원래 유전자 위치에서 인간 대응 유전자를 교체하는 것이다. 인간화 된 FUSδ14 마우스와 같이 마우스 세포의 FUS 포지셔닝에 장애가 발생하여 운동 뉴런의 사망을 초래할 수 있다.
참고 문헌 및 인용 사진 출처:
[1] Al Sultan A, Waller R, HeathP, Kirby J. The genetics of amyotrophic lateral sclerosis: current insights.Degener Neurol Neuromuscul Dis. 2016;6:49-64
[2] Giorgio F D , Maduro C ,Fisher E M C , et al. Transgenic and physiological mouse models give insightsinto different aspects of amyotrophic lateral sclerosis[J]. Disease Models& Mechanisms, 2019, 12(1):dmm037424.




영업일 기준 1-2일 내에 답변해 드리겠습니다.