


위장 조직에는 가장 많은 내분비 세포가 포함되어 있다. 많은 위장 호르몬은 포도당 및 지질 안정 상태에서 중요한 작용을 한다. 5-hydroxytryptamine(5-HT, 5-하이드록시세라민)은 가장 흔한 위장 호르몬으로 중추와 외주 기능을 한다. 5-HT의 90% 이상이 장크롬친화성(enterochromaffin)세포에 의해 합성돼 방출된다. Tryptophan hydroxylase(TPH)는 5-HT 시작 합성 및 속도 제한의 핵심 촉매 효소이다. 최근 연구에 따르면 외주5-HT는 백색지방조직의 지방생성을 촉진하고 갈색지방조직의 적응적 열생성을 억제한다. 마우스에서 유전자 침묵이나 약물을 통해 5-HT를 억제하는 합성 키효소 TPH1은 마우스가 식이유도 비만과 포도당 불내성에 저항할 수 있도록 한다. 외주5-HT는 지방 대사와 전신 에너지 밸런스의 중요한 조절인자로 제시됐다.
ZnT8은 췌도 β세포에 축적된 Zinc transporter로 1형과 2형 당뇨병 발병과 밀접한 관련이 있다. 그러나 ZnT8의 계통 에너지 대사에서의 정확한 작용과 그 작용기전은 여전히 매우 적게 알려져 있다. 19년 Diabetes에 발표된 한 연구는 ZnT8 유전자 녹아웃 마우스를 확립함으로써 ZnT8 마우스의 체내에서 지질 대사를 조절하는 메커니즘을 연구하였다. 저자는 먼저 마우스에게서 ZnT8 두드려서 유도된 지질 축적을 발견했고 마우스의 혈액과 조직에서 일련의 생화학적 검사 및 면역염색을 통해 ZnT8/TPH1/5-HT 조절축을 발견했다. 저자는 먼저 마우스에게서 ZnT8 두드려서 유도된 지질 축적을 발견했고 마우스의 혈액과 조직에서 일련의 생화학적 검사 및 면역염색을 통해 ZnT8/TPH1/5-HT 조절축을 발견했다. 더 나아가 세포실험에서 siRNA를 통해 ZnT8을 낮게 두드려 동물실험 결과를 검증했고, ZnT8이 세포 내 아연 이온(Zinc ions) 농도를 조절해 하류 통로 변화에 영향을 줄 수 있음을 발견했다. 이 글에서 우리는 유전자 제거 마우스의 대사 연구에서의 이점을 알 수 있다. 세포 실험으로는 각 기관 및 외주 순환의 대사 변화를 관찰할 수 없기 때문에 이러한 장점은 기존의 세포 실험과는 비교할 수 없을 뿐만 아니라 더욱 설득력이 있다.

표형1:ZnT8 유전자 녹아웃 마우스에서 지방 증가 발현
첫째, 저자는 TALEN 기술을 통해 C57BL/6N 마우스를 ZnT8 단백질로 코딩한 Slc30a8 유전자 녹아웃을 한다 (이 ZnT8 유전자 녹아웃 마우스는 Cyagen에 의해 제공됨). ZnT8 녹아웃 마우스는 야생형 마우스와 형태 및 성장세가 비슷한다. 하지만 수컷과 암컷의 ZnT8 녹아웃 마우스는 모두 지방 체중 증가와 지방뺀체중(Lean body mass) 하강의 추세를 보이고 있다. 흰색지방조직 WAT(부고환 흰색지방조직 eWAT와 피하 흰색지방조직 scWAT 포함)도 모두 눈에 띄게 증가했다. 이 같은 변화는 지방세포의 크기가 커지면서 발생한다.
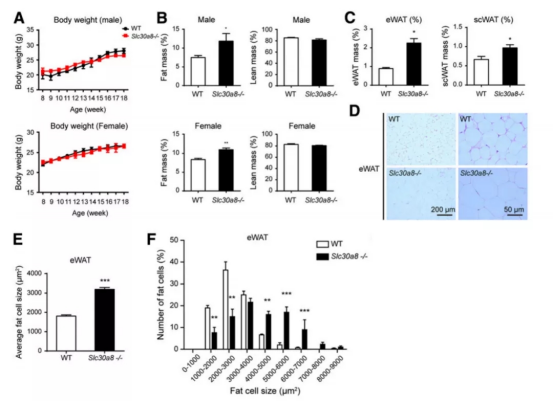
그림1. ZnT8 녹아웃으로 인한 지방 증가
표형 2: ZnT8 녹아웃 마우스 간장의 지질및 글리코겐 증착 증가
간장은 지질대사의 중요한 기관으로 저자는 HE염색, 유홍염색 및 PAS염색법을 통해 ZnT8 녹아웃 마우스의 간장에서 지질과 글리코겐의 퇴적을 발견하였다. 또한 간의 트리글리세리드(triglyceride) 수준이 현저히 높아져 총콜레스테롤이 높아지지 않았는데, 위의 수치는 ZnT8의 부재로 지방조직과 간에 지질이 쌓일 수 있다는 것을 보여준다.
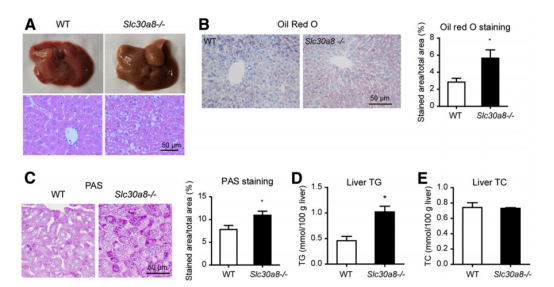
그림 2. ZnT8 녹아웃은 간장에서 지질과 글리코겐의 축적을 초래한다
메커니즘: ZnT8은 장내분비세포에서 발현되어 외주의 5-HT 수준을 조절한다
위장도 당지대사를 조절하는 중요한 기관이기 때문에, 저자는 ZnT8 이 쥐의 장을 두드리는 것이 눈에 띄게 두꺼워진다는 것을 발견했다. PCNA 염색에서 양성으로 염색한 세포가 현저하게 증가하여 ZnT8이 결핍되면 장세포 증식이 촉진된다는 것을 밝혀냈다. 다음으로 저자는 면역 형광 염색을 통해 ZnT8 이 장에서 표현되는지, 그리고 장내에서의 위치를 확인한다. 저자는 ZnT8이 평활근층이나 고유층이 아닌 장내 상피층에 존재한다는 사실을 발견했다. 양성 염색 세포는 삼각형으로 결장 상피 세포층 내에 분포한다. 이어 ZnT8 항체를 장내분비세포의 표지자인 CgA 및 기타 장내 호르몬 표지자와 공염색해 ZnT8이 주로 CgA와 5-HT 양성세포에 존재하는 것을 관찰했다. 5-HT는 가장 흔한 위장호르몬으로 순환계의 90%가 넘는 5-HT가 장에서 합성되어 분비된다.
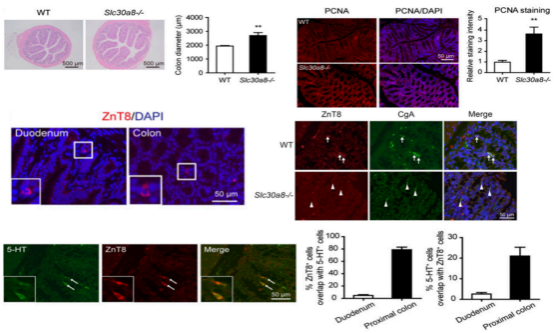
그림 3. 위장에서 ZnT8 의 발현과 위치
주목할 점은 ZnT8 녹아웃 마우스의 결장 5-HT 세포의 염색 강도와 수가 현저하게 증가하였으며, 외주 혈청 5-HT 수준도 야생형 마우스보다 현저히 높았다. TPH1은 외주에서의 5-HT 합성을 담당하며 결장 내 mRNA 및 단백 수준이 모두 현저하게 높아진다. 상술한 결과는 ZnT8이 장내분비세포, 특히 5-HT양성의 장크롬친화성(enterochromaffin)내분비세포에서 표현됨을 시사한다. 반면 ZnT8의 부재는 장내 TPH1의 수준을 높여 5-HT 합성을 촉진해 외주계로 분비된다.
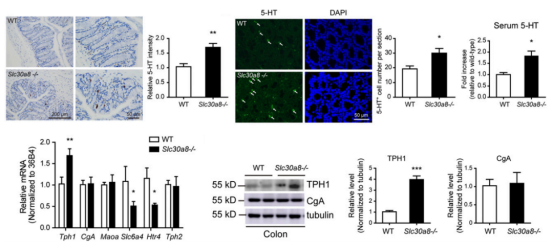
그림 4. ZnT8 녹아웃 마우스 TPH1 수준 및 5-HT 합성분비 향상
ZnT8 이 5-HT 수준을 조절하는 메커니즘을 더 검토하기 위해 저자는 RIN14B 세포를 체외 세포 실험 모델로 사용했고, RIN14B 세포는 Rat의 한 δ세포계로, 이미 5-HT 분비를 연구하는 데 적합한 세포 모델로 여겨졌다. 저자는 RIN14B에서 siRNA를 이용해 ZnT8의 표현을 낮춘 결과 TPH1의 단백질 수준이 3배 가까이 증가했음을 발견했다. ELISA 실험에서 ZnT8이 낮아지면 세포분열액 및 배지(Medium) 상청액중(supernatant liquor)의 5-HT가 현저하게 증가한다는 것을 밝혀냈다. 위의 체외 실험 데이터는 ZnT8 의 결필이 TPH1의 표현를 증가시켜 5-HT 의 합성을 촉진한다는 것을 보여준다. ZnT8은 아연 이온(Zinc ions)의 세포막 통과를 매개하는 운반 단백질이기 때문에 저자는 세포 아연 이온(Zinc ions) 농도의 변화가 TPH1과 5-HT 수준에 영향을 줄 수 있는지 알아보려고 한다. 배지(Medium)에 ZnSO4를 첨가한 뒤 TPH1과 5-HT 수준을 획기적으로 높였다. 반면 아연 이온(Zinc ions) 킬레이트제(chelatingagent) TPEN을 첨가해 아연 이온(Zinc ions)을 제거하면 TPH1의 mRNA와 단백질의 표현이 약화되지만 5-HT의 배지상청액 분비에 유의미한 영향은 없다. 위의 결과는 ZnT8 이 세포 내 아연 이온 농도를 조절하여 TPH1 의 표현에 영향을 줄 수 있음을 보여준다.
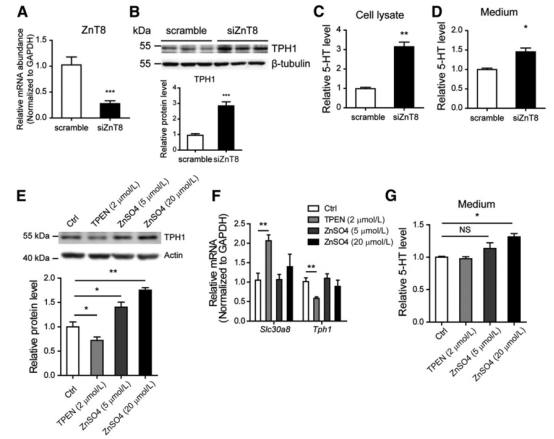
그림 5. ZnT8 아연 이온 조절로 TPH1 표현에 영향
결론
저자는 먼저 유전자 녹아웃 마우스에서 ZnT8이 빠진 마우스의 지질대사에 중요한 조절기능을 발견해 마우스 체내의 표형 및 메커니즘에 대해 설명한 뒤 체외 세포모델 실험을 통해 보조증명했다. 전체 연구는 장내분비세포 중 ZnT8이 TPH1의 표현을 조절하고, 나아가 위장호르몬 5-HT의 합성을 조절하며, 5-HT가 외주계통으로 분비돼 마지막으로 전신의 지질대사 균형을 조절하는 것으로 요약된다. 이 글은 Cyagen가 제공하는 ZnT8 유전자 녹아웃 마우스의 이점을 살려 지질대사 연구에 성공적으로 적용했다.
우리가 어떤 유전자의 조절기능을 연구할 때 동물모델과 세포모델로부터 동시에 검증을 받을 수 있다면 조절 작용을 더욱 충분히 실증할 수 있고, 실험 설계의 엄밀성을 높일 수 있으며, 특히 고득점 문장의 발표에 더욱 중요하며, 또한 세포 모델과 동물 모델을 동시에 구축하면 시간을 절약할 수 있고, 문장을 더 빨리 발표할 수 있다.
Cyaegn 체내 체외 원스톱 서비스 플랫폼
Cyagen는 장기간 유전자 편집 세포와 동물 모델 구축에 힘쓰고 있으며, 경험이 풍부한 전문가 팀과 성숙하고 안정적인 기술 플랫폼을 보유하고 있으며, 고객은 전 세계 수십 개 국가와 지역에 걸쳐 있다. 우리는 고객에게 목적 유전자의 발현 조절을 위한 세포 모델과 동물 모델 및 관련 표형 검측, 기능 검증, 병리 분석 등의 일련의 서비스를 제공할 수 있으며, 많은 과학 연구자에게 편리한 서비스를 제공할 수 있다.
원문 검색:
Zhuo M, Hui L, Wen S, et al. Deficiency of ZnT8 Promotes Adiposity and Metabolic Dysfunction by Increasing Peripheral Serotonin Production. Diabetes. 2019.
DOI: 10.2337/db18-1321
About Cyagen
Cyagen은 15 년 동안 발전해 전 세계 수만 명의 과학자에게 봉사했으며, 제품과 기술은 CNS(Cell, Nature, Science) 3 대 저널을 포함한 4500 여 편의 학술 논문에 직접 적용되었습니다.유전자녹아웃, 유전자노크인, 조건부 녹아웃 모델 맞춤형 서비스 외에도 Cyagen에는 전문적인 수술질환 모델팀이 있어 다양하고 세밀한 작은 동물수술 질병모델을 제공할 수 있습니다.약물선별평가 마우스 플랫폼은 구미 업계 리더로부터 도입한 면역결핍마우스, 심혈관 및 알츠하이머병 등의 연구에 사용되는 인간화 마우스를 제공할 수 있습니다.국제 표준화 무균쥐 기술 플랫폼은 무균마우스, 무균동물 맞춤형 서비스, 미생물 균군 이식 서비스 등 무균동물 모델에 기반한 각종 제품과 서비스를 제공할 수 있으며, Cyagen의 성숙하고 안정적인 유전자 편집 마우스 플랫폼과 결합하여 균군과 유전자의 상호작용 메커니즘을 연구하는데 도움을 줄 수 있습니다.




영업일 기준 1-2일 내에 답변해 드리겠습니다.