

관련 배경
CAR-NK 세포에 대한 이야기를 하기 전에, 지난 몇 년 동안 더 유명했던 CAR-T 세포에 대해 이야기하겠습니다.
무엇이 CAR-T 세포입니까? CAR의 전체 이름은 Chimeric Antigen Receptor이며, 키메라 항원 수용체로 번역되었다. 그 구조는 세포외 구조 영역, 막횡단영역(transmembrane domain)과 세포내 신호 구조 영역을 포함하고, 세포외 구조 영역은 표적에서 종양 표적 항원을 식별하는 scFv (VH-linker-VL), 경첩 영역(Hinge area)을 포함한다. 세포내 신호 구조 영역은 협동공자극 분자(CD28 또는 4-1BB)와 CD3ζ 신호 구조 영역으로 구성된다. CAR-T 세포는 CAR 로 무장한 T 세포이고, CAR 분자의 scFv 세그먼트는 T 세포 표적성을 부여하고, 세포 내 신호 영역은 T 세포의 동력 엔진으로 T 세포에 강력한 활성화 동력을 부여한다. 따라서 CAR-T 세포의 전투력은 T 세포보다 현저히 향상되었다.
CAR-T세포는 과계성 면역치료 분야의 스타로 이미 7명의 형제자매가 지구 곳곳을 누비며 암세포 사멸의 중요한 사명을 다하고 있다. 그러나 CAR-T세포는 완전무결하지는 않다:우선 그것은 고도로 맞춤화된 항암 무기이며 또한 응용전장도 매우 제한적이다:환자 자신의 치료에만 사용할 수 있기 때문에 그것의 제조가 매우 어렵고 대량생산이 어렵다. 다음으로, CAR-T세포는 매우 강력한 항암무기로서, 킬 암세포와 동시에 스스로 '발열'하여 전장에서 땀을 많이 흘리며(사이토카인을 다량 방출하여) 심각한 손상을 입힙니다(사이토카인 폭풍). 또 CAR-T세포는 표적성이 매우 높은 무기이지만 표적 선택이 적절하지 않을 때도 비타격 표적(정상적인 조직과 기관)을 잘못 쳐서 민간인 사상자(탈표적 독성)를 발생시킬 수 있다.
CAR-T세포의 이러한 결함을 극복하기 위해 현재 많은 연구자들이 서로 다른 방법을 시도하고 있다. 예를 들어 T세포에 대해 약간의 수술을 하고, 그 표면의 TCR과 CD52 등 그 응용 장면을 제한하는 부품들을 두드려 제거하고(GVHD를 피하고), 산업화 생산을 실현하며, 그 응용 범위를 넓힌다(이체 치료에 사용된다). 이와 함께 일부 연구자도 T세포의 다른 형제자매에게 주목하고 있는데 NK세포가 그 중에서도 가장 주목받고 있다.
NK 세포
NK세포의 큰 이름은 자연살상세포(Nature killer cell)로 1957년에 발견된 인체의 고유 면역세포로, 외주 단핵세포의 10% 정도를 차지한다. 외적의 침입에 대항하는 중요한 무장력인 바이러스 감염에 맞서 종양을 감시하고 사멸하는 데 중요한 역할을 한다. NK세포는 작전 범위가 훨씬 넓고(이체치료에 사용 가능) 킬은 외적이 있을 때 T세포처럼 번거로운 준비를 하지 않아도 되며 항상 경계태세를 유지하며 언제든 투입돼 적을 죽일 수 있다. NK세포는 자신의 적과 아군을 정확히 식별하는 구분 시스템을 가지고 있으며, 그 표면에는 다양한 수용체가 발현되어 있으며, 기능에 따라 크게 두 가지 유형으로 나눌 수 있다. 즉, 활성화 수용체와 억제성 수용체이다. NK세포의 전쟁 준비 상태는 이들 수용체의 리간드 (ligand)상호작용을 통해 정밀하게 조절될 수 있다.
NK세포는 주로 세 가지 종류의 무기를 통해 종양세포에 대항한다
❖천공소 및 과립효소를 함유한 세포질 입자를 방출함으로써 표적세포를 직접 살상한다.
❖IFN-γ, TNF-α와 같은 사이토 카인을 방출하고 종양 세포 표면의 해당 수용체와의 상호 작용을 통해 종양 세포의 세포 사멸을 유도한다.
❖Fc수용체 CD16은 항체의 Fc단과 결합해 항체에 의존하는 세포가 매개하는 세포독성(ADCC)을 자극해 세포를 살상한다.
따라서 NK세포는 종양이라는 악마에 대항하는 중요한 장기이기도 하다. NK세포상 T세포에 'CAR 한 대'만 탑재해도 종양에 대항하는 전투력을 크게 증강시킬 수 있으며 CAR-T세포의 많은 단점을 극복할 수 있을 것으로 기대된다.
CAR 분자설계의 차이점과 동일점
지금까지 다수의 CAR-NK세포 연구에서 사용된 CAR 분자구조는 모두 CAR-T세포를 위해 설계되었으며, 이러한 CAR 분자는 NK세포에서도 기능할 수 있지만, 많은 연구자들은 여전히 NK세포에 더욱 적합한 CAR 분자를 더욱 설계하고 최적화하는 데 힘쓰고 있다. 표 1은 현재 CAR-NK 세포 연구에서 가장 많이 사용되는 CAR 분자 구조를 요약한 것이다.연구에 따르면 CD28/4-1BB 공자극 분자를 포함하는 CAR보다 공자극 분자가 2B4(NK세포 특이성의 공자극 신호)인 CAR를 발현하는 NK세포는 증식능력, 사이토카인 분비능력과 항종양 활성이 강하며, NK 특이성의 공자극 신호 분자는 CAR-NK 성능을 증강시키는데 중요한 역할을 한다고 설명하였다. NK세포를 기반으로 한 CAR 분자구조가 더욱 커지면서 CAR-NK세포의 항암전력도 꾸준히 향상될 것으로 기대된다.
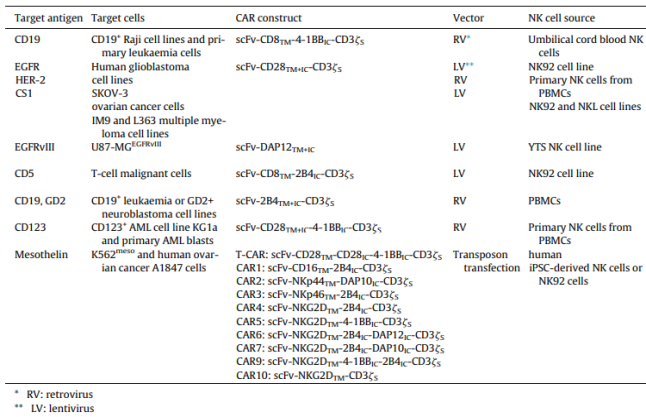
표 1. 현재 연구에서 많이 사용되는 CAR 분자구조 [1]
CAR-NK세포 제작 준비
T세포와 달리 NK세포는 이물질 치료에 사용될 때 GvHD를 일으킬 위험이 매우 낮기 때문에 CAR-NK세포는 이물질 치료에 사용할 수 있는 현물형 제품이 될 것으로 기대된다. 또 이 특성은 NK세포의 공급원을 크게 넓혔다. 그림 1과 같이 이미 여러 출처의 NK세포는 모두 임상 수준의 제조를 실현할 수 있으며, 여기에는 외주혈(PB), 제대혈(UCB), 유도만능줄기세포(iPSC) 및 NK세포계 NK-92가 포함된다. 현재, 인간 외주단핵세포 (PBMC) 는 가장 중요한 NK 세포의 원천이며, NK 세포를 통해 테스트 키트 분류함으로써 고순도 NK 세포를 쉽게 얻을 수 있어 임상급 NK 세포 제비를 실현할 수 있다. 외주 유래한 NK세포에서 제조된 CAR-NK세포는 통상 CD56dimCD16+NK세포를 위주로 하며 그 비중은 90% 이상에 이를 수 있다. 이러한 NK세포는 비교적 강한 독성작용을 가지고 있으나 그 증식능력은 비교적 약한다. 제대혈은 또한 NK세포의 중요한 공급원이다. PB출처의 NK세포와 마찬가지로 제대혈 중의 NK세포도 분선을 통해 부집합할 수 있다.
PB 출처한 NK세포와 달리 UCB 출처한 NK세포는 미성숙한 표형과 낮은 세포독성을 보이는 경우가 많다. 그러나 PB 와 UCB 출처의 CAR-NK 세포는 출처가 고르지 않아 표준화가 어렵다. iPSC는 무한대의 대물림 특성과 유전자 편집성을 가지고 있어 CAR-iPSC의 제조를 실현할 수 있지만, CAR-iPSC는 안정적인 공급원으로서 지속적으로 매우 균일한 CAR-NK 세포를 제조할 수 있다. iPSC가 유도하는 NK세포는 UCB 출처한 NK세포와 비슷한 면역표현형을 갖고 있으며 모두 미성숙한 NK세포가 주를 이룬다.
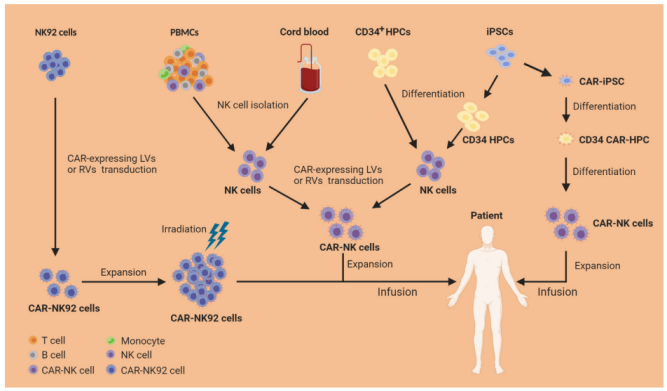
그림 1 NK세포 출처 및 서로 다른 CAR-NK 제조공정 [1]
CAR-NK세포의 연구진전
아직 CAR-NK 세포 치료 제품이 출시되지 않았으며, CAR-T 세포의 임상 연구 수에 비해 CAR-NK 세포 연구는 아직 걸음마 단계이다. 그러나 최근 CAR-NK세포치료연구에 관한 보도가 많아지면서 많은 기업들이 CAR-NK세포치료 코스에 적극적으로 나서고 있다. clinicaltrials.gov에서 CAR-NK를 검색함으로써 현재 35건의 CAR-NK세포 임상시험이 진행 중이거나 종료되었으며, 대부분은 Phase 1/2의 연구 단계에 있는 것을 발견했다.
표적 분포의 경우 혈액 종양은 주로 CD19(10개, 이중 표적Double targets 포함), BCMA(3 개), CD33 개 (2 개), CD22 개 (2 개, 이중 표적Double targets 포함) 에 집중되어 있다. 고형 종양의 치료 목표는 주로 NKG2D(4개), ROBO1(3개), 메소텔린Mesothelin (1개), PSMA(1개) 입니다.
지리 분포를 연구하면 현재 임상실험을 가장 많이 하고 있는 나라는 중국, 그 다음 미국, 그 다음 다른 나라이며, 그림 2와 같다.
치료효과에 대하여 말하자면, CAR-NK세포의 치료효과는 일부 임상전 및 임상연구에서 이미 초보적으로 검증되었다. CD19를 대상으로 한 CAR-NK 임상시험에서 치료받은 종양 환자 11명 중 7명은 완치 판정을 받았고 CRS와 신경독성 등 부작용도 나타나지 않아 NK세포의 양호한 응용 전망을 보였다.
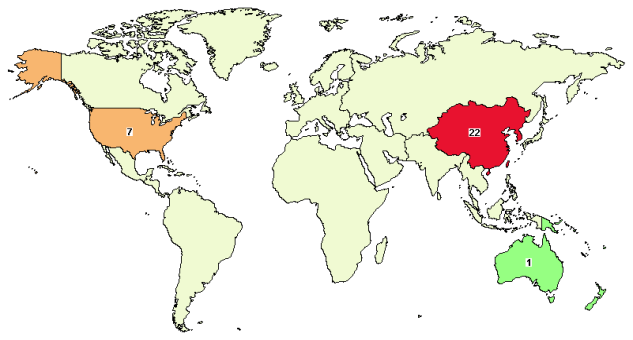
그림 2. CAR-NK 임상연구 수량분포도
결론
T세포에 비해 NK세포는 독특한 작용기전을 가지고 있어 면역작용을 할 때 사전활성이 필요하지 않으며 목표물의 식별에 MHC 분자의 제한을 받지 않기 때문에 NK세포는 이체치료에 적합한다. 또 CAR-NK세포치료는 독의 부작용이 약해 통상 CAR-T세포와 유사한 심각한 CRS 및 신경독성 작용을 일으키지 않는다. 그러나 CAR-NK 세포 요법도 NK 세포의 증식과 순도, CAR 유전자 전달 도구의 선택과 전달 효율과 같은 도전에 직면해 있다. 그러나 CAR-NK에 대한 연구는 아직 초기 단계이며, 연구가 진행됨에 따라 이러한 문제들은 결국 하나씩 해결될 것이며, CAR-NK 세포 요법도 종양 치료 분야에서 혁명적인 진전을 이룰 것으로 믿습니다.
참고 문헌:
[1]Xie G, Dong H, Liang Y, Ham JD, Rizwan R, Chen J. CAR-NK cells: A promising cellular immunotherapy for cancer. EBioMedicine. 2020;59:102975.
Cyagen세포 치료 원스톱 솔루션은 종양 면역세포 치료 임상 전 연구를 돕다
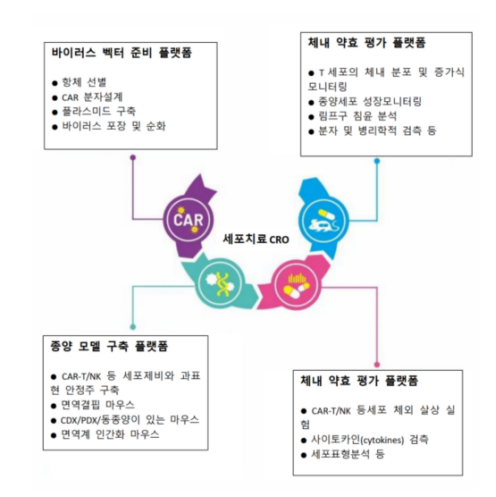
CAR-T 기타 세포치료의 전임상연구에서 세포모델, 동물모델의 선택은 모두 매우 중요하며 연구의 목적을 명확히 하고 효과적인 실험모델과 방안을 수립하면 연구를 반배시킬 수 있다. Cyagen은 세포치료 원스톱 서비스를 제공하며 항체 선별부터 안정주 구축, 세포/동물 모델 구축부터 약효학 평가까지 CAR-T 및 기타 세포치료 연구개발 과정을 더욱 가속화한다. 필요하시면 문의 연락주세요~




영업일 기준 1-2일 내에 답변해 드리겠습니다.