

조절성 T(Treg)세포는 면역체계의 과도한 활성화와 이상활성화를 억제하는 면역안정 유지에 매우 중요한 역할을 합니다. 종양 마이크로환경(TME) 에서 Treg세포 억제 T작동 세포 (CD8+T세포 포함) 는 암세포를 죽이는 주역입니다. 따라서 종양미세환경에서 CD8+ T세포와 Treg세포 사이의 균형은 각종 암의 예후에 매우 중요합니다.
면역체크포인트(Immune checkpoint ) 차단요법은 암 환자에게 새로운 희망을 주었습니다. 하지만 절반이 넘는 환자가 이 치료 후 면역응답을 생기하지 않습니다. 따라서 바이오마커를 정의해 응답자를 선택하고 보다 효과적인 면역항암요법을 개발할 필요가 있습니다. 최근 연구에서 효과T세포와효과Treg세포(eTreg, 활성화 Treg세포) 사이의 PD-1 발현 균형이 PD-1 차단 요법의 예측적 표지물로 활용될 수 있다는 사실이 밝혀졌습니다.
효과 T세포와 Treg세포가 서로 다른 대사특성을 갖고 있다는 점을 감안해 2022년 1월 일본 국립암센터 연구진은 Cancer Cell에 'Lactic acid promotes PD-1 expression in regulatory T cells in highly glycolytic tumor microenvironments' 라는 제목의 글을 올렸습니다. TME에서PD-1을 나타내는 효과 T세포와 Treg세포 사이의 균형이 어떻게 만들어지는지 대사적 관점에서 논의합니다. 젖산이 Treg세포의 대사 검사점이 되고 TME에서 면역 응답을 제어할 수 있다고 본 것입니다.

재료와 방법
이번 연구에서 연구진은 말기 위암, 비소세포폐암, 악성 흑색종 환자의 종양 샘플과 종양침윤림프구(TIL)를 채취했습니다. 체외 실험은 생쥐와 인간의 일부 세포계에서 진행되었는데, 생쥐 결장 암세포계와 사람 T세포 백혈병 세포계 Jurkat E6.1 등을 포함합니다. 동시에, 그들은 또한 동물 모델에서 생체 내 연구를 수행하고 있으며, Slc16a1 유전자 완전 녹아웃 및 조건부 녹아웃 마우스는 모두 Cyagen에 의해 제공됩니다.
이들은 주로 RNA시퀀싱(RNA-seq)과 전외현자 그룹 시퀀싱 및 돌연변이 분석을 적용하고 ChIP-seq 데이터를 처리해 분석했습니다. 세포사멸과 증식 분석, 면역조성화(IHC) 분석도 병행했습니다. LC-MS, Western blotting,RT-PCR 등의 분석도 전개됐습니다.
연구결과
1● 젖산증강eTreg세포의 PD-1표현
우선 연구팀은 TME에서 Treg 세포의 PD-1발현에 어떤 요인이 영향을 미치는지 연구했습니다. 종양은 주로 포도당을 이용하여 해당과정을 촉진하여 생존을 유지하게 합니다. 저포도당과 고젖산 환경은 효과 T세포에 적합하지 않지만 Treg세포는 다량 침윤되어 면역억제기능을 나타냅니다. 위암과 비소세포폐암 시료의 분석을 통해 eTreg세포의 PD-1발현이 고도로 당효가 풀린 종양에서 상향 조정되는 반면 종양침윤 CD8+T세포와 Treg세포의 비율 및 CD8+T세포의 PD-1발현이 현저히 감소되는 것을 발견했습니다.
이어 이들은 eTreg 세포의 PD-1발현이 CD8+ T세포보다 더 높은 메커니즘을 탐색했습니다. 젖산이 종양 효분해의 최종 결과물인 점을 감안하면 젖산 수송 단백질을 코딩화한 Slc16a1 유전자가 PD-1+eTreg 세포에서 높게 발현돼 MCT1에 집중한 것입니다(그림 1). ChIP-seq 데이터를 분석한 결과 FOXP3가 eTreg세포에서 MCT1과 그 상호작용 단백질 CD147의 발현을 촉진한다는 사실을 발견했습니다.
그렇다면 젖산은 eTreg 세포의 PD-1 표현과 어떤 관련이 있을까? eTreg 세포의 PD-1 표현은 젖산 농도가 증가함에 따라 현저히 높아지지만 CD8+T 세포의 PD-1 표현은 반대 추세를 보이고 있습니다. 또한 젖산은 eTreg 세포의 증식을 촉진하고 사멸을 억제합니다. 이 결과 낮은 포도당과 높은 젖산 환경에서 eTreg세포가 MCT1을 통해 젖산을 흡수해 PD-1 발현을 향상시킨 것으로 나타났습니다.
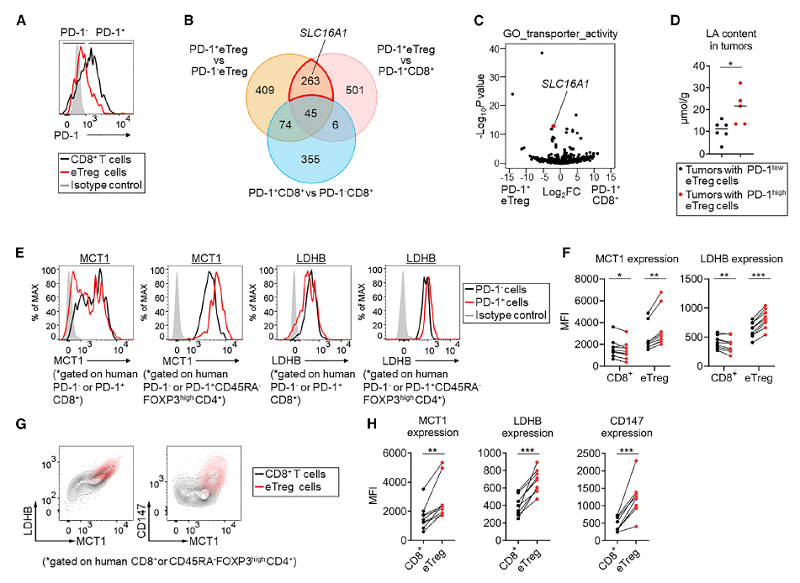
그림1. 젖산은 MCT1을 통해 eTreg세포를 유도하여 PD-1을 표현한다
2●PD-1 차단 eTreg세포 면역억제 활성증강
PD-1 차단은 이 같은 환경에서의 eTreg세포의 활성을 높여 CD8+T세포의 효과기능을 더 강하게 억제한다는 분석이 나왔습니다. 이는 고젖산이 유도한 PD-1high eTreg 세포와 PD-1 차단 치료 실패 사이에 직접적인 연관이 있음을 의미하기도 합니다. 동물 모델의 분석과 결합해 MYC 표현이 당효분해 활성을 조절하고 고젖산 종양 마이크로환경을 만들어 T 세포군의 PD-1 표현 균형을 조절하는 것으로 나타났습니다.
3● 젖산증강eTreg세포의 PD-1표현
연구진은 이후 체내 실험을 진행하여 간내 종양이 확실히 당효해를 증진시키고 종양미세환경에서 Treg세포의 PD-1 발현을 촉진시키며 CD8+T세포의 수와 PD-1 발현을 현저하게 감소시킨다는 것을 발견했습니다. PD-1 항체요법은 간 내 종양에 항종양 작용을 하지 않고 종양 내 트레그세포를 활성화시킵니다. 요컨대 종양미세환경에서 다량의 젖산이 Treg세포에 PD-1을 유도하여 PD-1 항체요법에 내성을 갖게 됩니다. Treg 세포의 젖산 대사를 억제하면 Myc 를 표현하는 종양의 PD-1 차단 요법에 대한 저항성을극복할 수 있습니다.
결국 이들은 여러 암 환자 코호트에서 위암, 비소세포폐암, 악성 흑색종 등 PD-1 차단 요법의 효과에 어떤 영향을 미치는지를 확인했습니다. LDHA나 MYC가 높은 표현을 한 환자들은 비교적 무진행 생존기간이 짧은 것으로 나타났습니다. 당효해 및 젖산 대사 유전자의 발현을 통해 PD-1 차단요법의 암환자에 대한 유효성을 예측할 수 있습니다.
결론
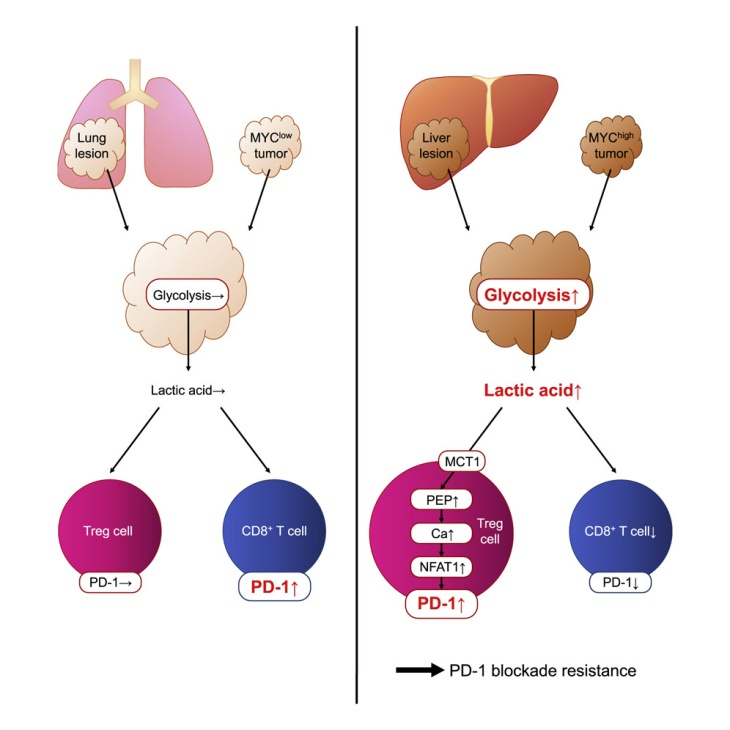
결론적으로, 이 연구에 따르면 고도로 당효해된 종양은 포도당을 소비하고과도한 젖산을 방출하기 때문에 Treg세포의 PD-1 발현과 활성을 억제하는데 이는 PD-1 차단요법의 효과를 일정 부분 저하시킬 수 있습니다. 연구진은 젖산이 Treg 세포 특유의 대사 검사점이라는 점이 새로운 면역요법 개발에 새로운 아이디어를 제공했다고 보고있습니다.




영업일 기준 1-2일 내에 답변해 드리겠습니다.