

유전자는 많은 인간 질병의 내부 요인이며 질병 관련 유전자에 대한 연구는 생명의학 연구 분야의 주류입니다. 질병 관련 유전자와 이러한 유전자의 정보를 빠르게 알 수 있는 방법은 무엇일까요? 연구자들의 시간과 에너지를 절약하기 위해 Cyagen은 새로운 프로젝트인 'Gene of the Week'를 시작하게 되었습니다. 매주 목요일마다 유전자를 하나씩 소개하여 매주 한 개의 유전자를 빠르게 이해할 수 있도록 도와 드리겠습니다.
오늘 우리가 이야기 할 주인공은 바로 APP 유전자입니다.
Gene location:chromosome 21 (21q21.3)
Full length: spans 290 kb and includes 18 exons
Values of amino acid: 639-770AA
Conservation: Nematodes, drosophila, and all vertebrates
Cleavage product: sAPPα, sAPPβ, Aβ, C83, C99, AICD, P3
Cell location: membrane protein
Protein molecular weight: ~87kd
Number of major protein amino acids: 770,695,751
Gene family: APLP1, APLP2
Gene location:chromosome 16 (16 C3.3;)
Full length: spans 222 kb and includes 19 exons
Knockout (KO): prolong the long-term enhancement; affects learning and memory; both the App gene knockout (KO) and conditional knockout (cKO) mouse models are available in our Mouse Model eBank.
Overexpression: Long-term enhancement and weakening
Common models: 5×FAD, 3×Tg, APP/PS1, APPswe
Gene location:chromosome 11 (11q11)
Full length: spans 217 kb and includes 18 exons
Knockout (KO): no validation data
Overexpression: no information
Common models: APP21, APPKI, APPPS1
아밀로이드전구체단백질(Amyloid Precursor Protein, APP) 자체의 주요 생리적 기능은 철저히 연구되지 않았지만 APP의 일부 돌연변이는 Aβ의 생산을 증가시킬 수 있거나 Aβ가 응집될 가능성이 더 높다. Aβ의 응집(올리고머이든 노인반이든)은 세포 칼슘 신호의 문란과 미토콘드리아 기능의 장애를 유발할 수 있으며, 더 나아가 시냅스의 상실과 뉴런의 사망, 그리고 일련의 신경 염증 발생을 초래하는데, 이것이 바로 현재 AD 발병 가설의 주요 지위를 차지하고 있는 Aβ 가설이다. 또 다른 연구에서는 Aβ가 AD의 부산물로 AD의 초기 단계에서 뉴런에 보호 효과가 있다고 믿고 있다.
일반적으로 APP는 ADAM10 (일종의 α-secretase)에 의해 절단되고, 이는 Aβ를 직접 절단하기 때문에 Aβ의 생성을 방지하지만, APP가 BACE1에 의해 먼저 절단될 때 Aβ 생성의 전제가 생긴다. 많은 가족성 AD에서 APP 돌연변이는 크게 세 가지로 나눌 수 있다.
a. β-cutting 부위(예: swe 등)에서 돌연변이가 발생하면 β-cutting이 증가한다.
b. γ-cutting부위(예: Flo, Lon 등)에서 돌연변이가 발생하면 Aβ 발현을 증가시킨다.
c. Aβ내부(Iow, Dut 등)에서 돌연변이가 발생하면 Aβ의 응집 능력을 변화시킴으로써 AD를 유발한다.
또한 IDE, NEP, ECE, ACE, MMP 등과 같은 Aβ 제거에 관여하는 효소의 활성도 AD-afflicted 조직에서 감소하는 것으로 확인됐으며 최근 몇 년 동안 APP의 일부 돌연변이가 AD 발병률을 낮춘다는 사실도 밝혀졌다.
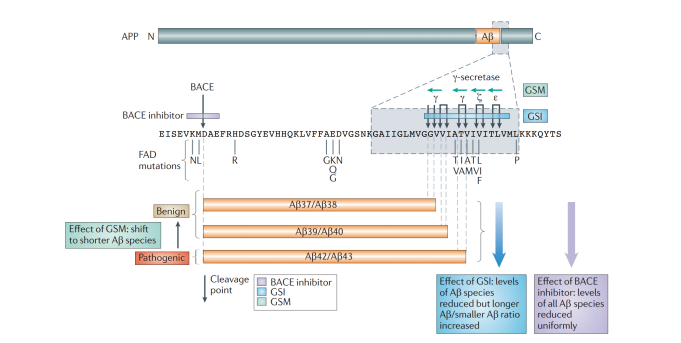
그림1. APP 돌연변이와 절단
알츠하이머병은 세계에서 가장 흔한 신경 퇴행성 질환 중의 하나다. 임상 증상은 세포 외 아밀로이드반과 세포 내 신경섬유매듭으로 나타내 뉴런 기능 장애와 세포 사멸을 초래한다. Aβ는 칼슘항상성(calcium homeostasis), 미토콘드리아 산화스트레스, 에너지 대사와 포도당 조절에 영향을 미치며 궁극적으로 신경 세포 사멸로 이어진다. 알츠하이머병은 또한 신경섬유매듭의 존재를 특징으로 하며, 이러한 매듭은 미세소관 관련 단백질(Microtubule-Associated Protein)인 Tau가 과도하게 인산화된 결과이다. PKC, PKA, Erk2와 같은 다른 키나아제도 참여하지만 Tau의 인산화는 주로 GSK-3와 CDK5 키나아제에 의해 발생된다. Tau 단백질의 과인산화로 인해 Tau 단백질이 미세소관에서 분리되어 미세소관의 불안정과 세포 내 Tau 단백질의 올리고머화가 초래된다. 신경섬유매듭은 Tau 올리고머화의 결과이며 신경세포 자멸사로 이어진다. 현재 연구에 따르면 Aβ의 독성은 Tau 과인산화를 일으키는 원인 중 하나이다.
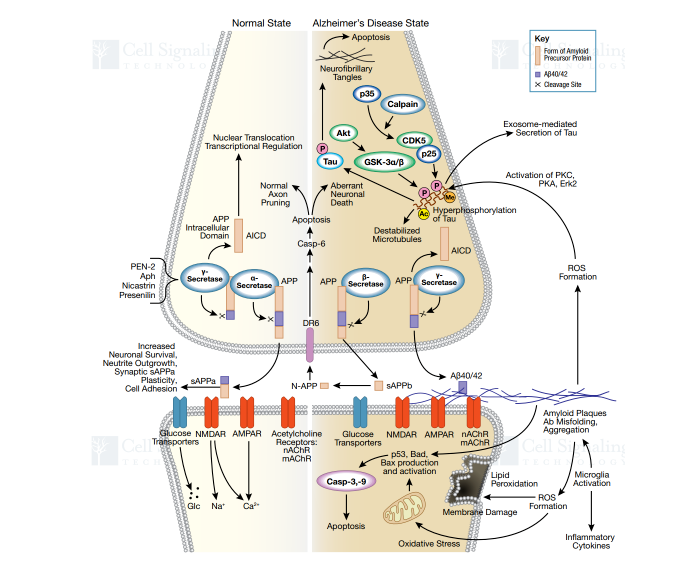
그림2. AD 신호 통로
인간 조직에서 APP 유전자의 발현
APP는 성인의 뇌 조직에서 많이 발현되며 갑상선과 신장에서도 발현량이 높다. 그러나 다른 주요 장기 및 소화관 조직에서는 expression abundance가 낮다.

그림3. APP의 발현(relative expression values)
References:
1. Karran E, Mercken M, De Strooper B. The amyloid cascade hypothesis for Alzheimer's disease: an appraisal for the development of therapeutics. Nat Rev Drug Discov.2011 Aug 19;10(9):698-712. DOI: 10.1038/nrd3505. PMID: 21852788.
2. Sala Frigerio C, De Strooper B. Alzheimer's Disease Mechanisms and Emerging Roads to Novel Therapeutics. Annu Rev Neurosci. 2016 Jul 8;39:57-79.
DOI: 10.1146/annurev-neuro-070815-014015. Epub 2016 Apr 4. PMID: 27050320.
3. Reitz C. Alzheimer's disease and the amyloid cascade hypothesis: a critical review. Int J Alzheimers Dis. 2012;2012:369808. DOI: 10.1155/2012/369808. Epub 2012 Mar 17. PMID: 22506132; PMCID: PMC3313573.




영업일 기준 1-2일 내에 답변해 드리겠습니다.