

B6-Igl KO 마우스 모델 소개: B 세포 및 항체 연구를 위한 혁신적인 Knockout 마우스
Cyagen에서 개발한 최신의 B6-Igl Knockout(KO) 마우스 모델은 κ Light-chain 면역글로불린(Immunoglobulins, Ig)만을 발현하며, 연구자들에게 B 세포 발달 및 항체 다양성 연구에 유용한 연구 모델을 제공합니다. 이 Igl KO 마우스 모델은 B6 배경에서 λ Light-chain gene segment를 삭제하여 κ Light-chain의 면역 반응, 자가 면역 질환, 면역글로불린 다양성에서의 역할을 집중적으로 연구할 수 있게 개발되었습니다. 독특한 유전적 프로필을 가진 B6-Igl KO 마우스 모델은 항체 기반 연구 및 치료법 발견의 진전을 위한 중요한 인사이트를 제공합니다. 면역학 분야의 전임상 및 생의학 연구에 최적화하기 위한 B6-Igl Knockout(KO) 마우스 모델의 특징과 응용 분야를 살펴보세요.
면역글로불린(Immunoglobulins): 항체 활성의 핵심 요소
면역글로불린(Ig)은 항체와 유사한 구조를 가진 "Y" 모양의 큰 당단백질(Glycoprotein) 분자로, 면역계에서 항원을 인식하고 중화시키는 데 사용됩니다. 면역글로불린(Ig)은 분비형(용해성)과 막 결합형(소수성 막 통과 영역 포함) 두 가지 형태로 분류됩니다.
막 결합형 면역글로불린(Membrane-bound Immunoglobulins, mIg)은 B세포 항원 수용체(B cell antigen receptor, BCR) 복합체의 일부로 B 세포 표면의 존재하고, 항원을 인식하며 B 세포 활성화 및 분화에 도움을 주는 역할을 합니다.
보통 항체(Ab)로 불리는 분비형 면역글로불린(Secreted immunoglobulins, sIg)은 주로 혈청과 체액에서 발견되며, 혈장 세포(분화된 B 세포)에서 형성되어 특이 항원과 결합하고 면역 반응을 매개할 수 있습니다.
면역글로불린(Ig)은 두 개의 동일한 Light-chain과 두 개의 동일한 Heavy-chain으로 구성됩니다.[1-2] 포유류 동물 체내에 kappa (κ)와 lambda (λ) 두 가지 유형의 Light-chain을 보유하고 있지만, 개별 B 세포는 한 종류의 Light-chain만을 발현합니다. 이번 새로 개발한 B6-Igl Knockout 마우스 모델은 λ Light-chain을 Knockout(KO)하여 κ Light-chain 면역글로불린(Ig)만을 발현하도록 제작되었습니다.
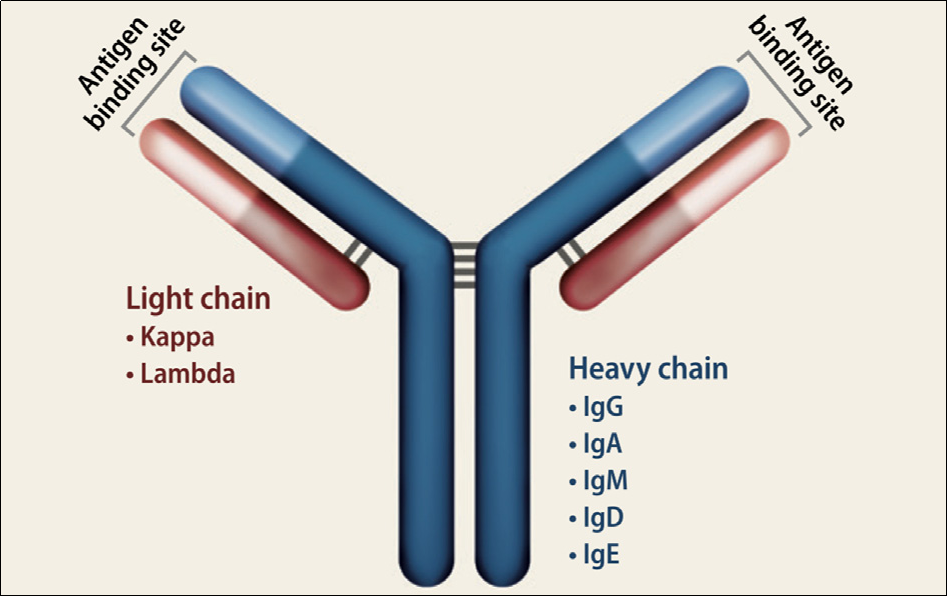
그림 1. 면역글로불린(Ig) 분자의 구조와 유형 [2]
면역글로불린(Ig)의 유전자 재배열 및 항체 다양성
면역글로불린(Ig)은 두 개의 동일한 Light-chain과 두 개의 동일한 Heavy-chain으로 구성되어 있으며, 항체쇄관(Interchain)의 이황화 재결합 (disulfide bond)과 비공유 결합 상호작용(Non-covalent interaction) 그리고 유연한 경첩부위(Hinge region)를 통해 Y 형태의 구조로 연결됩니다. [3-4] 면역글로불린(Ig)의 각 Light-chain과 Heavy-chain에서 가변 영역(Variable region)과 불변 영역(Constant region)을 포함하고 있으며, 그중 가변 영역(Variable region)은 특정 항원을 인식하고 결합하는 역할을 합니다. 항체 다양성은 주로 이러한 가변 영역(Variable region)의 서열 차이에 의해 발생하며, 이를 통해 B 세포는 다양한 항원을 인식할 수 있습니다. 포유류 동물의 면역글로불린(Ig)에서 κ Light-chain과 λ Light-chain을 포함하고 있으며, 이 두 가지 Light-chain의 기능에 큰 차이가 없지만 개별 B 세포는 한 종류의 Light-chain만을 발현할 수 있습니다. κ Light-chain과 λ Light-chain의 비율은 생물종에 의해 다릅니다. 인체에서 κ Light-chain과 λ Light-chain의 비율은 약 2:1이며, 마우스 체내에서는 이 비율이 약 20:1로, 대부분의 마우스 B 세포는 κ Light-chain을 발현합니다. [5]
가변 영역 다양성은 면역글로불린 재배열 과정, 즉 V(D)J 재조합을 통해 더욱 향상됩니다. 이 과정에서 B 세포 수용체를 인코딩하는 유전자들이 재배열되어 독특한 면역글로불린을 생성합니다. 항체를 인코딩하는 gene segment(Ig gene loci)는 주로 가변 영역(V)과 불변 영역(C)으로 구성됩니다.
가변성이 높은 V 가변 영역은 V 유전자(variable gene), D 유전자(Diversity gene), J 유전자(Joining gene)를 포함하고 이 유전자들이 DNA의 무작위 재배열에 의해 서로 연결되고 상대적으로 보존된 불변 영역(C)과 연결되어 다양한 유형의 항체를 암호화(encode)합니다 [6].
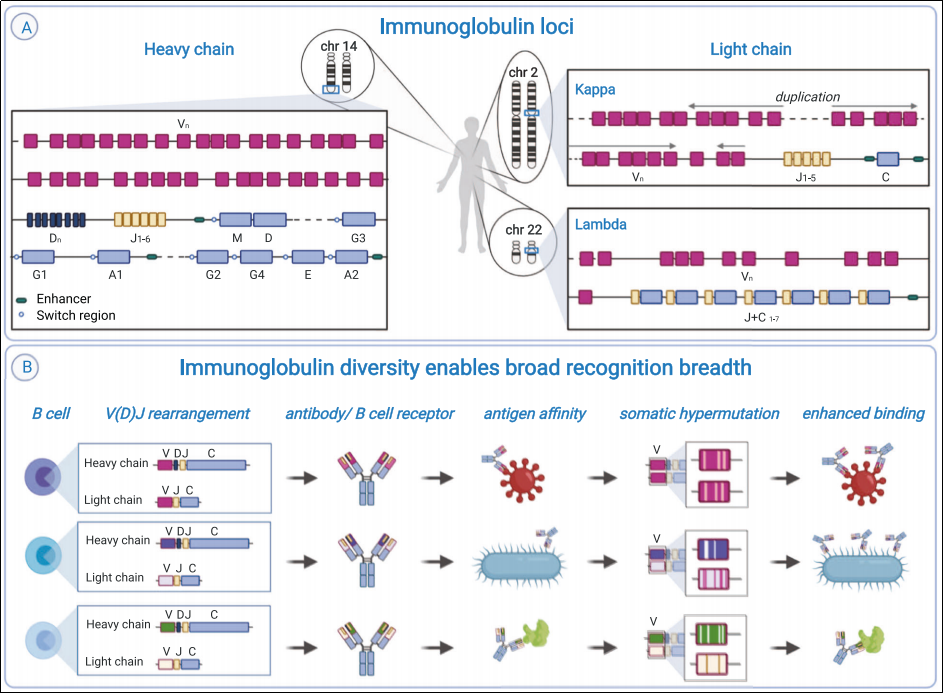
그림 2. 면역글로불린(Ig) Light-chain 및 Heavy-chain의 gene loci 재배열이 서로 다른 항원 특이성을 가진 항체와 BCR을 형성합니다. [7]
B 세포 발달과 질환에서 λ Light-chain의 역할
B 세포 발달 과정에서 유전자 재배열을 통해 기능적인 B세포 수용체(BCR)가 형성됩니다. B 세포는 κ Light-chain 유전자를 우선으로 재배열하고, λ Light-chain(Igλ)은 κ Light-chain(Igκ)의 대체물로 작용합니다. 이 메커니즘은 Igκ 재배열이 실패하더라도 B 세포가 여전히 기능적으로 다양한 항체를 생성할 수 있도록 보장하며, 이는 항체 레퍼토리의 다양성과 기능성을 유지하는 데 중요합니다. [8-10] λ Light-chain(Igλ)은 BCR의 일부분으로 특정 항원에 결합할 수 있어, 이를 통해 B 세포의 활성화와 plasma 세포 및 기억 B 세포(memory B cell)로의 분화를 촉진합니다.
λ Light-chain(Igλ)의 비정상적인 재배열 또는 기능 장애는 전신 홍반 루푸스(Systemic lupus erythematosus, SLE), 류마티스 관절염과 같은 자가면역 질환을 일으킬 수 있으며, 다발성골수종(Multiple myeloma, MM) 및 경쇄 아밀로이드증(AL amyloidosis) 등 B 세포 악성종양과도 관련이 있습니다. [11-13]
또한, λ Light-chain(Igλ)의 결손 또는 이상은 저감마글로불린혈증(Hypogammaglobulinemia), 종합 면역기능 저하증(Common Variable Immune Deficiency, CVID), 일차 면역결핍 질환(Primary Immunodeficiency Diseases, PIDD) 등이 이에 해당되어, 일반적으로 면역글로불린(Ig) 수치가 낮고 감염에 대한 취약성이 이어집니다. [14-16]
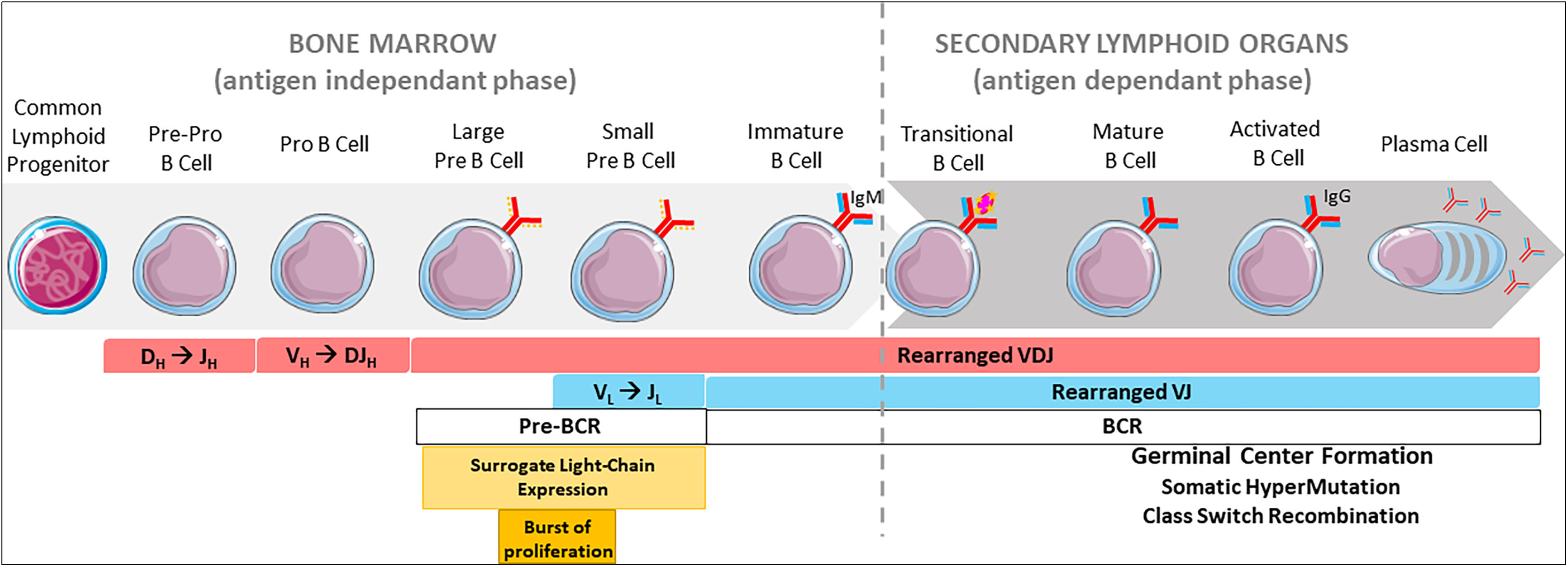
그림 3. B 세포 발달 중 면역글로불린(Ig)의 재배열 과정. [10]
B6-Igl KO 마우스 모델 개발
λ Light-chain(Igλ) 및 κ Light-chain(Igκ) gene loci에는 D 유전자가 없으며 V, J, C 유전자 구간만 포함되어 있습니다. Cyagen은 유전자 편집 기술을 이용하여 마우스 λ Light-chain gene locus(Igl) 내에서 V, J, C 구간을 인코딩하는 모든 유전자 서열을 제거(Knockout)하여 B6-Igl KO 마우스(제품 번호: C001550)를 개발하였습니다. 그 결과, B6-Igl KO 마우스 모델은 λ Light-chain(Igλ)을 더 이상 발현하지 않으며, B 세포는 κ Light-chain(Igκ)만을 특이적으로 발현합니다. 아래는 B6-Igl KO 모델에 대한 세부 정보입니다.
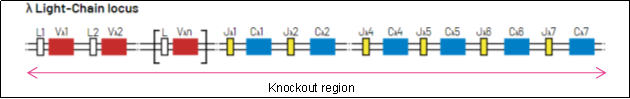
그림 4. B6-Igl KO 마우스의 유전자 Knockout 전략 다이어그램.
Wild-type(WT) 마우스에서는 B 세포가 주로 κ Light-chain(Igκ)을 발현하며, 소수의 B 세포가 λ Light-chain(Igλ)을 발현하는 것으로 나타났습니다. 반면, B6-Igl KO 마우스는 λ Light-chain gene locus(Igl)가 제거(Knockout)되어 B 세포가 κ Light-chain(Igκ)만 특이적으로 발현하며, λ Light-chain(Igλ) 발현은 검출되지 않았습니다.
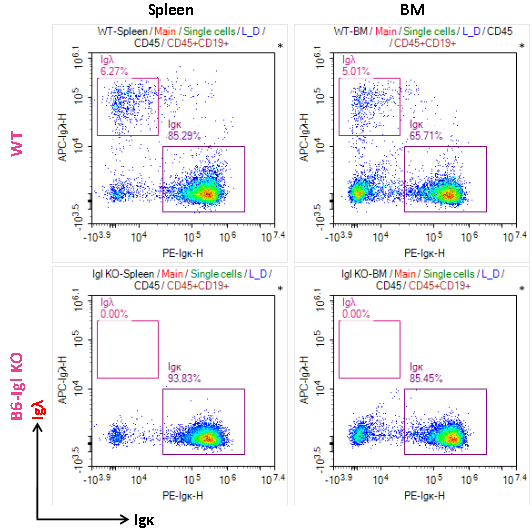
그림 5. Wild-type(WT) 마우스 및 B6-Igl KO 마우스의 비장과 골수에서 면역글로불린 λ Light-chain(Igλ) 또는 κ Light-chain(Igκ)을 발현하는 B 세포의 비율.
모델 요약 및 연구 응용
λ Light-chain gene locus (Igl)의 결실로 인해, B6-Igl KO 마우스(제품 번호: C001550)의 B 세포는 오직 κ Light-chain(Igκ)을 발현합니다. 따라서 이 모델은 오직 κ Light-chain(Igκ)만 포함하는 마우스 항체를 제작하는 데 사용될 수 있으며, λ Light-chain(Igλ)이 B 세포 발달과 기능에서 차지하는 역할을 연구할 수 있으며, 특정 면역 반응 또는 자가면역 질환에서 λ Light-chain(Igλ)과 관련된 메커니즘을 분석하는 데도 유용합니다. B6-Igl KO 모델은 항체 다양성, 면역 시스템 조절, 잠재적인 치료 방법을 탐구하는 데 가능성을 제공합니다.
B6-Igl KO 마우스는 인간화된 Light-chain 마우스 모델과 교배하여 human-specific Light-chain을 발현하는 마우스를 개발할 수 있으며, 이를 통해 연구 및 치료 개발을 위한 완전 인간 항체를 제작할 수 있습니다. 또한, 마우스 항체 서열이 없는 경우, 다른 유형이나 species-specific 항체 서열을 마우스 모델에 삽입하여 in vivo 연구를 진행할 수 있습니다.
Cyagen은 면역학 및 인간 항체 연구 분야에서 다양한 유전 질환 모델, 유도성 질환 모델, 타겟 인간화 모델, 완전 인간 항체 마우스 모델을 개발하였습니다. 이러한 모델은 연구자들에게 다양한 질환에 대한 타겟 치료제 및 항체 약물 개발할 수 있는 중요한 연구 모델입니다.
|
제품 번호 |
모델명 |
품종 계통 |
응용분야 |
|
C001413 |
C57BL/6NCya |
Development and screening of CTLA4-targeted inhibitors/antibody drugs; Evaluation of the efficacy and safety of CTLA4-targeted inhibitors/antibody drugs; Assessment of tumor immunotherapy and research on immune system mechanisms; Research on autoimmune diseases. |
|
|
C001419 |
C57BL/6JCya |
Development and screening of CD47-targeted inhibitors/antibody drugs; Evaluation of the efficacy and safety of CD47-targeted inhibitors/antibody drugs; Assessment of tumor immunotherapy and research on tumor immune evasion mechanisms. |
|
|
C001420 |
C57BL/6NCya |
PDL1 (aka CD274)-targeted drug development, screening, and evaluation of efficacy and safety; Assessment of tumor immunotherapy; Research on the immune system and tumor immune evasion mechanisms. |
|
|
C001524 |
C57BL/6JCya |
Immune checkpoints, tumor research. |
|
|
C001272 |
C57BL/6NCya |
Factor XI deficiency, Hemophilia C (Rosenthal syndrome); related to blood clotting disorders |
|
|
C001400 |
C57BL/6JCya |
Research on metabolic diseases such as atherosclerosis and hyperlipidemia; Studies on angiogenesis and endothelial cell adhesion; Development and screening of ANGPTL3-targeted drugs. |
|
|
C001401 |
C57BL/6NCya |
Research on the mechanisms and pathways of immunoglobulins; Studies on the development and screening of IgG antibody drugs; Research on tumor proliferation, migration, and chemotherapy resistance; Studies on diseases such as chronic lymphocytic leukemia and amyloidosis. |
|
|
C001421 |
C57BL/6NCya |
Research on the pathogenic mechanisms and drug development screening for obesity and type 2 diabetes; Study of other metabolic diseases such as cardiovascular and myocardial diseases; Research on neuroprotective effects in neurological diseases. |
|
|
C001492 |
C57BL/6NCya |
Development and evaluation of ALB-targeted drugs; Design and evaluation of albumin-based drug carriers; Research on ALB-related metabolic diseases. |
|
|
C001497 |
C57BL/6JCya |
Development of migraine treatment drugs, efficacy, and safety evaluation; Research on vascular biology and blood pressure regulation; Study of cell proliferation and apoptosis; Research on tumor growth inhibition and inflammation; Investigation of hematopoietic stem/progenitor cell generation and differentiation. |
|
|
C001500 |
C57BL/6NCya |
Research on antibody-dependent cell-mediated cytotoxicity (ADCC); Study of immune system phagocytosis and antigen presentation; Assessment of affinity, pharmacology, and efficacy of IgG antibody drugs based on FcγRI receptors. |
|
|
C001523 |
C57BL/6JCya |
Migraine drug development, efficacy, and safety evaluation; Vascular biology and blood pressure regulation research; Cell proliferation and apoptosis studies; Tumor growth inhibition and inflammation research; Hematopoietic stem/progenitor cell generation and differentiation research. |
|
|
C001520 |
C57BL/6JCya |
Heart disease, diabetes, anorexia, colorectal cancer, prostate cancer, etc. |
|
|
C001521 |
C57BL/6NCya |
Arteriosclerosis, hyperlipidemia, thrombotic cardiovascular disease. |
|
|
C001522 |
C57BL/6NCya |
Arteriosclerosis, hyperlipidemia, thrombotic cardiovascular disease. |
|
|
C001325 |
C57BL/6NCya |
Immunology Research; T Cell Activation and Antigen Recognition Research; Immunosuppressive Therapy Research for Autoimmune Diseases |
|
|
C001326 |
BALB/cAnCya |
Immunology Research; T Cell Activation and Antigen Recognition Research; Immunosuppressive Therapy Research for Autoimmune Diseases |
|
|
C001542 |
C57BL/6NCya |
Lp(a) cardiovascular disease, atherosclerosis, hyperlipidemia, thrombotic cardiovascular disease. |
|
|
CR004 |
Sprague-Dawley |
Hypertension drug screening model. |
|
|
I001192 |
C57BL/6JCya |
Metabolic dysfunction-associated fatty liver disease (MAFLD), Metabolic dsfunction-asociated seatohepatitis (MASH). |
Cyagen은 HUGO(Humanized Genomic Ortholog) 프로젝트를 시작했으며, 신약 개발을 지원하는 혁신적인 완전 인간화 모델을 개발하기 위해 협력할 글로벌 파트너를 모집하고 있습니다.
HUGO-GT™ 차세대 인간화 모델
HUGO-GT™(Genomic Ortholog for Gene Therapy) 마우스 모델은 기존의 연구 모델에 비해 보다 높은 수준의 인간화를 제공하며, 특히 안티센스 올리고뉴클레오티드(ASO), CRISPR, siRNA(small interfering RNA)와 같은 유전자 서열 완전성을 요구하는 유전자 치료 약물을 평가하는 데 효과적인 모델로 적용됩니다.
Cyagen의 HUGO-GT™ 전체 게놈 인간화 마우스 모델은 IP Issue에 대한 걱정 없이 광범위한 intervention 타겟을 포함하고, 병원성 유전자 돌연변이 부위를 완전히 커버할 수 있는 독점적인 TurboKnockout-Pro 기술을 기반으로 개발되었습니다. HUGO-GT™ 모델 내의 완전 인간화된 타겟 유전자들은 인간이 가진 병원성 유전자와 일치하며, 대부분의 약물 타겟을 포괄하여 다양한 종류의 전임상 약물 실험에서 스크리닝 효율성을 크게 향상시킵니다.

완전 인간 항체 발굴을 위한 HUGO-Ab™ 마우스
HUGO-AbTM(HUmanized Genomic Ortholog for Antibody Development) 마우스는 항체 발굴 모델에서 비약적인 발전을 이루었습니다. 이 마우스는 항체 가변 부위에 in vivo 완전 인간화 유전자가 있어 고친화도와 저면역원성을 가진 완전 인간 항체를 제작할 수 있습니다.
항체 발굴을 위한 HUGO-Ab™ 마우스
High-throughput 완전 인간화 항체 발굴 플랫폼
Cyagen의 HUGO-Ab™ 마우스와 Biointron의 AbDrop™을 결합하는 High-throughput 플랫폼을 통해 완전 인간화된 항체를 최대 3개월 이내에 발굴할 수 있습니다. 이 혁신적인 완전 인간 항체 발굴 플랫폼은 복잡한 유전자 편집이 없이 비용을 절감하고, 보다 안전하고 효과적인 항체 치료제 개발을 가속화합니다.

참고 문헌:
[1] PEDIAA. (2024, September 5). What is the Difference Between B Cell Receptor and Antibody.
https://pediaa.com/what-is-the-difference-between-b-cell-receptor-and-antibody/
[2] Batko K, Malyszko J, Jurczyszyn A, Vesole DH, Gertz MA, Leleu X, Suska A, Krzanowski M, Sułowicz W, Malyszko JS, Krzanowska K. The clinical implication of monoclonal gammopathies: monoclonal gammopathy of undetermined significance and of renal significance. Nephrol Dial Transplant. 2019 Sep 1;34(9):1440-1452.
[3] Wilson IA, Stanfield RL. 50 Years of structural immunology. J Biol Chem. 2021 Jan-Jun;296:100745.
[4] Schroeder HW Jr, Cavacini L. Structure and function of immunoglobulins. J Allergy Clin Immunol. 2010 Feb;125(2 Suppl 2):S41-52.
[5] Larijani M, Chen S, Cunningham LA, Volpe JM, Cowell LG, Lewis SM, Wu GE. The recombination difference between mouse kappa and lambda segments is mediated by a pair-wise regulation mechanism. Mol Immunol. 2006 Mar;43(7):870-81.
[6] Giudicelli V, Chaume D, Lefranc MP. IMGT/GENE-DB: a comprehensive database for human and mouse immunoglobulin and T cell receptor genes. Nucleic Acids Res. 2005 Jan 1;33(Database issue):D256-61.
[7] Mikocziova I, Greiff V, Sollid LM. Immunoglobulin germline gene variation and its impact on human disease. Genes Immun. 2021 Aug;22(4):205-217.
[8] Pieper K, Grimbacher B, Eibel H. B-cell biology and development. J Allergy Clin Immunol. 2013 Apr;131(4):959-71.
[9] Derudder E, Cadera EJ, Vahl JC, Wang J, Fox CJ, Zha S, van Loo G, Pasparakis M, Schlissel MS, Schmidt-Supprian M, Rajewsky K. Development of immunoglobulin lambda-chain-positive B cells, but not editing of immunoglobulin kappa-chain, depends on NF-kappaB signals. Nat Immunol. 2009 Jun;10(6):647-54.
[10] Bruzeau C, Cook-Moreau J, Pinaud E, Le Noir S. Contribution of Immunoglobulin Enhancers to B Cell Nuclear Organization. Front Immunol. 2022 Jun 24;13:877930.
[11] Sternke-Hoffmann R, Pauly T, Norrild RK, Hansen J, Tucholski F, Høie MH, Marcatili P, Dupré M, Duchateau M, Rey M, Malosse C, Metzger S, Boquoi A, Platten F, Egelhaaf SU, Chamot-Rooke J, Fenk R, Nagel-Steger L, Haas R, Buell AK. Widespread amyloidogenicity potential of multiple myeloma patient-derived immunoglobulin light chains. BMC Biol. 2023 Feb 3;21(1):21.
[12] Attaelmannan M, Levinson SS. Understanding and identifying monoclonal gammopathies. Clin Chem. 2000 Aug;46(8 Pt 2):1230-8.
[13] Cleveland Clinic. (2024, September 5). Hypogammaglobulinemia.
https://my.clevelandclinic.org/health/diseases/25195-hypogammaglobulinemia
[14] Barandun S, Morell A, Skvaril F, Oberdorfer A. Deficiency of kappa- or lambda-type immunoglobulins. Blood. 1976 Jan;47(1):79-89.
[15] Collins AM, Watson CT. Immunoglobulin Light Chain Gene Rearrangements, Receptor Editing and the Development of a Self-Tolerant Antibody Repertoire. Front Immunol. 2018 Oct 8;9:2249.
[16] Stiehm's Immune Deficiencies (Second Edition). (2024, September 5). Immunoglobulin Lambda Chain.
https://www.sciencedirect.com/topics/immunology-and-microbiology/immunoglobulin-lambda-chain




영업일 기준 1-2일 내에 답변해 드리겠습니다.