

어셔 증후군(USH, Usher Syndrome)은 내이 및 망막 기능에 중요한 역할을 하는 유전자의 돌연변이로 인해 청력과 시력을 모두 잃게 되는 유전 질환입니다. 어셔 증후군(USH)의 가장 일반적인 subtype은 어셔 증후군 II형(USH2)입니다. USH2A 유전자 돌연변이로 유발된 어셔 증후군 IIA형(USH2A)은 전체 USH2 사례의 절반 이상을 차지하며, 진행성 퇴행성 안질환인 망막색소변성증(RP, Retinitis Pigmentosa)과 밀접한 관련이 있습니다. [1-2]
현재 어셔 증후군 II형(USH2) 치료에 대한 연구는 주로 CRISPR 및 안티센스 올리고뉴클레오티드(ASO)와 같은 새로운 접근법이 포함한 Exon Skipping 및 유전자 편집 기술에 집중하고 있습니다. [2]
효과적인 치료법에 대한 시급한 필요를 해결하기 위해, Cyagen은 전임상 연구를 위한 정밀한 플랫폼을 제공하는 첨단 USH2A 인간화 마우스를 개발하였습니다. 이러한 인간화 질환 모델은 Exon Skipping 및 유전자 편집 치료법의 개발을 가속화하는 데 도움이 되며, 어셔 증후군(USH) 치료법 연구에 중요한 연구 모델입니다.
어셔 증후군(USH) 소개
어셔 증후군(USH)은 유전성 난청-망막색소변성증 증후군으로도 알려져 있으며, 발생 빈도가 약 5,000명 중 1명에서 16,000명 중 1명 정도로 보고 됩니다. 모든 유형의 USH는 열성 유전 방식으로 유전되며, I형과 II형이 가장 흔합니다. 어셔 증후군(USH) 환자는 일반적으로 경증에서 중등도의 청력 손실을 겪으며, 성인기에 망막색소변성증(RP) 증상을 보입니다. 어셔 증후군(USH)은 진행성과 진단의 어려움으로 인해 진단되지 않은 경우가 많아 실제 발생 빈도는 현재 추정치보다 더 높을 수 있습니다.
현재 어셔 증후군(USH) 치료에 대한 연구는 주로 안티센스 올리고뉴클레오티드(ASO) 및 CRISPR 같은 새로운 접근법을 포함한 Exon Skipping 및 유전자 편집 기술에 중점을 두고 있습니다.[2] USH2A 유전자에서 400개 이상의 다양한 돌연변이가 어셔증후군 II형(USH2) 환자에서 확인되었으며, 이는 전체 USH2 사례의 절반 이상을 차지합니다.
Cyagen은 USH2A를 타겟으로 하는 Exon Skipping 및 유전자 편집을 활용하는 치료법의 연구 및 평가를 위해 인간화 USH2A(hUSH2A) 마우스 모델을 개발했습니다.
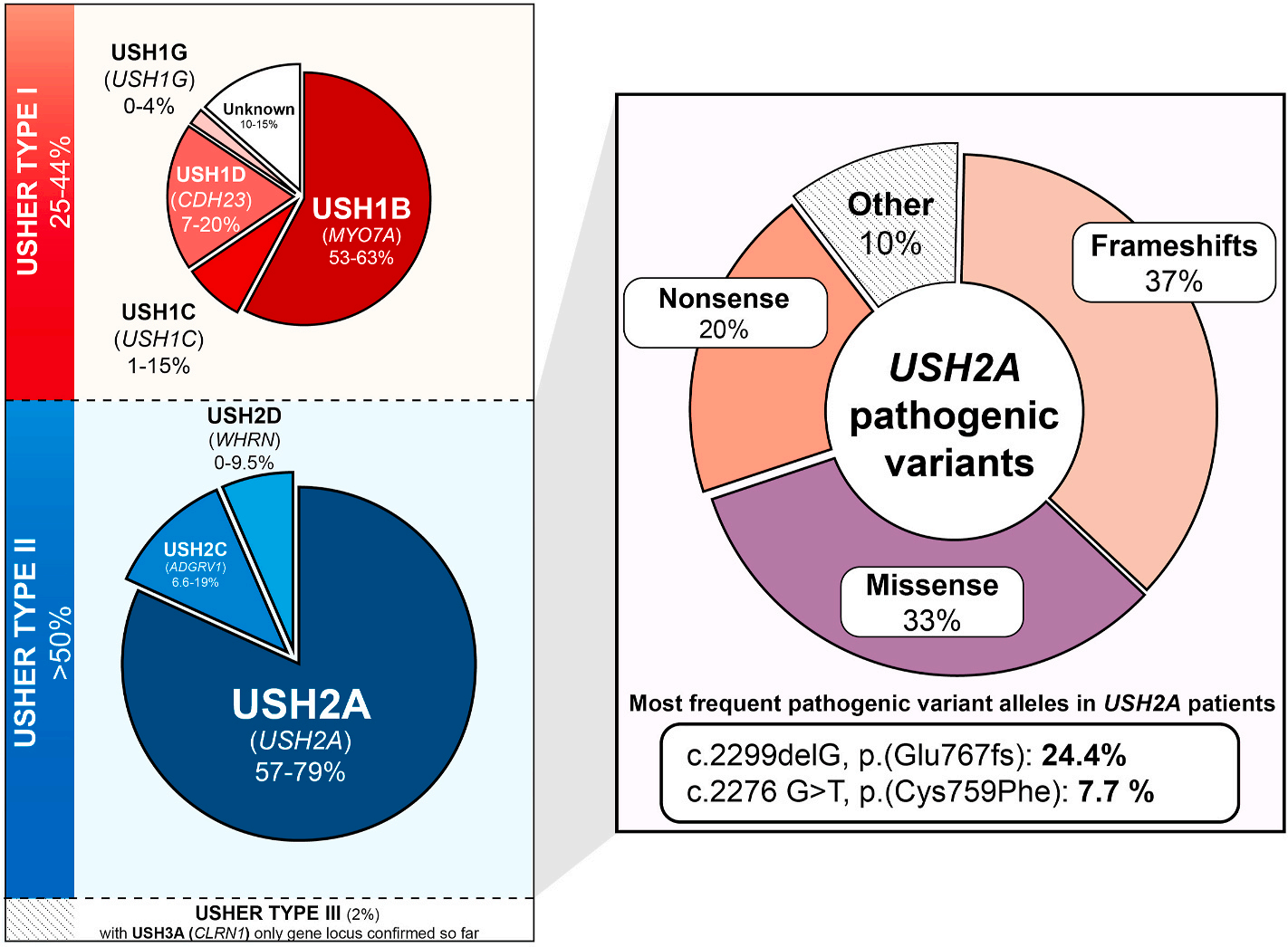
그림 1. USH2A는 어셔 증후군(USH) 에서 가장 흔한 병원성 유전자 돌연변이입니다. [2]
어셔 증후군(USH) 연구를 위해 USH2A를 타겟으로 하는 이유
어셔 증후군 II형(USH2)은 어셔 증후군(USH)의 가장 일반적인 subtype으로, 어셔 증후군 II형(USH2) 환자의 약 57%~79%가 Usherin 단백질을 암호화하는 USH2A 유전자에 돌연변이를 가지고 있습니다. Usherin 단백질은 내이와 망막의 발달 및 항상성 유지에 필수적인 역할을 합니다. [2-3] Usherin 단백질은 laminin EGF-like 모티프, 펜타펩타이드(pentapeptide) 도메인, 그리고 여러 fibronectin type III 모티프를 포함하고 있으며, 주로 기저막에서 발현됩니다. Usherin 단백질은 내이 털세포(hair cell)의 발달과 청각 신호 전달에 중요한 역할을 하며, 망막 기저막에서는 fibronectin과의 상호작용을 통해 부착 기능을 조절합니다. [2-3] USH2A 유전자에서 발생하는 돌연변이는 절단된 Usherin 또는 domain-deleted 단백질을 생성하여 정상적인 단백질 기능을 방해하고, 내이 털세포의 정상적인 발달을 방해하며 망막 기저막에서의 fibronectin 조합에 이상을 초래합니다. 결과적으로 이는 난청과 망막색소변성증(RP) 증상을 유발합니다.
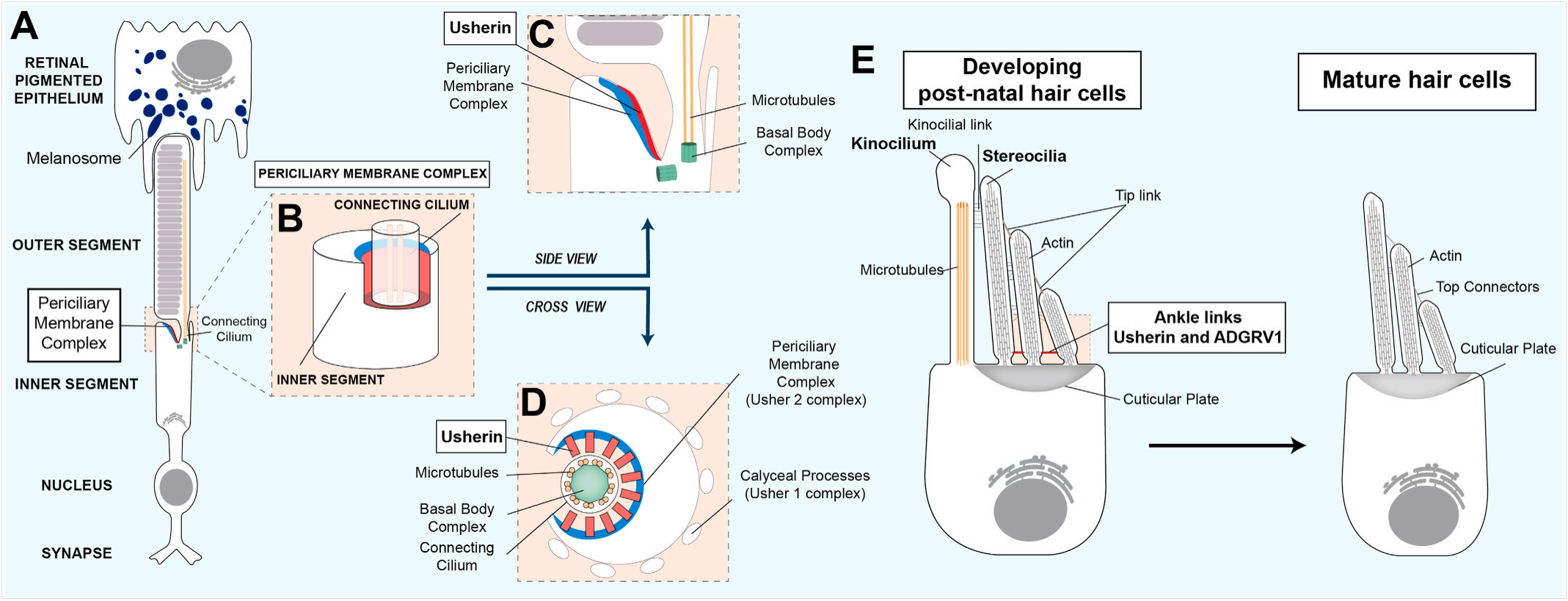
그림 2. USH2A로 암호화된 Usherin 단백질이 광수용체 세포 및 털세포에서의 위치와 기능을 보여줍니다. [2]
현재까지 USH2에 대한 승인된 치료법은 없으며, 진행 중인 치료법 연구는 주로USH2A 유전자 타겟팅에 중점을 두고 있습니다. 가장 큰 도전 과제는 USH2A 유전자의 크기(800k bp 초과)와 그 코딩 서열(CDS)(15k bp 초과)이 커서 기존의 아데노연관바이러스(AAV) 벡터 운반 용량을 초과한다는 점입니다. 따라서 연구자는 USH2와 관련된 병원성 돌연변이의 hotspot 부위인 USH2A 유전자 exon 13을 타겟으로 삼았으며, 이 부위에서 두 가지 흔한 돌연변이인 c.2299delG와 c.2276G>T는 ASO-mediated Exon Skipping과 CRISPR 기반 유전자 편집 등 치료법의 주요 타겟입니다. [2, 4-6]
현재 많은 연구가 USH2A 유전자 exon 13에 집중하고 있으며, 안티센스 올리고뉴클레오티드(ASO)와 유전자 편집을 기반으로 한 치료법은 유전자 편집을 통해 돌연변이를 수정하거나 ASO-mediated Exon Skipping을 통해 정상적인 Usherin 단백질 발현을 복원하는 것을 목표로 하고 있습니다. [7-9]
인간과 마우스의 유전적 차이를 고려하고 안티센스 올리고뉴클레오티드(ASO)와 유전자 편집 치료가 인간 USH2A 유전자를 타겟으로 한다는 점에서 Cyagen은 B6-hUSH2A(E10-15) 인간화 마우스 모델(제품 번호: C001554)을 개발하였습니다. 이 모델은 인간 USH2A exon 13을 포함하고 있어 상기 언급한 치료법을 효과적으로 평가하고 임상 시험으로 발전시킬 수 있는 이상적인 연구 모델입니다.
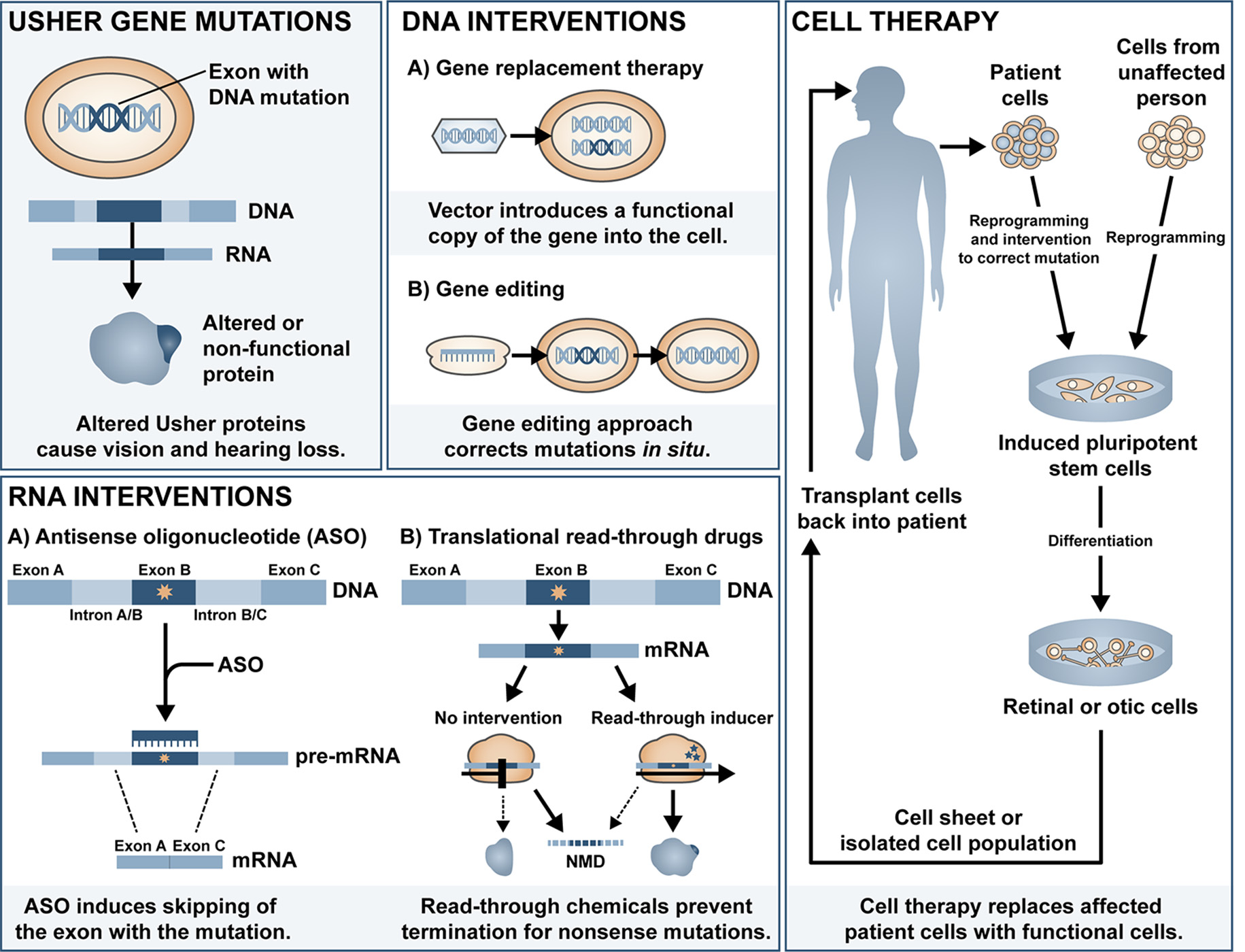
그림 3. 현재 유전자 편집 치료와 ASO-mediated Exon Skipping은 USH 치료를 위한 주요 연구 방향입니다. [9]
B6-hUSH2A(E10-15) 인간화 마우스 모델 구축 방법
마우스 Ush2a 유전자의 ATG(start codon)는 exon 1에 위치한 반면, 인간 USH2A 유전자의 ATG(start codon)는 exon 2에 위치합니다. 따라서 인간 USH2A 유전자의 exon 13은 마우스 Ush2a 유전자의 exon 12에 해당합니다. B6-hUSH2A(E10-15) 인간화 마우스 모델(제품 번호: C001554)은 마우스 Ush2a 유전자의 exon 9~14와 해당 flanking sequence를 인간 USH2A 유전자의 exon 10~15와 해당 flanking sequence로 대체하여 개발되었습니다.
B6-hUSH2A(E10-15) 모델은 인간 USH2A 유전자의 exon 13을 정확히 발현할 수 있으며, 해당 exon의 flanking sequence를 인간화합니다. 유전자 시퀀싱 결과에 따르면, B6-hUSH2A(E10-15) 모델에서 Ush2a 유전자가 인간 USH2A 유전자의 해당 염기서열로 대체되었으며, 해당 염기서열은 인간 USH2A 유전자의 참조 염기서열과 일치합니다. 따라서 B6-hUSH2A(E10-15) 모델은 안티센스 올리고뉴클레오티드(ASO) 및 CRISPR 기반 치료와 같은 인간 USH2A를 타겟으로 하는 연구에 적합한 모델입니다.
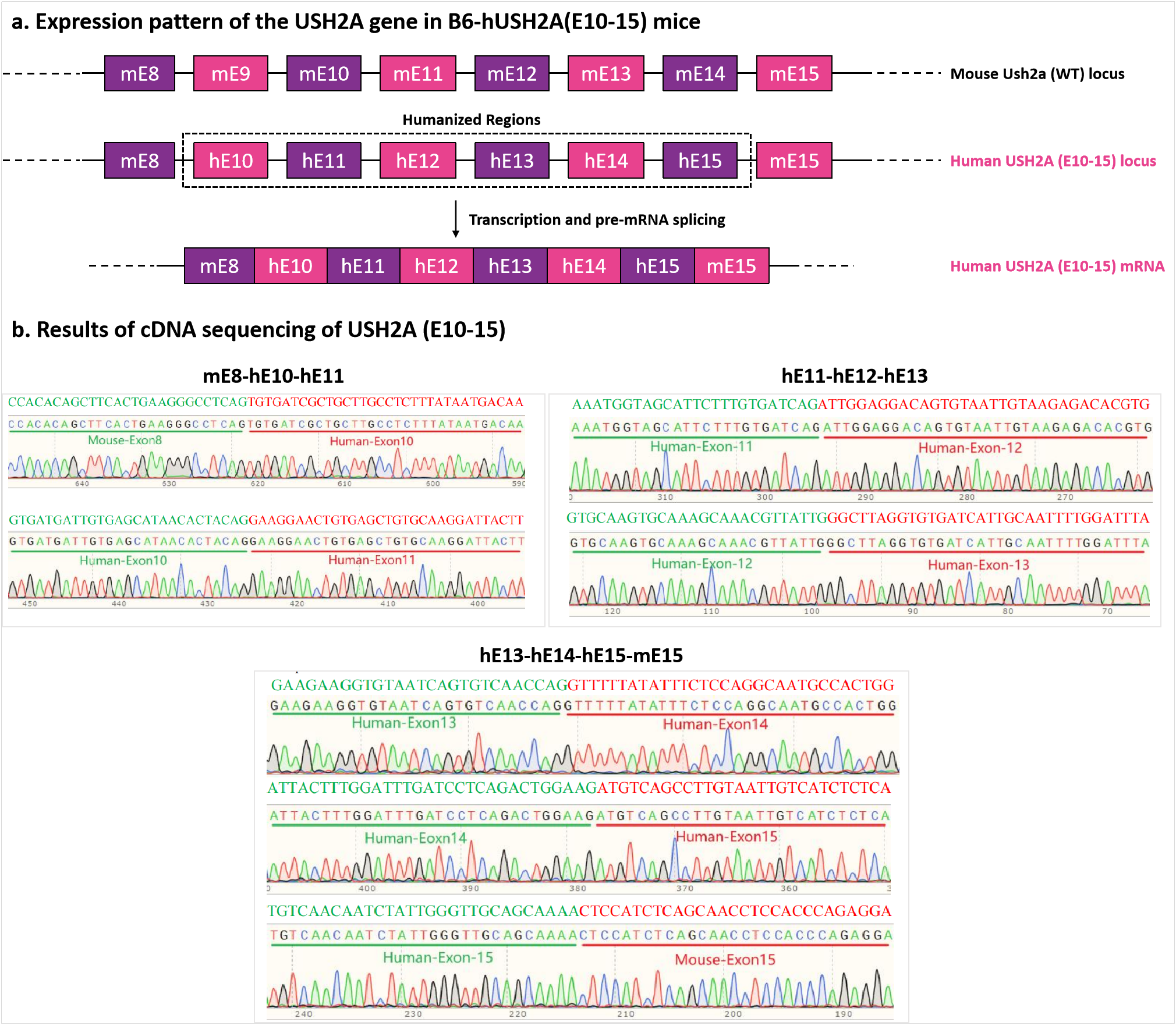
그림 4. B6-hUSH2A(E10-15) 마우스 모델의 인간화 전략과 Regional Sequencing 분석 결과
B6-hUSH2A(E10-15) 마우스 모델에서 인간 USH2A 유전자는 wild-type(WT) 형태로 발현되기 때문에, 이 모델은 wild-type(WT) 마우스와 동일한 건강한 표현형(정상적인 망막 형태, 망막 혈관, 그리고 광수용체 기능)을 나타냅니다.
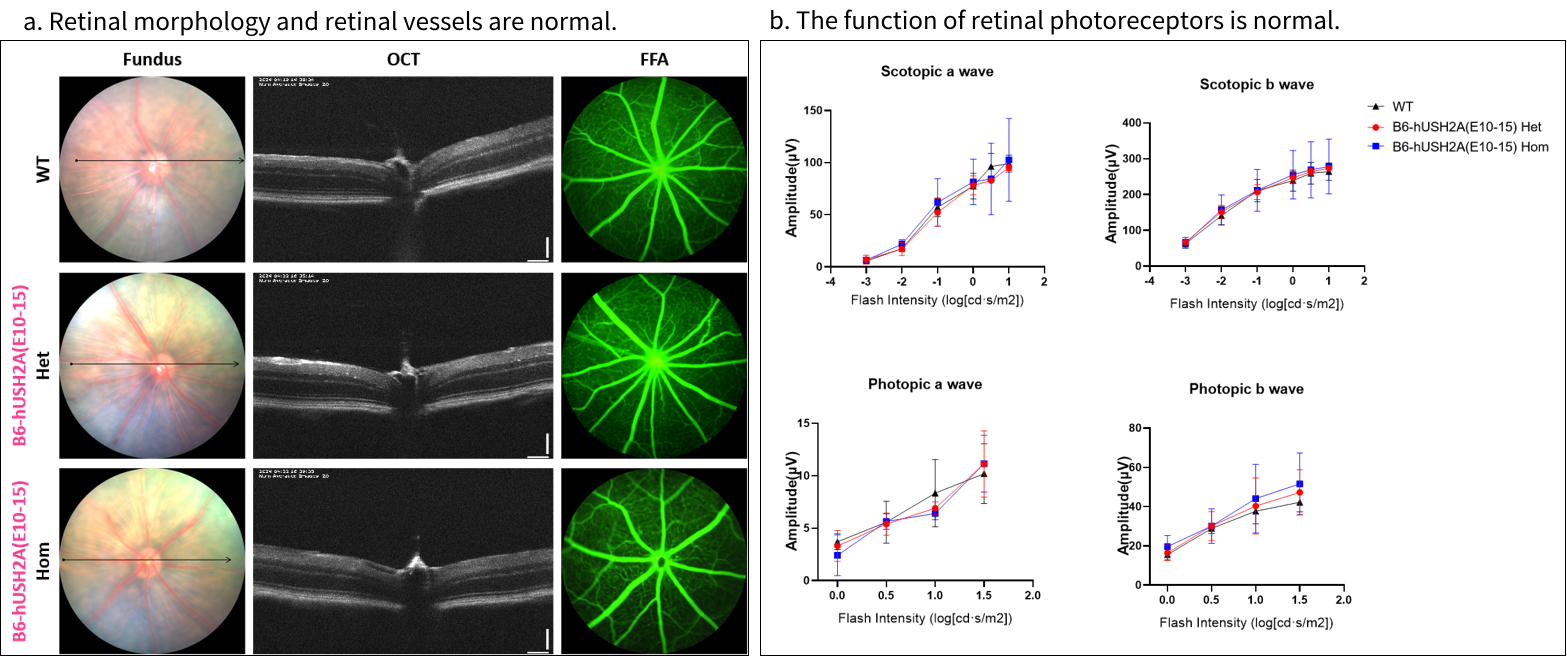
그림 5. 야생형(WT) 마우스와 B6-hUSH2A(E10-15) 마우스의 안저 형태(Fundus), OCT 검사, 현광안저조영술(FFA), 망막전위도(ERG) 결과
현재 USH2A를 타겟으로 하는 치료법 연구 개발은 주로 exon 13 및 그 주변 부위에 집중되어 있으며, 안티센스 올리고뉴클레오티드(ASO)와 CRISPR 유전자 편집과 같은 기술을 활용하고 있습니다. B6-hUSH2A(E10-15) 인간화 마우스 모델(제품 번호: C001554)은 인간 USH2A 유전자를 성공적으로 발현하며, 정상적인 망막 형태와 기능을 유지합니다. 이 모델은 인간 USH2A 유전자의 참조 서열과 완전히 일치하기 때문에 안티센스 올리고뉴클레오티드(ASO) 및 CRISPR 유전자 편집을 포함한 인간 USH2A 유전자 타겟팅 치료법 연구를 위한 중요한 플랫폼으로 활용됩니다. 또한, Cyagen은 B6-hUSH2A(E10-15) 모델을 기반으로 가장 흔한 USH2 병원성 돌연변이(c.2299delG)를 가진 인간화 질환 모델을 개발하여 인간 질환 표현형을 시뮬레이션하고, 정밀 치료법 개발의 필요를 충족하고 있습니다. 관심 있으신 연구자는 추가 정보를 문의하실 수 있습니다.
Cyagen은 망막 질환 분야에서 다양한 유전 질환 모델, 유도성 질환 모델, 인간화 모델을 개발하며, 종합적인 안과 CRO 서비스를 제공합니다. Cyagen의 USH2A 인간화 질환 모델 또는 종합적인 안과 CRO 서비스에 대해 더 알고 싶으시면 문의해 주시기 바랍니다.
|
제품 번호 |
모델명 |
응용 분야 |
타겟팅 유형 |
|
C001395 |
Age-related Macular Degeneration (AMD), Diabetic Retinopathy (DR) |
Humanization(TG) |
|
|
C001396 |
Retinitis Pigmentosa (RP) |
Humanization(KI) |
|
|
C001384 |
Retinitis Pigmentosa (RP), Congenital Stationary Night Blindness (CSNB) |
KO |
|
|
C001385 |
Retinitis Pigmentosa (RP), Age-related Macular Degeneration (AMD), Macular Dystrophy (MDs) |
KO |
|
|
C001386 |
Retinal Degeneration (RD) |
KO |
|
|
C001387 |
Retinal Degeneration (RD), Leber Congenital Amaurosis 2 (LCA2) |
KO |
|
|
C001360 |
Leber Congenital Amaurosis 2 (LCA2) |
Mu |
|
|
C001425 |
Enhanced S Cone syndrome, ESCS; Retinitis pigmentosa, RP |
KO |
|
|
- |
The Complement System |
Humanization |
|
|
- |
Leber Congenital Amaurosis Type 10(LCA10) |
Humanization |
Cyagen은 HUGO(Humanized Genomic Ortholog) 프로젝트를 시작했으며, 신약 개발을 지원하는 혁신적인 완전 인간화 모델을 개발하기 위해 협력할 글로벌 파트너를 모집하고 있습니다.
HUGO-GT™ 차세대 인간화 모델
HUGO-GT™(Genomic Ortholog for Gene Therapy) 마우스 모델은 기존의 연구 모델에 비해 보다 높은 수준의 인간화를 제공하며, 특히 안티센스 올리고뉴클레오티드(ASO), CRISPR, siRNA(small interfering RNA)와 같은 유전자 서열 완전성을 요구하는 유전자 치료 약물을 평가하는 데 효과적인 모델로 적용됩니다.
Cyagen의 HUGO-GT™ 전체 게놈 인간화 마우스 모델은 IP Issue에 대한 걱정 없이 광범위한 intervention 타겟을 포함하고, 병원성 유전자 돌연변이 부위를 완전히 커버할 수 있는 독점적인 TurboKnockout-Pro 기술을 기반으로 개발되었습니다. HUGO-GT™ 모델 내의 완전 인간화된 타겟 유전자들은 인간이 가진 병원성 유전자와 일치하며, 대부분의 약물 타겟을 포괄하여 다양한 종류의 전임상 약물 실험에서 스크리닝 효율성을 크게 향상시킵니다.

완전 인간 항체 발굴을 위한 HUGO-Ab™ 마우스
항체 발굴을 위한 HUGO-Ab™ 마우스
High-throughput 완전 인간화 항체 발굴 플랫폼
Cyagen의 HUGO-Ab™ 마우스와 Biointron의 AbDrop™을 결합하는 High-throughput 플랫폼을 통해 완전 인간화된 항체를 최대 3개월 이내에 발굴할 수 있습니다. 이 혁신적인 완전 인간 항체 발굴 플랫폼은 복잡한 유전자 편집이 없이 비용을 절감하고, 보다 안전하고 효과적인 항체 치료제 개발을 가속화합니다.

참고 문헌:
[1]Delmaghani S, El-Amraoui A. The genetic and phenotypic landscapes of Usher syndrome: from disease mechanisms to a new classification. Hum Genet. 2022 Apr;141(3-4):709-735.
[2]Toualbi L, Toms M, Moosajee M. USH2A-retinopathy: From genetics to therapeutics. Exp Eye Res. 2020 Dec;201:108330.
[3]McGee TL, Seyedahmadi BJ, Sweeney MO, Dryja TP, Berson EL. Novel mutations in the long isoform of the USH2A gene in patients with Usher syndrome type II or non-syndromic retinitis pigmentosa. J Med Genet. 2010 Jul;47(7):499-506.
[4]Pendse ND, Lamas V, Pawlyk BS, Maeder ML, Chen ZY, Pierce EA, Liu Q. In Vivo Assessment of Potential Therapeutic Approaches for USH2A-Associated Diseases. Adv Exp Med Biol. 2019;1185:91-96.
[5]Yan D, Ouyang X, Patterson DM, Du LL, Jacobson SG, Liu XZ. Mutation analysis in the long isoform of USH2A in American patients with Usher Syndrome type II. J Hum Genet. 2009 Dec;54(12):732-8.
[6]Dreyer B, Tranebjaerg L, Brox V, Rosenberg T, Möller C, Beneyto M, Weston MD, Kimberling WJ, Cremers CW, Liu XZ, Nilssen O. A common ancestral origin of the frequent and widespread 2299delG USH2A mutation. Am J Hum Genet. 2001 Jul;69(1):228-34.
[7]Dulla K, Slijkerman R, van Diepen HC, Albert S, Dona M, Beumer W, Turunen JJ, Chan HL, Schulkens IA, Vorthoren L, den Besten C, Buil L, Schmidt I, Miao J, Venselaar H, Zang J, Neuhauss SCF, Peters T, Broekman S, Pennings R, Kremer H, Platenburg G, Adamson P, de Vrieze E, van Wijk E. Antisense oligonucleotide-based treatment of retinitis pigmentosa caused by USH2A exon 13 mutations. Mol Ther. 2021 Aug 4;29(8):2441-2455.
[8]Stemerdink M, García-Bohórquez B, Schellens R, Garcia-Garcia G, Van Wijk E, Millan JM. Genetics, pathogenesis and therapeutic developments for Usher syndrome type 2. Hum Genet. 2022 Apr;141(3-4):737-758.
[9]French LS, Mellough CB, Chen FK, Carvalho LS. A Review of Gene, Drug and Cell-Based Therapies for Usher Syndrome. Front Cell Neurosci. 2020 Jul 9;14:183.




영업일 기준 1-2일 내에 답변해 드리겠습니다.