


CRISPR-Pro 시스템은 사용하기 쉽고 강력한 유전자 편집 도구입니다.질병 기초 연구,표적 검증,약물 분자의 고통량 선별(High throughput screening,HTS), 유전성 질환 치료 등에서 점점 더 광범위하게 응용되고 있습니다.이 가운데 CRISPR-Pro을 이용해 유전자녹아웃(KO) 세포를 구축하는 기술이 갈수록 성숙해지고 있습니다.그렇다면 KO세포는 흔히 볼 수 있는 유전자 기능 연구에 사용되는 것 외에 어떤 응용들이 있을까? KO세포가 우리를 위해 어떤 연구문제를 해결할 수 있을까?
질병발병 메커니즘 연구
어떤 질병의 발생 메커니즘을 연구할 때 유전자 기능 (표적) 의 연구가 그 중의 관건입니다.유전자 기능의 체외 연구는 종종 목적 유전자 표현 조절의 세포 모델을 필요로 합니다.만약 유전자 과표현되거나 유전자 녹다운 (Gene knock-down)표현을 해서목적 유전자를 실현하는 gain of function과 loss of function입니다.기술 유전자 유전자 교란에 사용함은 이미 매우 성숙한 loss of function지만 많은 경우 RNAi를 사용한다고 해서 목적 유전자의 표현이 줄어들지는 않거나표현은 감소했지만 세포 생물학 기능의 변화는 검사할 수 없었습니다.이때 KO 세포를 사용해야 하고, CRISPR-Pro 유전자 편집 기술 매개 유전자 녹아웃도 비코딩 영역 유전자 조각에 작용할 수 있습니다.
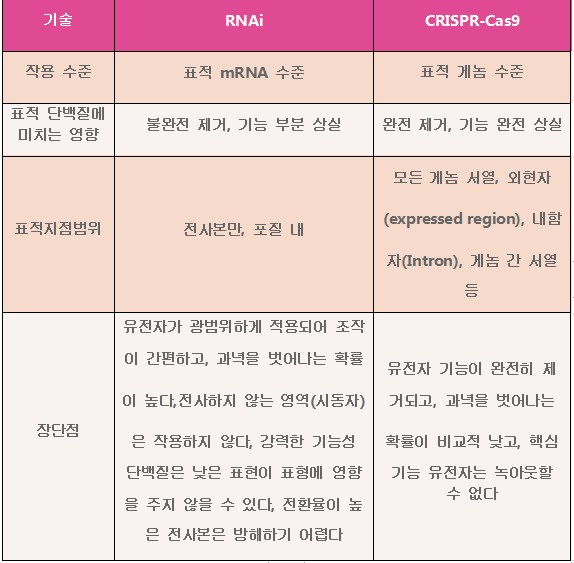
표 1. 유전자 녹다운(Gene knock-down)과 녹아웃 기술 비교
또한, 우리는 설립 된 KO 세포에서 목적 유전자의 과발현을 더 수행 할 수 있습니다.정상 유전자를 보완해 표형을 회복하는 역할을 함으로써 목적 유전자의 기능을 더 충분히 입증할 수 있습니다.KO세포는 우리가 유전자나 신호 통로의 기능을 연구하는 데 도움을 주었고, 최근 몇 년 사이 KO세포로 loss of function 발표를 실현하는 문헌도 많아졌습니다.
약물 표적지의 선별 및 검증
임상에 들어간 것으로 집계돼 현재 연구 단계인 최종 성공에 상장된 약물 비중이 10%약물, 특히 종양 관련 비율이 더낮아 5%밖에 안 됩니다.그중 중요한 원인은 효과적인 약물 표적지가 부족하기 때문입니다.좋은 약물 표적지는 약물의 자금 투입과 개발 주기를 효과적으로 낮출 수 있고 개발 실패 위험도 크게 낮출 수 있습니다.2013년 장봉팀이 Science에서 CRISPR 문고에서 shRNA 문고보다 더 효과적인 선별 결과를 최초로 보도하면서 CRISPR 녹아웃 문고는 세포생존신호, 내성 등의 연구분야에 활용되고 있습니다.현재, 전체 게놈 gRNA 문고를 이용하여 높은 특이성 유전자 표적의 선별을 할 수 있으며, 약 처리 후 사라지거나 농축된 gRNA 에 대해 약물 민감성이나 내성 관련 유전자 표적을 찾을 수 있습니다.
그러나 약물 표적의 선별과 발견은 첫 번째 단계일 뿐 체내 실험을 진행하기 전에 일련의 유효성과 안전 실험을 거쳐야 하기 때문에, 우리는 표적인 KO 를 작용하는 세포주를 건립하고, 약물 처리를 통해 세포 표형이 변하는지 관찰할 수 있습니다.표적지에 따라 이 표적지에 작용하는 약물을 선별하거나 개발합니다 .
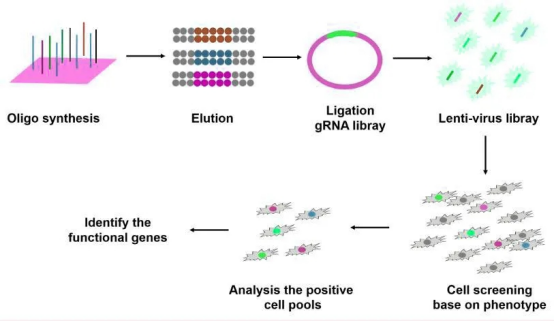
그림 1. gRNA 문고 건립 및 약물 표적지 선별 및 검증
항체 특이성 검증
항체는 우리가 실험에서 가장 많이 사용하는 시약 중 하나로 널리 응용되며,항원-항체반응을 통해 다양한 생명활동 변화를 밝혀낼 수 있습니다.하지만 현재 상업화 항체 특이성,민감성,기능성이 반드시 완전히 검증되는 것은 아니며,다른 상인들이 제공하는 항체 품질도 들쭉날쭉하여 결과의 불일치성을 초래하고 있으며,이로 인해 과학자들은 '재현 위기'를 지속하고 있습니다.KO 세포를 사용하면 항체 특이성을 효과적으로 검증할 수 있고,특이항체 KO 세포는 검증 결과에서 신호를 생성하지 않으며,야생형 세포주는 특이성 단백질 신호를 생성할 수 있으므로, KO 세포는 항체 검증의 좋은 기준품으로 사용되어 항체 특이성을 확인할 수 있습니다.
유전자 치료 연구
유전자 치료는 최근 몇 년 동안 매우 인기 있고 발전도 매우 빠른 방향의 하나입니다. 현재 전 세계에서 이미 수백 개의 유전자 편집자가 지도하는 유전자 치료 임상시험이 진행 중이고, 자주 사용하는 유전자 치료 방식에는 유전자 수정, 유전자 비활성화,유전자 치환 등이 포함됩니다.예를 들어 자가 T세포의 PD-1 유전자를 녹아웃 하는 방법으로 전립선암,식도암,신장세포암을 포함한 암을 치료합니다.BCL11A 의 홍계 특이성 증자를 녹아웃 해 자체홍계 HSC 의 γ글로불린을 올리면 낫 세포병과 베타-지중해빈혈의 잠재적 치료법 등으로 사용할 수 있습니다.이러한 연구나 임상 실험은 모두 CRISPR/Cas9 유전자 녹아웃 기술을 이용하여 이뤄졌습니다.
결론적으로, KO 세포계는 기초연구나 약물 개발 등 분야에서 좋은 응용 전망을 가지고 있습니다.유전자 기능의 완전한 결핍, 게놈의 임의의 세그먼트 조절, 답변 실험의 편리함 등의 장점을 실현할 수 있습니다.질병 메커니즘과 약물 표적지 연구에서 대체 불가한 일환입니다.
Cyagen생물 세포유전자 편집 기술
Smart-CRISPR™
Cyagen생물의 독창적인 Smart-CRISPR™ 기술로 인공지능을 기반으로 한 AlphaKnockout 유전자 편집 전문가 시스템과 CRISPR/Cas9 기술이 독자 개발한 세포 유전자 편집 시스템입니다.일반 CRISPR/Cas9 기술에 비해 유전자 절단 효율이 높고, 세포 이동 코드 돌연변이( frame shift mutation),조각 녹아웃,다중 유전자 녹아웃 등 다양한 녹아웃 전략을 쉽게 실현할 수 있으며,단백질 양성 잔류 등의 문제를 더 잘 해결할 수 있으며,유전자 편집 효율이 크게 향상되어 당신이 빠른 문장을 발표하도록 도와준다.저희에게 연락하여 상담해 주신 것을 환영합니다!

About Cyagen
Cyagen은 15 년 동안 발전해 전 세계 수만 명의 과학자에게 봉사했으며,제품과 기술은 CNS(Cell, Nature, Science) 3 대 저널을 포함한 4500 여 편의 학술 논문에 직접 적용되었습니다.유전자녹아웃, 유전자노크인,조건부 녹아웃 모델 맞춤형 서비스 외에도 Cyagen에는 전문적인 수술질환 모델팀이 있어 다양하고 세밀한 작은 동물수술 질병모델을 제공할 수 있습니다.약물선별평가 마우스 플랫폼은 구미 업계 리더로부터 도입한 면역결핍마우스,심혈관 및 알츠하이머병 등의 연구에 사용되는 인간화 마우스를 제공할 수 있습니다.국제 표준화 무균쥐 기술 플랫폼은 무균마우스,무균동물 맞춤형 서비스,미생물 균군 이식 서비스 등 무균동물 모델에 기반한 각종 제품과 서비스를 제공할 수 있으며, Cyagen의 성숙하고 안정적인 유전자 편집 마우스 플랫폼과 결합하여 균군과 유전자의 상호작용 메커니즘을 연구하는데 도움을 줄 수 있습니다.




영업일 기준 1-2일 내에 답변해 드리겠습니다.