

SARS-CoV-2의 기원에 대한 결론은 아직 정해지지 않았지만, 과학계는 다양한 데이터 증명으로부터 박쥐가 SARS-CoV-2의 최초 전파원일 수 있다는 잠정 결론을 내렸다. 만약 이 관점이 완전히 정확하다면, SARS-CoV-2가 박쥐에서 종간장벽을 넘어 인간으로 전염되는 것은 아마도 쉽지 않은 과정을 거쳐야 할 것이다. 전세계적으로 전염병 발생 상황을 보면, SARS-CoV-2의 감염성은 점차적으로 낮아지는 것이 아니라 지속적으로 높아지고 있다. 그러면 SARS-CoV-2가 박쥐에서 인간에 이르기까지 무엇을 겪었을까? 나중에 사라질 것일까? 다음으로 이러한 문제에 대해 한 번 살펴보고자 한다.
그림1: SARS-CoV-2는 박쥐에서 인간으로
(출처: Thamina Acter et al. 2020)
박쥐는 유일하게 날 수 있는 포유류로 알려져 있다. 박쥐가 수천 종의 바이러스를 가지고 있으며 종간장벽을 넘어 인간에게까지 전염되어 심각한 질병을 일으킬 수 있는 것은 SARS, MERS, Ebola, 그리고 현재 퍼지고 있는 SARS-CoV-2를 포함한다. 먼저 SARS-CoV-2에 대해 자세히 분석한다.
코로나바이러스의 속(genus)인 SARS-CoV-2의 진화는 규칙적이다. SARS-CoV의 출현 초기에 학자들은 코로나바이러스에 대한 연구가 계속되어 왔지만 SARS 사태가 갑자기 터지다가 금방 사라졌기 때문에 바이러스와 관련된 많은 연구 프로젝트가 갑자기 끝나게 되는 바람에 코로나바이러스에 대한 더 깊은 이해가 더 이상 이루어지지 않았다. 2020년 1월에 신종 코로나바이러스 전염병 사태가 터질 때까지에야 SARS-CoV-2가 무엇인지를 대중들이 알게 되었다. 다음으로 우리는 과학적 관점에서 SARS-CoV-2의 기원과 진화를 탐구함으로써 코로나바이러스의 다양성에 대해 알아본다.
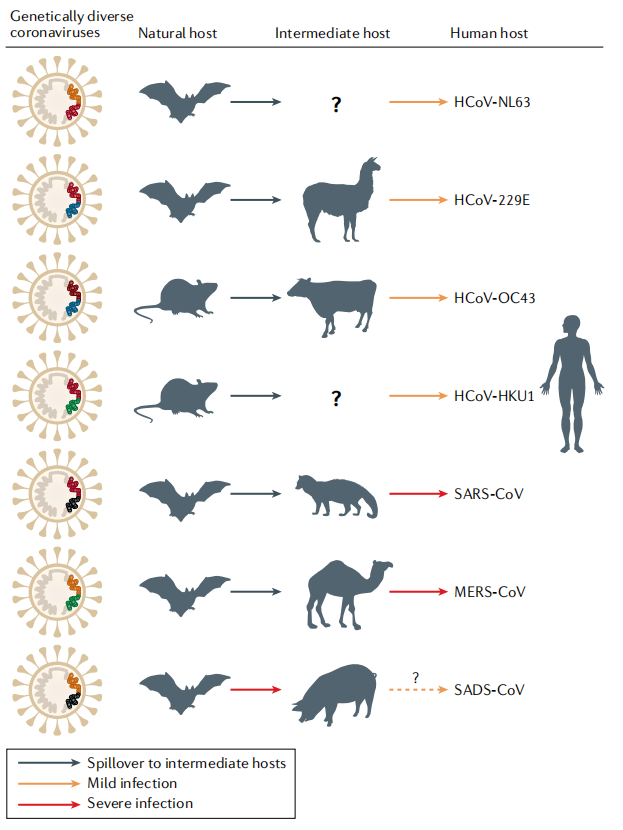
그림2: 인간 코로나바이러스의 동물 기원
(출처: Jie Cui et al. 2019)
우한 바이러스 연구소의 Shi Zhengli 교수는 Nature Review에 코로나바이러스의 기원과 진화에 대해 논술하는 "Origin and evolution of pathogenic coronaviruses"라는 글을 발표했다. 이 글은 사스와 메르스 코로나바이러스 치명률이 높은 원인에 대해 토론하고, 박쥐 유래 코로나바이러스의 다양성 및 종간 전염 가능성을 강조하며, 진화론적 시각에서 코로나바이러스 계통 발달의 관계를 분석해 사스 코로나바이러스가 종간장벽을 넘어 인간에게 전염되는 맥락을 알아냈다. 극적인 것은 이 글은 2019년 3월에 발표된 것으로, 그 당시에는 신종 코로나바이러스 전염병의 발생이 없었으며, 글에서 코로나바이러스에 대한 분류와 다양한 코로나바이러스의 서열 다양성에 대한 해석은 2019년 말에 신종 코로나바이러스 전염병 발생에 대한 조사에 좋은 이론적 근거를 제공했다.
바이러스의 종간 전염은 쉽지 않으며, 박쥐는 겨울에 동굴에서 산다. 이 두 가지의 이유는 바이러스가 종간장벽을 넘으려면 반드시 하나 또는 여러 개의 중간 숙주의 존재가 있어야 한다는 것을 일깨워준다. 그렇다면 바이러스는 종(種)끼리에서의 존재 형식은 같은 것인가? 그렇지 않다. 그림3은 코로나바이러스가 서열 다양성을 가지고 있다는 것을 보여준다.
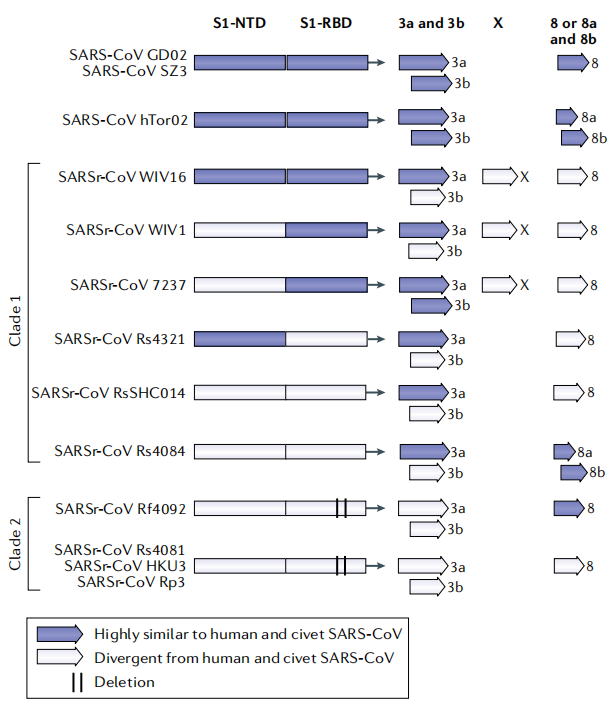
그림3: 코로나바이러스의 서열 다양성
(출처: Jie Cui et al. 2019)
연구가 계속 진행되면서 2020년 3월 베이징대학교 생명 과학 연구소의 연구팀은 National Science Review에서 "On the origin and continuing evolution of SARS-CoV-2"라는 제목의 글을 발표하여 유사한 관점을 증명했다. 이 글은 SARS-CoV-2와 다른 코로나바이러스 사이의 분자 차이를 탐색하고, 게놈 뉴클레오티드 차이로부터 분석했다. 또한 기능단백질의 각 구조적 단위를 다양한 유사한 코로나바이러스와 비교하고, 코로나바이러스 관련 시스템의 분자 발달 트리를 해석하며 SARS-CoV-2의 가능한 변종을 구조적으로 분석했다. 마지막으로, 박쥐 RaTG13 코로나바이러스와 SARS-CoV-2 사이에 단지 4%의 차이가 있는 것으로 밝혀졌다.
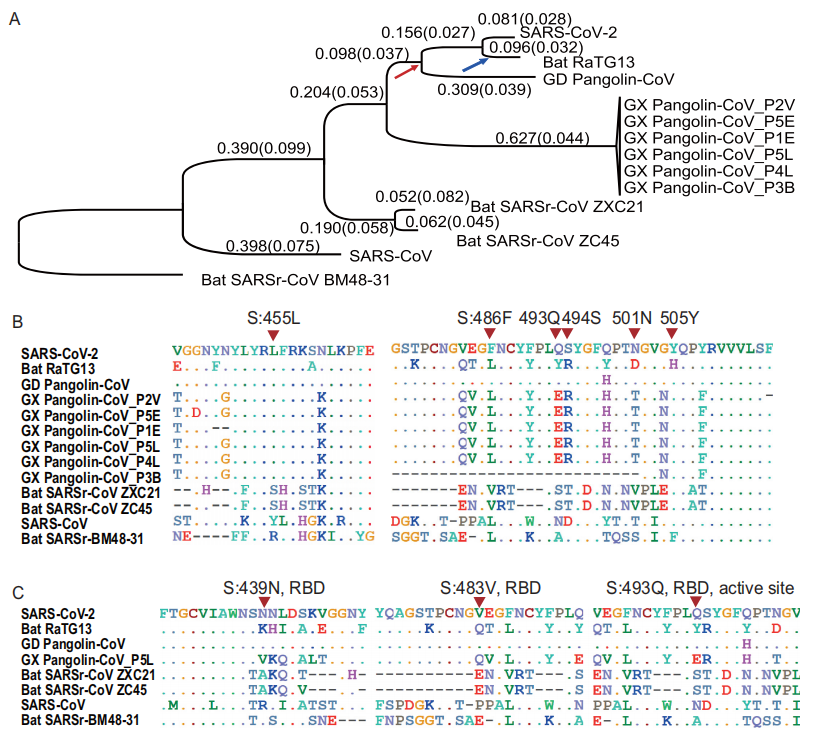
그림4: 코로나바이러스 진화과정에서의 분자발달 및 선택압력
(출처: Xiaolu Tang et al. 2020)
상기는 바이러스 진화 시스템 발달 및 바이러스 기능 분자 시스템 발달의 관점에서 SARS-CoV-2의 가능한 출처 및 코로나바이러스의 다양성을 설명했는데, 이는 바이러스가 종간장벽을 넘어 인간에게 전염될 때 그 자체의 진화 이점을 가져야 한다는 것을 나타낸다. 또한 다른 측면에서 보았을때 감염 과정에서 중요한 역할을 하는 SARS -CoV-2 S 단백질은 어떤 영향을 줄 것인가?
문헌 연구를 통해 계속 분석한 결과, SARS-CoV-2와 다른 종에 감염된 사스 바이러스 사이에 하나의 현상이 존재하는데, 바로 다음 표와 같이 바이러스 S 단백질의 RBM 잔기의 주요 위치에 차이가 있다는 것이다. 자연 진화 과정에서 선별된 5개의 중요한 잔기들은 SARS-CoV-2가 생존할 수 있는 진화적 이점이자 종별 감염표현형의 차이를 만드는 중요한 원인 중 하나이다. 연구에 따르면, 이 5개의 잔기는 숙주 수용체 ACE2가 바이러스에 대한 식별, 바이러스가 숙주 세포에 침입하는 과정에서 중요한 역할을 한다는 것을 증명했다.
표1. 2019-nCoV 및 SARS-CoV의 주요 잔기의 종별 차이
(출처: Yushun Wan et al. 2020)
이러한 진화의 힘은 바이러스가 끊임없이 고등동물을 향해 뛰어넘게 한다. 장기적인 생존과 발전을 위해 바이러스가 끊임없이 자신을 변화시키는 것 외에도 더 많은 외부의 힘을 빌려 자신의 에너지 소모를 줄여야 한다. 예를 들어, SARS-CoV-2가 종간 전염을 성공적으로 하려면 반드시 효과적인 매개체의 매개가 필요하다. 다음으로, 중요한 숙주 매개체인 ACE2 수용체 단백질의 종간 차이를 살펴보고, SARS-CoV-2가 최종적으로 인간에 기생하는 것은 단번에 이루어지는 것이 아니라 끊임없이 스스로를 진화시킴으로써 수용체를 변화시키는 것과 같은 일련의 긴 생물학적 과정을 거친다는 것에 대해 설명하고자 한다.
동물마다 SARS-CoV-2에 감염되는 표현형은 다르다. 일부 동물은 SARS-CoV-2에 취약하는 반면에 일부 동물은 SARS-CoV-2에 취약하지 않다. 왜 그럴까?
SARS 발생 이후 2015년까지 미국 국립보건연구원은 SARS 코로나바이러스에 대해 종별 동물 모델 감염 실험을 실시한 결과 근교계 마우스를 이용하여 제작된 바이러스에 감염된 마우스 모델은 서로 다른 표현형을 갖고 있으나 일반적으로 쉽게 바이러스에 감염되지 않는 것으로 나타났다. 시리아 햄스터 모델을 이용하여 SARS 코로나바이러스 strain별 감염 실험을 진행한 결과 FrK-1 strain 감염으로 인해 햄스터가 제한적으로 사망할 수 있다는 사실을 발견했다. 페럿 모델에서는 인간의 SARS 바이러스 감염과 비슷한 증상이 뚜렷하게 나타나는 반면에 아프리칸그린원숭이(African green monkey), 필리핀원숭이(Macaca fascicularis) 및 붉은털원숭이(Macaca mulatta)와 같은 비영장류 포유 동물에서는 명백한 치명적인 현상을 발견하지 못했다. 후속 연구자들은 SARS-CoV-2를 연구하고 유사한 현상을 또한 발견했다. 이는 SARS-CoV-2에 감염된 다양한 동물의 표현형이 인간의 SARS-CoV-2 감염으로 인한 신종 폐렴이나 다른 증상과 다르다는 것을 보여준다. 이것에 대한 주된 원인은 SARS-CoV-2의 주요 수용체 ACE2의 종간 차이로부터 생각해 보아야 한다.
우리는 ACE2단백질이 SARS-CoV 및 SARS-CoV-2의 주요 수용체이며, ACE2의 구조변화(conformational change) 또는 아미노산의 차이가 바이러스와의 결합능력의 차이로 이어질 수 있다는 것을 알고 있다. 미국 미네소타 대학교 수의학과 및 생물의학과학과 연구팀은 "Receptor Recognition by the Novel Coronavirus from Wuhan: an Analysis Based on Decade-Long Structural Studies of SARS Coronavirus"라는 논문을 공동으로 발표했으며 데이터 분석을 통해 종별 ACE2의 바이러스에 결합하는 주요 잔기의 차이가 있다는 것이 발견되었다. 아래 표와 같이 나와 있다.
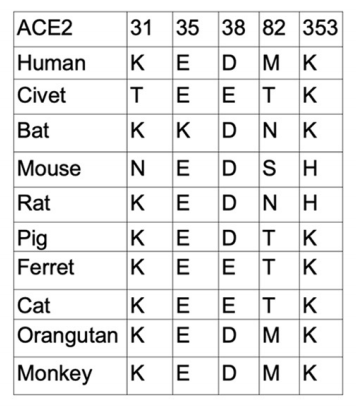
표2. 숙주별 ACE2의 주요 잔기의 차이 비교
(출처: Yushun Wan et al. 2020)
ACE2의 구조변화 또는 주요 잔기의 차이는 바이러스와의 결합능력의 차이로 이어질 것이며, 이는 왜 종별로 SARS-CoV-2의 감염에 대해 다른 감염 특징을 보이는지를 깨닫게 한다.
이처럼 우리는 SARS-CoV-2의 종간 차이를 알게 되었으며 바이러스는 진화 과정에서 아미노산의 돌연변이와 서열의 재조합으로 인해 바이러스의 구조가 더욱 복잡해졌다. 또한 SARS-CoV-2의 주요 숙주 수용체는 종간에 차이가 있기 때문에 바이러스에 대한 각 종별의 감염성, 친화성, 병원성 및 치사율의 차이를 초래한다.
바이러스의 종간 차이를 알면 바이러스의 진화 과정과 진화 방향을 더욱 잘 이해할 수 있으며, 이는 SARS-CoV-2가 박쥐에서 인간으로 넘어가는 중요한 과정이기도 하다. 생존을 위해 바이러스가 지속적으로 적합한 숙주를 찾아 다양하고 복잡한 신체 환경에 끊임없이 적응하면서 마침내 인간에서 살아남는 기회를 발견했다. 물론 기생적인 물질로서 바이러스가 우리를 공격하는 목적은 인간을 파멸시키는 것이 아니라, 사람들에게 그의 존재를 알리는 동시에 생물과 공존하는 최고의 생존 방식을 얻는 것이다. 마지막으로, 여러분이 관심을 가지고 있는 ‘SARS-CoV-2가 사라질까?’라는 질문에 대답해 보고자 한다. 위의 이론적 지식을 알게 되면 이 문제를 더 이상 고민할 필요가 없다고 생각한다. SARS-CoV-2가 사라지지 않으면, 우리는 스스로부터 몸 관리를 잘하고 예방 조치를 취해야 하는 반면에 SARS-CoV-2가 사라지면, 더 많은 신종 바이러스의 출현에 대비해야 한다.
SARS-CoV-2의 정체를 알게 되면, 우리가 해야 할 일은 좋은 예방 시스템을 구축하는 것이며, SARS-CoV-2이든 미래에 나타날 수 있는 신종 바이러스이든 바이러스의 출현 및 가능한 돌연변이에 대비해야 한다. 따라서 동물 모델의 적용이 매우 중요하며, 인간 건강을 보장하기 위해 동물 모델을 통해 인간의 바이러스 감염 증상을 시뮬레이션하여 백신 및 항바이러스 약물을 개발한다.
다음 글에서는 strain별 마우스가 SARS-CoV-2에 감염된 후 어떤 표현형이 나타나는지, 우리가 제작한 SARS-CoV-2 관련 마우스 모델의 장점이 무엇인지 자세히 설명할 예정이니 많은 관심 부탁드립니다.
현재 Cyagen에서 ACE2, DPP4, APN, TMPRSS2 마우스 모델 등을 포함한 여러 코로나바이러스 연구 관련 KO, KI, Humanized 마우스 모델을 제공하고 있으며 특별 할인 행사를 진행하고 있습니다.
| ACE2 / DPP4 | Service | Deliverable | Promotion Price(USD/Strain) |
|---|---|---|---|
| Knockout Mice | ≧3 F1 Heterozygotes | 3,599 | |
| Humanized Mice | 4 F1 Heterozygotes | 5,000 | |
| Knockin Mice (Rosa26) | 4 F1 Heterozygotes | 6,000 |
References:




영업일 기준 1-2일 내에 답변해 드리겠습니다.