

BRGSF(BALB/c Rag2tm1Fwa Il2rgtm1Cgn SirpαNOD Flk2tm1lrl)마우스는 현재 시중에서 면역결핍 정도가 가장 높은 마우스 중 하나이다. Rag2와 Il2rg 유전자의 녹아웃은 BRGSF 마우스의 T, B, NK 세포를 결핍되게 하고, SirpαNOD는 인간유래세포에 대한 마우스 대식세포의 식균작용을 억제하였으며, Flk2유전자의 녹아웃은 마우스 골수세포 구성성분(특히 마우스 수지상세포, Dc)을 크게 감소시켰다(그림 1). 당사는 BRGSF 마우스에 CD34+ 조혈모세포(HSC)를 이식하여 인간의 면역체계(human immune system, HIS)를 재건한BRGSF-HIS 마우스를 제작할 수 있다.
BRGSF-HIS 마우스의 장점 중 하나는 인간유래 림프계세포(예: T, B, NK세포), 인간유래 골수계세포 구성성분(예: 전통적인 수지상세포(cDCs), 형질세포양 수지상세포(pDCs)와 단핵/대식세포)를 포함하는 모든 주요한 인간 조혈모세포 분화 서브세트 구비하는 것이다.
따라서 BRGSF-HIS 마우스는 인간 pDCs에 타겟팅한 항체 개발에 사용될 수 있다.
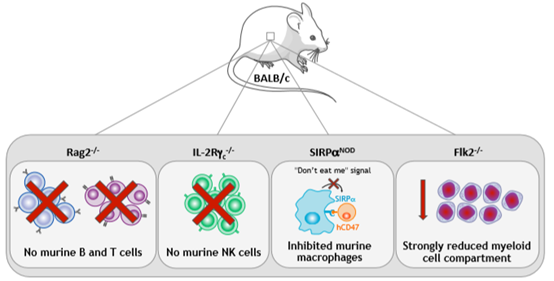
그림 1. BRGSF 중증면역결핍 마우스
수지상세포(dendritic cells, DCs)는 전문적인 항원제시세포(antigen-presenting cell, APC)이자 선천면역(innate immunity)과 적응면역(adaptive immunity)을 연결하는 다리이기도 하다. 수지상세포는 기능과 유래에 따라 클래식한 수지상세포(conventional dendritic cells, cDCs), 형질세포양 수지상세포(plasmacytoid dendritic cells, pDCs), 단핵세포 유래의 수지상세포(monocyte-derived dendritic cells, MoDCs) 및 랑게르한스 세포(Langerhans cells,LCs)로 나눌 수 있다[1].
특히 여기에서 pDC 서브세트는 형질세포양와 유사한 형태를 가지고 있으며 주로 외주 림프기관과 혈액순환 내에 존재하며 Toll-like receptor(TLR): TLR-7과 TLR-9를 통해 핵산을 식별할 수 있다. 활성화된 pDCs는 IFN-α와 IFN-β 위주의 I형 인터페론(INN)을 다량 생성시키기 때문에 천연 인터페론-프로듀싱 세포(natural interferon-producing cells)라고도 한다.[2] 또한 pDCs는 IL-6와 TNF를 포함한 다양한 염증 촉진 세포인자와 케모카인을 분비하여 I형 인터페론과 함께 T, B, NK와 같은 면역세포의 기능을 조절한다. 특히 pDC의 발달은 Flt3-L(Fms-related tyrosine kinase 3-ligand)에 의존하고 있으나 당사의 BRGSF 중증면역결핍 마우스는 Flk2(일명 Flt3) 유전자를 녹아웃하여 이 신호 채널을 차단하여 pDCs를 포함한 골수계 세포 구성성분(특히 DC)의 발육 손상을 초래해 수량이 크게 감소된다. 이로써 HIS된 후 인간 골수계 세포와 상응한 마우스 골수계 세포 간의 경쟁을 감소시켰기에 인간 골수계 세포가 BRGSF-HIS 마우스 체내에서 더 잘 발육하게 된다.
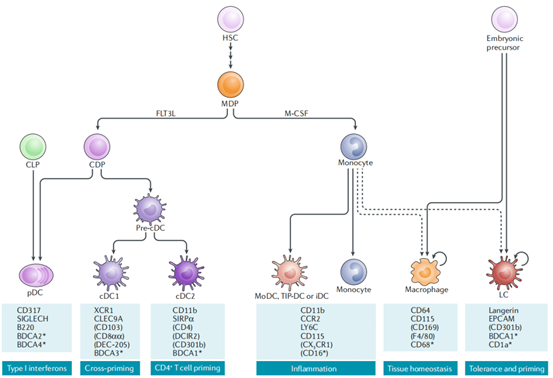
그림 2. DC 서브세트 및 관련 혈통[1]
pDCs는 다양한 종양의 발생과 진행에 관여하고 있다. pDCs는 종양 형질전환(neoplastic transformation)을 발생시켜 모구 형질세포양 수지상세포 종양(Blastic plasmacytoid dendritic cell neoplasm, BPDCN)을 발생시키고, 유방암과 난소암의 침윤성 pDCs는 불량 예후와 관련이 있으며, 골수 미세환경 내 pDCs는 다발성 골수암(multiple myeloma, Mm)에서 종양세포의 성장, 생존 및 약물내성을 촉진할 수 있다[3]. pDCs는 자가면역질환과도 관련이 있다. 비록 유기체에 많은 메커니즘이 있어 pDCs의 자체 물질 식별을 피면하나 여전히 빠져나가는 경우가 발생한다. pDCs는 이러한 자가항원에 대해 다량의 IFNs를 방출하여 자가면역질환을 유발한다.
인간 pDCs는 표면 상 CD123, CD303, CD304 등 분자가 고발현되며 마우스 pDC의 표면 표기는 CD11cintCD11b-B220+SiglecH+CD317+이다[4]. 특히 CD303은 인간 pDCs의 특이성 표지자이며 혈액 수지상세포 항원2(blood dendritic cell antigen 2, BDCA-2)라고도 한다. 따라서 표적 CD303의 항체는 침윤성 pDCs가 관여하는 암, 자가면역질환, 염성질환 치료에 활용될 수 있을 것으로 기대된다.
2018년 Dr.Fournier 등은 일련의 선택과 최적화를 거쳐 인간 Cd303를 타겟팅한 단일클론 항체(mAb)인 ch122A2를 구축했다[5].
In vitro 실험에서 Ch122A2 mAb는 인간 pDCs의 IFN-α 분비량을 낮추는 것으로 나타났다(그림3). 또한 투여량이 1ng/ml일 경우 Biogen사가 개발한 동일한 표적 CD303의 인간화 IgG1 단일클론항체(BIIB059/24F4)보다 사용 효과가 훨씬 좋았다.
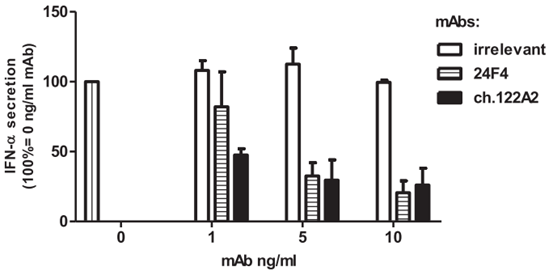
그림 3. Ch122A2 mAb는 인간 pDCs의 CpG 자극 후 IFN-α 분비량을 감소시켰다. 5×104개 인간 pDCs와 1mM CpG 및 농도별 IgG1, 24F4 또는 ch122A2를 공배양한다.
CD303가 pDCs에서만 특이성 발현이 있기 때문에 연구진은 BRGSF-HIS 마우스로 In vivo 실험을 진행했다. BRGSF-HIS 마우스가 인간 다혈통 조혈의 재건을 지원하기 때문에 재건 후 마우스 체내에는 인간유래 림프계 구성성분을 갖고 있을 뿐만 아니라 pDCs 등을 포함한 다양한 인간유래 골수계 세포 구성성분도 가지고 있다.
In vivo 실험 결과(그림 4):
(1) ch122A2 mAb는 BRGSF-HIS 마우스의 외주혈에서 빠르고 강한 인간 pDC 고갈 능력을 가지고 있으며 이 효과는 최소 3일간 유지된다.
(2) ch122A2 mAb는 BRGSF-HIS 마우스의 비장에서 인간 pDC 고갈 능력이 중등 수준이지만 IgG1 mAb 대조군에 비해 여전히 유의미한 차이가 있다.
(3) h122A2 mAb는 BRGSF-HIS 마우스의 골수에서 인간 pDC에 대해 뚜렷한 고갈 능력이 없다.
이와 같은 실험 결과는 ch122A2 mAb가 pDCs의 고갈 및 I형 인터페론 등 염증촉진 세포 인자의 분비 감소를 통하여 환자의 증세를 개선하는 목적에 도달할 수 있는 응용 전망이 밝은 특이성 표적 인간 pDCs 항체 약물이라는 것을 보여준다.
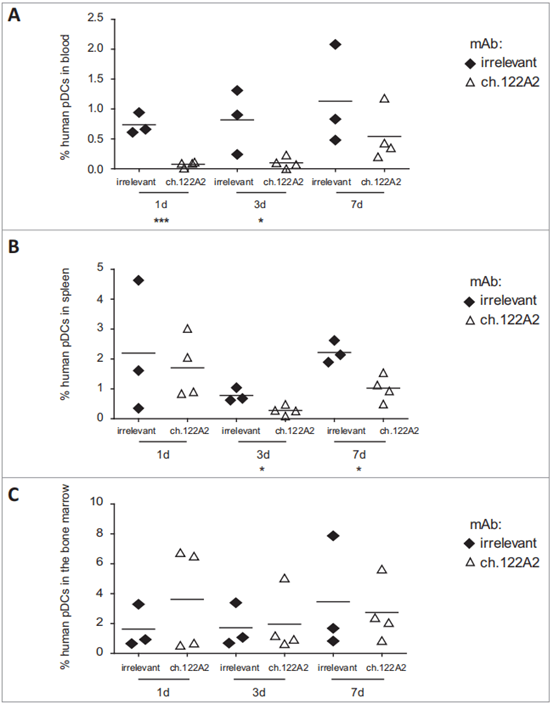
그림 4. BRGSF-HIS 마우스 외주혈(A), 비장(B) 및 골수(C)에서 ch122A2 mAb의 pDC 고갈능력
pDCs는 유기체내 I형 인터페론의 주요 생성세포이며 점점 더 많은 연구 결과에 의하면 자가면역질환과 염성 질환, 예를 들어 피부 홍반성 루푸스(cutaneous lupus erythemtosus, CLE), 전신 홍반 낭창(systemic lupus erythematosus, SLE), 쇼그렌증후군(Sjogren syndrosus)과 연관이 있다. 현재 이와 같은 질환은 모두 치료할 특효약이 없는 상태이다. 앞에서 언급한 표적 pDCs 표면의 특이성 marker인 CD303의 BIIB059/24F4 항체는 현재 임상시험 단계에 있으며 적응증은 CLE와 SLE이다. Biogen이 발표한 임상 2기 실험결과, 플라세보에 비해 BIIB059/24F4 항체는 환자의 증세를 현저히 개선시켜 주며 양자의 심각한 부작용 발생 횟수는 비슷하다. 이와 같은 데이터는 모두 pDCs가 유기체의 면역 반응에서 중요한 역할을 한다는 것을 보여준다.
종양은 인류의 건강을 심각하게 해치는 중대한 질병 중의 하나로, 마우스 종양 모델은 종양 발생 메커니즘 연구, 약물 선별 및 치료 효과 평가에 꼭 필요한 도구이며, Cyagen 모델 동물 혁신 약물 연구 개발 플랫폼은 연구자의 필요에 따라 각종 효과적인 종양 모델, 예를 들면 전통 면역결핍 마우스BALB/c nude(누드 마우스)와 NOD scid, 중증면역결핍 마우스BRGSF와 C-NKG, 면역관문 인간화 마우스, 종양 세포주 이식 모델, Cell Line-Derived Xenograft (CDX) 모델, 유전자 변형 및 표현형 분석 서비스 등을 제공할 수 있다. 당사는 각종 피하, 인시투 혹은 전이종양 모델을 제작할 수 있으며, 그에 상응하는 모델에 대해 고도로 맞춤화된 체내 약효학 서비스를 제공하여 고객의 수요를 만족시킬 수 있다.




영업일 기준 1-2일 내에 답변해 드리겠습니다.