

각막이영양증(Corneal Dystrophy, CD)은 각막에 비정상적인 물질이 침착되어 발생하는 유전성 희귀 질환입니다. 임상적으로 각막이영양증(CD)은 점진적인 각막 투명도 상실로 나타나며, 재발 각막 침식(Recurrent corneal erosion) 및 시력 손실을 초래할 수 있습니다. 과립형각막이상증(Granular Corneal Dystrophy, GCD)은 TGFBI(Transforming Growth Factor Beta Induced) 유전자 변이에 의해 발생하는 각막이영양증(CD)의 일반적인 subtype입니다. [1] TGFBI 유전자가 암호화하는 TGFBIp 단백질은 세포와 콜라겐 사이의 상호작용에 참여하여 세포의 부착, 이동 및 증식 과정에서 중요한 역할을 합니다. TGFBIp 단백질의 돌연변이는 각막 상피 및 기질에 비정상적인 침착을 유발하여 각막 투명도와 디옵터(diopter)를 감소시키며 결국 시력을 손상시킵니다. [1-2]
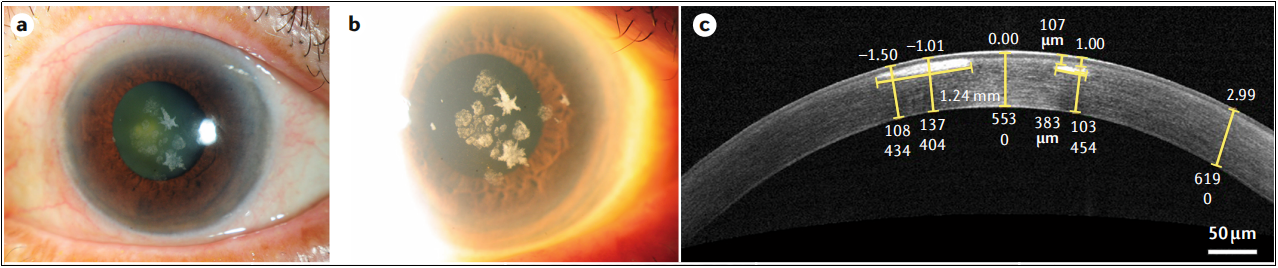
그림 1. 각막 전부(前部) 기질에 침착물이 보인 과립형각막이상증(GCD) 환자의 안구 증상 [2]
각막이영양증(CD) 새로운 치료법의 필요성
각막은 눈의 앞쪽에 위치한 투명한 무혈관 조직으로, 빛을 망막에 집중시키고 눈의 굴절력(refractive power)의 2/3를 제공합니다. 각막이영양증(CD)의 대표적인 병리적 특징은 각막의 각 층에 특정 물질이 축적되는 것으로, 양쪽 눈에 모두 발병하는 경우가 많습니다. 다양한 유형의 각막이영양증(CD)은 다양한 정도의 시력 장애를 초래할 수 있습니다. [3] 현재 각막이영양증(CD)에 대한 근본적인 치료법은 없고, 각막 이식이 기존의 주된 치료법으로 수술 후 재발, 이식 실패, 합병증 및 각막 기증자 부족과 같은 문제에 직면하고 있습니다. 따라서 유전자 치료, 재생 치료, 세포 치료와 같은 새로운 대체 치료법 개발이 미래 각막이영양증(CD) 연구의 중요한 주제가 되고 있습니다. [3-4] TGFBI 관련 각막이영양증(CD)은 가장 흔한 subtype 중 하나이기 때문에, TGFBI 유전자 변이에 의한 각막이영양증(CD) 그리고 이를 타겟으로 하는 치료법이 현재 연구의 주요 초점이 되고 있습니다.

Figure 2. 정상 TGFBIp 단백질 및 돌연변이 TGFBIp 단백질의 서로 다른 수송 및 침착 패턴 [4]
RNA Interference와 유전자 편집 위주의 TGFBI-Targeted 치료법
TGFBI 유전자가 암호화하는 TGFBIp 단백질은 세포의 부착, 이동, 증식 및 분화를 매개함으로써 다양한 생리적 및 병리적 반응에서 중요한 역할을 합니다. TGFBIp는 각막, 피부, 결합 조직에서 발현되어 콜라겐과의 결합을 통해 각막의 세포외 기질 구조적 지지를 제공합니다. [5] TGFBI의 돌연변이는 각막에 비정상적인 물질 침착을 초래할 수 있으며, 돌연변이 유전자의 발현을 억제하는 것이 잠재적인 치료 전략이 될 수 있습니다. SiSaf Ltd에서 개발한 RNA Interference 치료법 SIS-201-CD와 CRISPR-Cas9 유전자 편집 치료법 SIS-201-CDC는 TGFBI 유전자 돌연변이를 억제하거나 편집하여 돌연변이 단백질의 생성 또는 응집을 방지합니다. [6-7] 또한 최근 연구에 따르면 TGFBI는 다양한 암에서 비정상적으로 발현되며, 종양 면역 미세환경에서 면역 억제 효과를 나타냅니다. [8] TGFBI는 종양 세포 증식, 혈관 신생 및 세포 자살에 중요한 역할을 하여 여러 종류의 종양의 침윤 및 전이를 촉진합니다. [8-9] 따라서 TGFBI에 대한 타겟 치료법은 잠재적인 항암 전략이 될 것으로 예상됩니다.
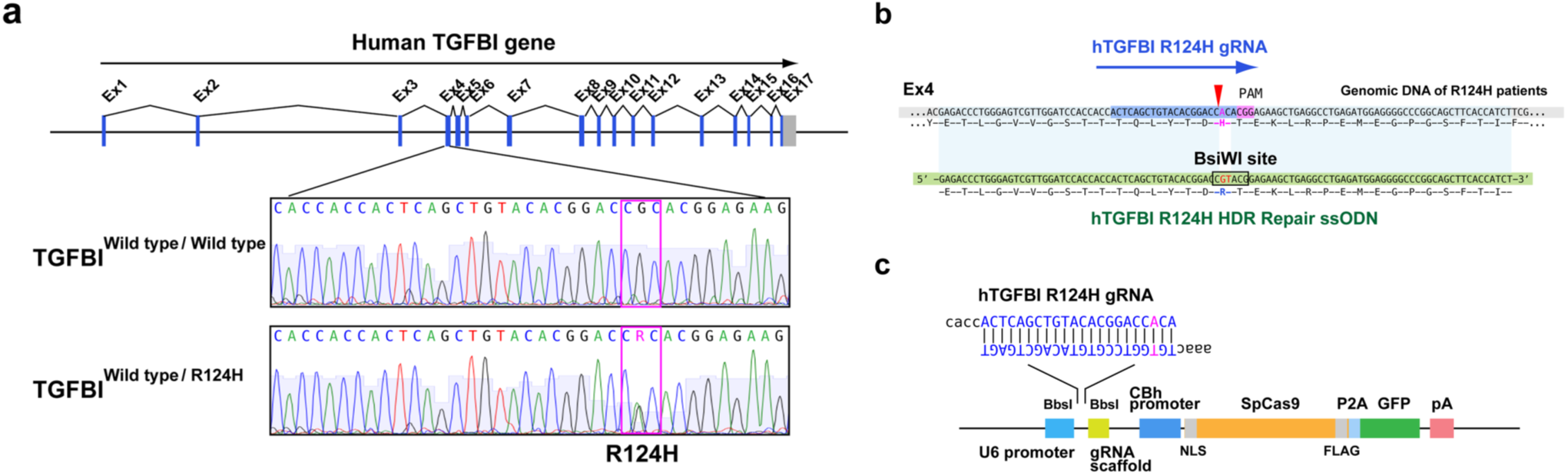
그림 3. 돌연변이 TGFBI 유전자를 타겟으로 하는 유전자 편집 치료의 초기 전임상 세포주 연구. [7]
TGFBI 연구를 위한 B6-hTGFBI 인간화 마우스 모델 소개
RNA Interference 및 유전자 편집 치료법은 모두 인간 유전자를 타겟으로 하지만, 마우스 유전자와 인간 유전자 간의 차이는 임상적 translation 가능성을 제한할 수 있습니다. 이러한 유전적 차이를 극복하기 위해, Cyagen은 마우스 Tgfbi 유전자 서열을 인간 TGFBI 유전자 서열로 대체한 B6-hTGFBI 인간화 마우스 모델(제품 번호: C001546)을 성공적으로 개발하였습니다. B6-hTGFBI 마우스 모델은 인간 TGFBI 유전자를 발현하며 정상적으로 발달하고, 비정상적인 안구 표현형을 나타내지 않습니다. 또한 Cyagen은 B6-hTGFBI 마우스 모델을 기반으로 인간화 Point Mutation 질환 모델을 추가로 개발하여 TGFBI 관련 연구에 유용한 연구 모델을 제공할 예정입니다. 해당 연구에 관심 있으시면 문의해 주세요. 아래는 B6-hTGFBI 마우스 모델의 구체적인 표현형 정보입니다.
인간 TGFBI 유전자의 성공적인 발현
Homozygous B6-hTGFBI 마우스 모델은 간과 안구에서 인간 TGFBI 유전자를 성공적으로 발현하며, 마우스 Tgfbi 유전자를 발현하지 않습니다.
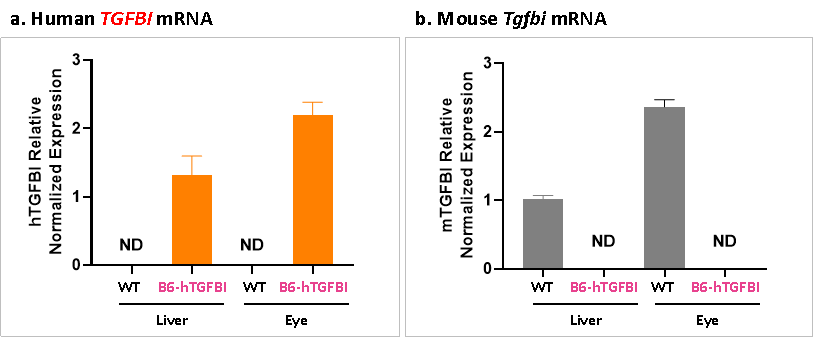
그림 4. B6-hTGFBI 마우스와 wild-type (WT) 마우스의 간과 안구의 유전자 발현 분석 결과
B6-hTGFBI 마우스의 정상적인 안구 형태:
Homozygous 및 Heterozygous B6-hTGFBI 마우스는 wild-type (WT) 마우스와 비교했을 때 각 안구 조직의 형태에 유의미한 차이가 나타나지 않고, B6-hTGFBI 마우스에서 정상적인 안구 표현형이 관찰됩니다.

그림 5. 안저(fundus), 망막 OCT 검사, 각막 및 전방(anterior chamber) OCT 검사 결과
Homozygous 및 Heterozygous B6-hTGFBI 마우스는 암순응(어두운 환경 적응)과 명순응(밝은 환경 적응)에서 ERG의 a-wave와 b-wave 진폭이 wild-type (WT) 마우스와 일치하고 B6-hTGFBI 마우스의 정상적인 망막 광수용체 기능을 의미합니다.
그림 6. wild-type (WT) 마우스와 B6-hTGFBI 마우스의 ERG 검사 결과
요약
B6-hTGFBI 마우스 모델(제품 번호: C001546)은 인간 TGFBI 유전자를 성공적으로 발현하고 더 이상 마우스 Tgfbi 유전자를 발현하지 않으며, 정상적으로 발달하고 비정상적인 안구 표현형을 보이지 않습니다. B6-hTGFBI 마우스의 안구 조직 형태는 wild-type (WT) 마우스와 유의미한 차이가 없으며 정상적인 망막 광수용체 기능을 가집니다. 따라서 B6-hTGFBI 마우스 모델은 TGFBI 관련 각막이영양증(CD) 연구에 이상적인 연구 모델로 RNA Interference 치료제 및 유전자 편집 치료제 후보물질의 스크리닝 및 전임상 검증에 사용할 수 있습니다.
또한, Cyagen은 B6-hTGFBI 마우스를 기반으로 인간화된 Point Mutation 질환 모델을 개발하고 있습니다. 전임상 연구 개발의 필요에 맞추어 다양한 Point Mutation 맞춤형 서비스도 제공하고 있습니다. 아래는 질환 모델링을 위해 Cyagen에서 개발한 HUGO-GT™ 차세대 인간화 모델입니다.
|
제품 번호 |
모델명 |
품종 계통 |
응용 분야 |
|
C001396 |
C57BL/6JCya |
Retinitis Pigmentosa (RP), Congenital Stationary Night Blindness (CSNB), and other retinal diseases. |
|
|
C001410 |
C57BL/6JCya |
Frontotemporal Dementia (FTD), Alzheimer's Disease (AD), and other neurodegenerative diseases. |
|
|
C001418 |
C57BL/6JCya |
Amyotrophic Lateral Sclerosis (ALS), Frontotemporal Dementia (FTD), and other neurodegenerative diseases. |
|
|
C001427 |
C57BL/6NCya |
Parkinson's Disease (PD). |
|
|
C001437 |
C57BL/6NCya |
Spinal Muscular Atrophy with Respiratory Distress Type 1 (SMARD1) and Charcot-Marie-Tooth Disease Type 2S (CMT2S). |
|
|
C001495 |
C57BL/6JCya |
Retinitis pigmentosa (RP), congenital stationary night blindness (CSNB), and other retinal diseases research |
|
|
C001504 |
C57BL/6NCya |
Spinal muscular atrophy (SMA) |
|
|
I001128 |
C57BL/6NCya |
Rett Syndrome (RTT) |
|
|
I001124 |
C57BL/6NCya |
Hutchinson-Gilford Progeria Syndrome (HGPS) |
|
|
C001398 |
C57BL/6NCya |
Spinocerebellar Ataxia Type 3 (SCA3) |
|
|
C001512 |
C57BL/6NCya |
Transthyretin Amyloidosis (ATTR) |
|
|
I001131 |
C57BL/6NCya |
Epilepsy |
|
|
I001132 |
C57BL/6NCya |
Cystic Fibrosis (CF) |
|
|
C001525 |
C57BL/6NCya |
Transthyretin Amyloidosis (ATTR) |
|
|
I001130 |
C57BL/6NCya |
Hepatolenticular Degeneration (HLD) |
|
|
IR1019 |
Sprague-Dawley |
Alexander disease (AxD), traumatic brain injury |
|
|
C001533 |
C57BL/6NCya |
Obesity, metabolic disorders associated with improper fat distribution and storage |
|
|
C001538 |
C57BL/6NCya |
Dystrophic Epidermolysis Bullosa (DEB) |
|
|
C001428 |
C57BL/6NCya |
Epidermolysis Bullosa (EB) |
|
|
C001546 |
C57BL/6JCya |
Corneal Dystrophy (CD) |
|
|
C001551 |
C57BL/6JCya |
Stargardt Disease (STGD) |
|
|
C001554 |
C57BL/6JCya |
Usher Syndrome (USH) |
|
|
C001555 |
C57BL/6JCya |
Age-related Macular Degeneration (AMD); Diabetic Retinopathy (DR); Corneal Neovascularization; Mechanisms of Tumorigenesis and Development, and Development of Antitumor Drugs. |
참고 문헌:
[1] Li Haoliang, Liang Shu. Research progress on TGFBI-related granular corneal dystrophy [J]. Chinese Journal of Clinical Physicians (Electronic Edition), 2020, 14(11): 931-936.
[2]Corneal dystrophies. Nat Rev Dis Primers. 2020 Jun 11;6(1):47.
[3]Han KE, Choi SI, Kim TI, Maeng YS, Stulting RD, Ji YW, Kim EK. Pathogenesis and treatments of TGFBI corneal dystrophies. Prog Retin Eye Res. 2016 Jan;50:67-88.
[4]Vision Center. (2024). Corneal Dystrophy: Symptoms, Types, and Treatments. https://www.nei.nih.gov/learn-about-eye-health/eye-conditions-and-diseases/corneal-conditions/corneal-dystrophies
[5]Nielsen NS, Poulsen ET, Lukassen MV, Chao Shern C, Mogensen EH, Weberskov CE, DeDionisio L, Schauser L, Moore TCB, Otzen DE, Hjortdal J, Enghild JJ. Biochemical mechanisms of aggregation in TGFBI-linked corneal dystrophies. Prog Retin Eye Res. 2020 Jul;77:100843.
[6]SiSaf Ltd. (2024). Pipeline. https://sisaf.com/pipeline/
[7]Taketani Y, Kitamoto K, Sakisaka T, Kimakura M, Toyono T, Yamagami S, Amano S, Kuroda M, Moore T, Usui T, Ouchi Y. Repair of the TGFBI gene in human corneal keratocytes derived from a granular corneal dystrophy patient via CRISPR/Cas9-induced homology-directed repair. Sci Rep. 2017 Dec 1;7(1):16713.
[8]Huang H, Tang Q, Li S, Qin Y, Zhu G. TGFBI: A novel therapeutic target for cancer. Int Immunopharmacol. 2024 Jun 15;134:112180.
[9]Corona A, Blobe GC. The role of the extracellular matrix protein TGFBI in cancer. Cell Signal. 2021 Aug;84:110028.




영업일 기준 1-2일 내에 답변해 드리겠습니다.